Давление в кислородном баллоне: характеристики резервуара
Отправим материал на почту
Техника безопасности
Устройство кислородного баллона очень простое, но надежное. Главное – точно соблюдать параметры закачиваемого внутрь газа, чтобы не произошел разрыв емкости. При эксплуатации и хранении нужно соблюдать некоторые очень жесткие требования.
Заправка кислородом – это сложный процесс, потому что в сварочные баллоны закачивается именно газ. А до распределительной станции он доходит в жидком состоянии. Такой кислород намного безопаснее, чем газообразный, но он быстро и в больших количествах испаряется, что невыгодно в финансовом плане. Но производители идут на такие потери, потому что безопасность превыше всего. Тем более, жидкий кислород транспортируется в больших количествах (авто- и железнодорожные цистерны). Если такой объем загорится и взорвется, то потери будут в несколько раз больше.
Закачка газа в баллоны производится насосным и безнасосным способом. При этом заполнение происходит не переохлажденным кислородом. При любых действиях с баллоном очень важно соблюдать аккуратность и требования техники безопасности. Самое уязвимое место – это вентиль, чаще всего именно он выходит из строя, потому что подвергается многократному открытию и закрытию.
Ремонту он не поддается, можно только поменять на новый. Делать это своими руками запрещено, такую операцию позволяют проводить только в заводских условиях. Здесь важно соблюсти правила установки, в основе которых лежит запрессовка, то есть вкручивание под определенным давлением. Затем сам баллон с вентилем проверяют испытательным давлением. Кстати, тестирование является гидравлическим. Внутрь баллона закачивается вода под давлением 225 или 300 кг/см², которая находится там в течение 5 минут. После чего давление снижают до рабочего – 150 или 200 кг/см².
Необходимо отметить, что по этой же технологии производится проверка самих баллонов на предмет обнаружения протечек. Если ничего не обнаружено: все стыки и стенки не стали мокрыми, значит, испытание прошло успешно, и само устройство может эксплуатироваться дальше.
Источник
Параметры баллона
Кислород при окислении выделяет в атмосферу много тепла. Избыток энергии может спровоцировать возгорание или детонирование (взрыв). Баллоны – безопасный сосуд, который облегчает перемещение при использовании вещества. При выборе емкости обращают внимание на 3 параметра.
Строение
Конструкции для перевозки кислорода делают бесшовным методом из высоколегированных или углеродистых марок стали. Толщина стен у резервуаров – 6-8 мм. Баллоны выполняют в форме цилиндра с закруглением с одной из сторон. У емкости выпуклое днище. В нижней части есть башмак из металлической ленты, который помогает удерживать изделие в вертикальном положении.
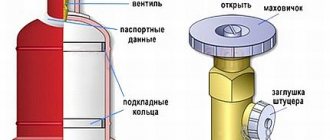
В области горловины располагают кольцо для монтажа колпака безопасности. Устройство устанавливают поверх вентиля. Элемент используют для защиты от попадания внутрь взрывоопасных компонентов, еще ограждает редуктор от механических повреждений.
Важной дополнительной деталью кислородного баллона является вентиль. Устройство создают из латуни. Сплав меди и цинка по химическим показателям намного превосходит другие металлы. У вещества высокая устойчивость к окислению и коррозийным процессам, что необходимо при работе с газом.
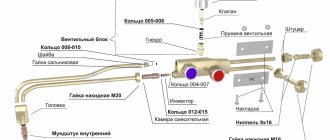
Латунный штампованный вентиль – запорная деталь, благодаря которой элемент подсоединяют к кислородному баллону. В нижней части корпуса расположен хвостовик с резьбой для горловины, сбоку – штуцер для трубки. Между емкостью и элементом вкручивают клапан и муфту с седлом, между компонентами устанавливают уплотнитель из меди.
При вращении вентиля по часовой стрелке механизм закрывает отверстие для газа. При обратном движении клапан поднимается, открывает скважину и кислород начинает выходить. Надежность оборудованию обеспечивает механическое строение конструкции.
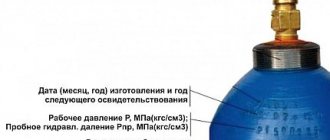
Баллоны по ГОСТу надо окрашивать в голубой оттенок. Черной краской поперек резервуара пишут название газа. На верхней овальной части поверхности выбивают клеймо производителя и информацию о емкости:
Чтобы данные были хорошо видны, верх оставляют неокрашенным. Вес стандартного баллона варьируется от 67 до 105 кг. Масса дополнительных деталей – до 10 кг. Высота у сорокалитровых моделей – 1,37-1,46 м, пятидесятилитровых – 1,68-1,76 м.
Давление
Характеристика давление важна при заправке кислородных баллонов. Профессионалы используют специальную формулу, позволяющую точно определить параметр. В вычислениях учитывают вместительность конкретной модели в кубических дециметрах.
Виды кислорода
Выбор разновидности зависит от задач, которое должно вещество выполнять. Для сварки и резки металла используют недорогое техническое сырье. Состав кислорода обязательно соответствует нормам ГОСТа 5583-48.
Летучий компонент производят методом ректификации низкотемпературной из воздуха. Газ в компрессоре вначале сжимают, потом резко охлаждают до комнатной температуры. В итоге получают концентрированный жидкий кислород. Вещество можно выделять при электролизе воды.
Дополнительно газ делят на 2 сорта, которые отличаются долей разных примесей. В составе технического вида могут содержаться незначительные включения соединений и едва уловимый запах. Характеристики не влияют на работу, поэтому вещество не очищают.
Медицинский вид – концентрированный вариант, в котором нет примесей и посторонних ароматов. Газ поставляют только в новых баллонах, а состав должен полностью соответствовать нормам ГОСТа 5583-48. У сырья очень сложный, дорогостоящий и трудоемкий процесс производства, что отражается на стоимости.
Медицинский сжиженный кислород относят к лечебным средствам, поэтому у производителя должна быть лицензия. Сырье проходит несколько этапов проверки, позволяющие выявить брак на любой стадии. Отличить вид от технического можно по надписи на баллоне и по сопроводительной документации.
Кислород: формула, плотность, масса, свойства, способы получения и применения
Газы: азот, кислород, водород, углекислый газ, аргон
Применение
oxygen
Газообразный кислород сегодня в промышленных масштабах получают из атмосферного воздуха. Его производство актуально и востребовано в наши дни. Существует специальное оборудование, которое позволяет получать кислород в необходимых объемах.
В условиях лаборатории газообразный (а затем и жидкий) кислород наиболее часто получают, используя возможности электролиза водных растворов щелочей. Также существует еще один способ получения небольшого количество кислорода — взаимодействие подкисленного раствора пероксида водорода и раствора перманганата калия.
Газообразный кислород сегодня востребован во множестве профессиональных видов деятельности человека.
Газ кислород
Кислород – один из важнейших элементов на планете. Он участвует в процессе дыхания, в метаболизме живых организмов, а также в круговороте веществ в биосфере. Кроме того, он способствует гниению и разложению органических остатков.
В нормальных условиях он является бесцветным газом, который не имеет вкуса и запаха. Он тяжелее воздуха и с трудом растворяется в воде. В химическом плане он очень активен и способен образовывать соединения практически со всеми элементами.
В свободном состоянии в виде молекул О2, состоящих из двух атомов оксигена, он находится в атмосфере. Благодаря такому строению элемент также называется «дикислородом», но он может существовать и в других вариациях. При определенных условиях его атомы могут образовывать «трикислород» с молекулой О3, которая представляет собой голубой газ озон со специфическим запахом.
В атмосфере содержание кислорода составляет примерно 21 % по массе, в земной коре его доля значительно выше и составляет около 47 % по массе.
Элемент входит в состав более полутора тысяч разнообразных пород и минералов, большая часть из которых являются силикатами. Там он присутствует в виде соединений.
В воде его содержание доходит до 85 %, и это не удивительно, ведь атомы оксигена и образуют воду вместе с элементом гидрогеном.
История открытия
Официально считается, что кислород был открыт английским химиком Джозефом Пристли 1 августа 1774 года путём разложения оксида ртути в герметично закрытом сосуде (Пристли направлял на это соединение солнечные лучи с помощью мощной линзы). 2HgO →ot 2Hg + O2↑
Однако Пристли первоначально не понял, что открыл новое простое вещество, он считал, что выделил одну из составных частей воздуха (и назвал этот газ «дефлогистированным воздухом»). О своём открытии Пристли сообщил выдающемуся французскому химику Антуану Лавуазье. В 1775 году А. Лавуазье установил, что кислород является составной частью воздуха, кислот и содержится во многих веществах.
Несколькими годами ранее (в 1771 году) кислород получил шведский химик Карл Шееле. Он прокаливал селитру с серной кислотой и затем разлагал получившийся оксид азота.
Шееле назвал этот газ «огненным воздухом» и описал своё открытие в изданной в 1777 году книге (именно потому, что книга опубликована позже, чем сообщил о своём открытии Пристли, последний и считается первооткрывателем кислорода). Шееле также сообщил о своём опыте Лавуазье.
Важным этапом, который способствовал открытию кислорода, были работы французского химика Пьера Байена, который опубликовал работы по окислению ртути и последующему разложению её оксида.
Наконец, окончательно разобрался в природе полученного газа А. Лавуазье, воспользовавшийся информацией от Пристли и Шееле. Его работа имела громадное значение, потому что благодаря ей была ниспровергнута господствовавшая в то время и тормозившая развитие химии флогистонная теория.
Лавуазье провёл опыт по сжиганию различных веществ и опроверг теорию флогистона, опубликовав результаты по весу сожжённых элементов.
Вес золы превышал первоначальный вес элемента, что дало Лавуазье право утверждать, что при горении происходит химическая реакция (окисление) вещества, в связи с этим масса исходного вещества увеличивается, что опровергает теорию флогистона.
Таким образом, заслугу открытия кислорода фактически делят между собой Пристли, Шееле и Лавуазье.
Жидкий кислород
Как и другие вещества, кислород может пребывать в различных агрегатных состояниях. Чтобы превратить газ в твердое тело или жидкость, его нужно сильно охладить.
При давлении в 51 атмосферу он становится жидким уже при -119 °C. При нормальном давлении превращение происходит только при -183 °C.
Охлаждаясь до температуры -220 °C, он затвердевает, образуя светло-голубые снегоподобные кристаллы.
В жидком состоянии кислород окрашивается в голубой оттенок и усиливает некоторые свойства газообразного вещества. Так, он ведет себя более агрессивно в химических реакциях, а также становится сильным парамагнетиком и может притягиваться магнитом.
Он закипает только при -183 °C, а плавится при +219 °C. Благодаря устойчивости к столь низким температурам жидкий кислород обладает криогенными свойствами и может использоваться в качестве хладагента.
В нормальных условиях он быстро испаряется, превращаясь в газ. При этом он усиленно поглощает тепло и охлаждает окружающий воздух, отчего рядом с ним появляется ореол тумана. Во время испарения объем кислорода увеличивает в несколько сотен раз.
Так, 1 см3 жидкости образует почти 800 см3 газа.
Сфера использования
Сжатый кислород – популярный газ, область применения которого зависит от вида сырья. Медицинское вещество используют во время реанимации пациентов. Элемент оказывает благоприятное воздействие на сердце и легкие, поэтому часто назначают лечебные процедуры при проблемах со здоровьем. Компонент берут для насыщения коктейлей при кислородном голодании.
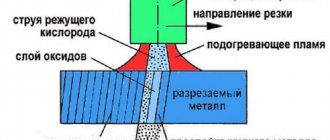
Технический газ быстро нагревается и долго поддерживает высокие температуры. Полученная сплошная струя прожигает металл любой плотности, что позволяет разрезать или спаивать детали. Характеристика полезна как в строительстве, так и в бытовом использовании. В металлургии вещество усиливает КПД печей, чем улучшает качество готовой продукции.
История открытия кислорода
Открытие кислорода приписывают Джозефу Пристли (Joseph Priestley). У него была лаборатория, оборудованная приборами для собирания газов. Он испытывал его физиологическое действие на себе и на мышах. Пристли установил, что после вдыхания газа некоторое время ощущается приятная легкость. Мыши в герметически закрытой банке с воздухом задыхаются быстрей, чем в банке с O2. Поскольку Пристли был приверженцем флогистонной теории он так и не узнал, что оказалось у него в руках. Он только описал этот газ, даже не догадываясь, что он описал. А вот лавры открытия кислорода принадлежат Антуан Лоран Лавуазье (Antoine Laurent de Lavoisier), который и дал ему имя.
Лавуазье, поставил свой знаменитый опыт, продолжавшийся 12 дней. Он нагревал ртуть в реторте. При кипении образовывалась ее красная окись. Когда реторту охладили, оказалось, что воздуха в ней убыло почти на 1/6 его объема, а остаток ртути весил меньше, чем перед нагревом. Но когда разложили окись ртути сильным прокаливанием, все вернулось: и недостача ртути, и «исчезнувший» кислород.
Впоследствии Лавуазье установил, что этот газ входит в состав азотной, серной, фосфорной кислот. Он ошибочно полагал, что O2 обязательно входит в состав кислот, и поэтому назвал его «оксигениум», что значит «рождающий кислоты». Теперь хорошо известны кислоты, лишенные «оксигениума» (например: соляная, сероводородная, синильная и др.).
Правила использования
Кислород – опасный газ, который может взорваться при контакте с огнем, маслом. Герметичный баллон ограждает сырье от соприкосновения с неблагоприятными условиями, но неприятность может возникнуть при падении или нагревании солнечными лучами. Существуют рекомендации, позволяющие обезопасить людей при эксплуатации летучего вещества.
Сварка
Кислород запрещено совмещать с асфальтом и углем, древесиной и бумагой. Пропитанные концентрированной сжатой жидкостью материалы способны детонировать. После работ с веществом нужно проветривать одежду в течение получаса.
Горючие и воспламеняющиеся компоненты располагают минимум в 5-10 м от емкости с газом. По технике безопасности резервуар размещают в вертикальном положении. Перед подключением баллоны обезжиривают тряпкой. Конструкцию подсоединяют крепко и устойчиво, иначе конструкция рухнет.
Если вентиль замерз, то запрещено отогревать огнем. Лучше подержать резервуар в теплом помещении или использовать горячую воду. Колпак легче отсоединить ключом, но некоторые модели откручиваются вручную. При движениях стараются не делать резких рывков, иначе возможно воспламенение.
При осмотре поверхности запорной детали обращают внимание на вмятины, царапины. Запрещена эксплуатация оборудования с поврежденной емкостью или с просроченным сроком годности. Ингредиенты при случайном попадании могут обжечь слизистую глаз и обморозить кожу. Работы с веществом проводят в защитных рукавицах и маске.
Заправка
Надежность и безопасность эксплуатации резервуара зависит от правильности заправки. На станцию вещество поступает в жидком виде, а в баллоны попадает в форме газа. Процедуру осуществляют через вентиль, к которому подсоединяют герметично трубу. Один конец подключают к базе, второй – к емкости.
Соединительные детали прикручивают плотно, но не пережимают. Обязательно следят за герметичностью соединения. Кран аккуратно открывают до характерного шипения. Прекращение шума – признак наполненности емкости.
Закачку для объемных резервуаров осуществляют при помощи насоса, небольшие сосуды можно без дополнительного оборудования. Давление в полном кислородном баллоне редуктором, иначе конструкцию может разорвать. По завершении процедуры вентиль завинчивают, откручивают трубу.
Как хранят и перемещают
Хранение резервуаров с газом прописано в ГОСТе 26460. В помещении должно быть электричество, отопление и вытяжная вентиляция. Рядом с веществом запрещено располагать другие газы, горючие ингредиенты и нагревательные приборы. Здание находится в удалении от производственных построек. Резервуары держат в металлических ящиках с отверстиями, далеко от направленного солнца.
Для перемещения баллонов с кислородом используют специальную технику (носилки, тележки). Емкости запрещено носить на руках (плечах). При перевозке на дальние расстояния нужен автомобиль с грузовым отсеком. Резервуары укладывают горизонтально в ячейки, для уплотнения и защиты от соударений применяют войлок. Если мероприятия проходят в жару, то конструкцию прячут под брезентом.
Опустошенную емкость мелом помечают словом «Пустой», закрывают колпак и заглушку. Кислород из баллонов нельзя полностью расходовать, поэтому оставляют немного вещества под давлением 0,5 кг/см2. Остатки нужны для лабораторного анализа состава газа на заправочной станции. Если информация совпадает с данными от прошлой процедуры, то не надо промывать оборудование.
Комплектация
Основным дополнительным элементом емкости для кислорода является вентиль. Изготавливают его из латуни. Поверх вентиля обязательно устанавливается защитный колпак, он может быть алюминиевым или пластмассовым. Обычно колпак идет, как неотъемлемая часть. Но теряются они часто, так что защитное приспособление может быть изготовлено из любого материала своими руками. Здесь важна надежность и герметичность. В сам баллон вентиль вкручивается посредству конической резьбы
Второй по значимости элемент – это башмак. Именно на него ложится вся весовая нагрузка. Изготавливается он из стальной ленты, которую формируют по сечению в квадрат. ГОСТом точно не определенно, как он должен закрепляться на баллоне, поэтому некоторые производители приваривают его, другие впрессовывают.
Кислород в баллонах
В вы можете купить кислород в баллонах 40 литров и по заказу 5, 10 и 20 литров, заправить баллоны кислородом, а также купитьжидкий кислород.
Кислород, наиболее востребованный технический газ который требуется на многих производствах включая металлургию, пищевую промышленность, медицину, косметологию и многие другие. Он необходим для окислительных процессов и без него невозможен процесс горения.
Этот газ тяжелее воздуха не имеет ни цвета, ни запаха. Очень важно и то, что он не ядовит, а значит безопасен для человека и окружающей среды. Однако большие концентрации кислорода вызывают воспламенение некоторых химических материалов.
Требует высокой культуры производства.
Кислород – рождающий кислоты
Содержание
Кислород при нормальных условиях (температуре и давлении) представляет собой прозрачный газ без запаха, вкуса и цвета. Не относится к горючим газам, но способен активно поддерживать горение.
По химической активности среди неметаллов он занимает второе место после фтора.
Все элементы, кроме благородных металлов (платина, золото, серебро, родий, палладий и др.) и инертных газов (гелий, аргон, ксенон, криптон и неон), вступают в реакцию окисления и образовывают оксиды. Процесс окисления элементов, как правило, носит экзотермический (с выделением теплоты) характер. Также необходимо учитывать тот факт, что при повышении температуры, давления или использовании катализаторов – скорость реакции окисления резко возрастает.
МАСЛООПАСЕН.
Хранение и транспортировка кислорода.
Упаковка и хранение кислорода осуществляется в соответствии с требованиями ГОСТ 26460. Для транспортировки технического и медицинского кислорода используются все виды транспорта, включая трубопровод. Транспортировка и хранение газообразного кислорода осуществляется в металлических кислородных баллонах, произведенных в соответствии с ГОСТ 949-73. Кислородные баллоны имеют голубой цвет и белую надпись «кислород». При температуре окружающей среды +20 C°, давление газа в кислородном баллоне не должно быть выше 14,7 МПа (150 кгс/см²) – в соответствии с требованиями ГОСТ 949-73, по которым производятся кислородные баллоны. В случая транспортировки кислорода по трубопроводу – давление кислорода в трубопроводе согласовывается между поставщиком и потребителем.
Требования безопасности.
Кислород в баллонах не является токсичным, пожароопасным или взрывоопасным газом. Кислород в баллонах является сильным окислителем, способным вызвать воспламенение некоторых материалов при прямом контакте или повышенной концентрации в помещении, которая не должна превышать 23%. Перед проведением освидетельствования кислородных баллонов или трубопровода – выполняется продувка обычным атмосферным воздухом (для снижения концентрации кислорода). Ремонт кислородных баллонов или трубопроводов осуществляется тоже с предварительной продувкой. При нахождении в помещениях с повышенной концентрацией кислорода (более 23%), строго запрещено курить, включать обогревательные электроприборы и наличие открытого огня, потому что это способствует возникновению пожара. Помещения с повышенной концентрацией кислорода обязательно должны быть оснащены вентилирующим оборудованием и средствами пожаротушения. Следует помнить, что кислородные баллоны не предназначены для хранения, транспортировки других газов! Для сохранения качества продукции, кислородный баллон или трубопровод должны быть чистыми внутри и не иметь посторонних загрязняющих веществ (пыль, песок и прочее). При транспортировке и осуществлении погрузо-разгрузочных работ, следует исключить возможности падения или ударов кислородных баллонов. В период хранения кислородных баллонов, они должны быть предохранены от воздействия прямых солнечных лучей, потому что повышение температуры способствует повышению давления газа внутри баллона. При повышенном давлении газа в кислородном баллоне, следует охладить баллон водой.
Правила приёмки кислорода.
Продажа и доставка кислорода к потребителю осуществляется партиями. Партией поставки кислорода может быть любой, с наличием сопроводительного документа качества.
Правила возврата кислородных баллонов поставщику.
практикует сдачу в аренду газовых баллонов различного типа. При возвращении газового баллона, потребитель должен обеспечить наличие остаточного давления в пустом кислородном баллоне не ниже 0,05 МПа (0,5кгс/см²).
Зависимость давления кислорода от температуры при наполнении, транспортировании и хранении баллонов
| Температура, ºС | Рабочее давление, МПа (кгс/см²) | Давление газа при температуре наполнения, МПа (кгс/см²) |
| -50 | 9,7 (99) | 12,4 (127) |
| -40 | 10,5 (107) | 13,5 (137) |
| -30 | 11,2 (114) | 14,5 (148) |
| -20 | 11,9 (121) | 15,5 (158) |
| -10 | 12,6 (128) | 16,6 (169) |
| -50 | 9,7 (99) | 12,4 (127) |
| 0 | 13,3 (136) | 17,7 (179) |
| 10 | 14,0 (143) | 18,6 (190) |
| 20 | 14,7 (150) | 19,6 (200) |
| 30 | 15,4 (157) | 20,6 (210) |
Примечание:
При наполнении баллонов, а также хранении или транспортировании наполненных баллонов при температурах, превышающих указанные в таблице, давление газов в баллоне не должно превышать:
Продажа и доставка газовых баллонов с кислородом.
производит снабжение предприятий (различного профиля) техническими газами: азот, аргон, ацетилен, газовые смеси, гелий марки «А» и гелий марки «Б», технический кислород, пропан, а также углекислота. Кроме поставок технических газов, компания специализируется на торговле газовыми баллонами, произведёнными по ГОСТ 949-73 и ГОСТ 15860-84 (для пропана). Среди дополнительных
Источник
Область применения
Кислород в баллонах для сварки находит применение во многих областях промышленности. Практически все места, где используется полуавтомат или газовая сварка, требуют применение кислорода. С его помощью осуществляется газопламенная обработка металла, как до начала сварки, так и после нее.
Если рассматривать применение газа для резки, то он становится неотъемлемым, так как именно он дает высокую температуру струи, которая прожигает металлические изделия. минимально допустимая чистота кислорода для использования кислорода в сфере сварки составляет 99,2%. Лучше, если этот показатель будет выше, если речь идет об ответственных работах. В домашнем применении встречаются бюджетные варианты и 92% кислорода.
Баллон кислородный новый
Кислород наиболее распространен на Земле. В земной коре (около 47% по массе) существует в связанном виде, в атмосфере (около 23% по массе) – в свободном.
Основные способы получения кислорода:
Кислород газообразный технический, согласно ГОСТ 5583-78, выпускается двух сортов: первого и второго. Баллон с кислородом окрашен в голубой цвет, с надписью «Кислород» черного цвета (ПБ 10-115-96, ГОСТ 949-73). Номинальное давление газообразного кислорода в баллоне и автореципиенте при 20°С (ГОСТ 5583-78) составляет 150 кгс/см 2 (14,7 МПа) или 200 кгс/см 2 (19,6 МПа).
Характеристики марок газообразного технического кислорода (ГОСТ 5583-78)
| Параметр | Кислород газообразный технический | |
| первого сорта | второго сорта | |
| Объемная доля кислорода O2, %, не менее | 99,7 | 99,5 (в ряде случаев – 99,2) |
| Объемная доля водяных паров, %, не более | 0,007 | 0,009 |
| Объемная доля водорода H2, %, не более (только для кислорода, полученного электролизом воды) | 0,3 | 0,5 |
| Содержание углекислоты CO2, окиси углерода CO, газообразных кислот и оснований, озона O3 и других газов-окислителей | Не нормируется | |
| Содержание щелочи (только для кислорода, полученного электролизом воды) | Кусок фильтровальной бумаги (смоченный раствором фенолфталеина, разбавленного водой в соотношении 1:10) в стеклянной трубке с пропускаемым кислородом (0,1–0,2 дм 3 /мин в течение 8–10 минут) не должен окраситься в красный или розовый цвет | |
| Запах | Не нормируется | |
Допустимое давление кислорода в баллонах в зависимости от температуры (при номинальном давлении 150 кгс/см 2 / 20°С)
| Температура, °С | -50 | -40 | -30 | -20 | -10 | 0 | +10 | +20 | +30 | +40 | +50 |
| Давление в баллоне, кгс/см 2 | 99 | 107 | 124 | 129,5 | 134,5 | 139,5 | 145 | 150 | 155 | 160 | 172 |
Для расчета объема газообразного кислорода в баллоне в м 3 при нормальных условиях используют формулу (ГОСТ 5583-78):
где K1 – коэффициент, Vб – вместимость баллона в дм 3 (л).
Некоторые значения коэффициента K1 для расчета объема газообразного кислорода при нормальных условиях
| t газа в бал- лоне, °С | Значение K1 при избыточном давлении, кгс/см 2 (МПа) | |||||||||||
| 140 (13,7) | 145 (14,2) | 150 (14,7) | 155 (15,2) | 160 (15,7) | 165 (16,2) | 170 (16,7) | 175 (17,2) | 180 (17,7) | 185 (18,1) | 190 (18,6) | 195 (19,1) | |
| -50 | 0,232 | 0,242 | 0,251 | 0,260 | 0,269 | 0,278 | 0,286 | 0,296 | 0,303 | 0,311 | 0,319 | 0,327 |
| -40 | 0,212 | 0,221 | 0,229 | 0,236 | 0,245 | 0,253 | 0,260 | 0,269 | 0,275 | 0,284 | 0,290 | 0,298 |
| -30 | 0,195 | 0,202 | 0,211 | 0,217 | 0,225 | 0,232 | 0,239 | 0,248 | 0,253 | 0,261 | 0,267 | 0,274 |
| -20 | 0,182 | 0,188 | 0,195 | 0,202 | 0,209 | 0,215 | 0,222 | 0,229 | 0,235 | 0,242 | 0,248 | 0,255 |
| -10 | 0,171 | 0,177 | 0,183 | 0,189 | 0,195 | 0,202 | 0,208 | 0,214 | 0,220 | 0,226 | 0,232 | 0,238 |
| 0 | 0,161 | 0,167 | 0,172 | 0,179 | 0,184 | 0,190 | 0,196 | 0,201 | 0,207 | 0,213 | 0,219 | 0,224 |
| +10 | 0,153 | 0,158 | 0,163 | 0,169 | 0,174 | 0,180 | 0,185 | 0,191 | 0,196 | 0,201 | 0,206 | 0,211 |
| +20 | 0,145 | 0,150 | 0,156 | 0,160 | 0,166 | 0,171 | 0,176 | 0,181 | 0,186 | 0,191 | 0,196 | 0,201 |
| +30 | 0,139 | 0,143 | 0,148 | 0,153 | 0,158 | 0,163 | 0,168 | 0,173 | 0,177 | 0,182 | 0,187 | 0,192 |
| +40 | 0,133 | 0,137 | 0,142 | 0,147 | 0,151 | 0,156 | 0,160 | 0,165 | 0,170 | 0,174 | 0,178 | 0,183 |
| +50 | 0,127 | 0,132 | 0,136 | 0,141 | 0,145 | 0,149 | 0,154 | 0,158 | 0,163 | 0,167 | 0,171 | 0,175 |
Таким образом, в новом баллоне (150 кгс/см 2 при 20°С) объемом 40 л содержится 6,24 м 3 кислорода при нормальных условиях.
Кислород жидкий технический, согласно ГОСТ 6331-78, также выпускается первого и второго сортов. Он хранится и перевозится в сосудах Дьюара, а также в других криогенных резервуарах (танках).
Характеристики марок жидкого технического кислорода (ГОСТ 6331-78)
При испарении 1 л жидкого кислорода образуется около 860 л газообразного (при нормальном атмосферном давлении и температуре 20°С). При транспортировке жидкого кислорода масса тары, приходящаяся на 1кг кислорода, в 10 и более раз меньше, чем при транспортировке газообразного. При хранении, перевозке и газификации сжиженного газа неизбежны потери на его испарение.
Кислород технический газообразный: для чего нужен, виды, ГОСТ
Кислород
Химический элемент Кипящий жидкий кислород
| Атомная масса | 15,99903 а.е.м. |
| Электронная конфигурация | [He] 2s2 2p4 |
| Электроотрицательность | 3,44 по шкале Полинга |
| Степени окисления | -2; -1; -0,5; -1/3; 0; +0,5; +1; +2 |
| Плотность | 0,00142897 г/см3 |
| Температура плавления | 54,8 K |
| Температура кипения | 90,19 K |
| Структура кристаллической решетки | моноклинная |
| Теплопроводность | (300 K) 0,027 Вт/(м·К) |
Химия. Кислород // Наука 2.0 [25:38]Кислород
(лат. Oxygenium
) — химический элемент c атомным номером 8. Обозначается символом O.
- 1 Описание
- 2 История
- 3 Распространение в природе
- 4 Физические свойства
- 5 Химические свойства
- 6 Получение
- 7 Применение 7.1 Сварка и резка металлов
- 7.2 В медицине
- 8 В металлургии
- 8.2 Ракетное топливо
- 8.3 Взрывчатые вещества
- 9 Биологическая роль кислорода
- 10 Токсичные производные кислорода
- 11 Изотопы
- 12 Факты о кислороде
- 13 Источники
- 14 Литература
[править] Описание
Кислород — буквально «тот, что порождает кислоту». Русское слово восходит к М. В. Ломоносову и является калькой французского слова oxygène
, предложенного А. Лавуазье (от др.-греч. ὀξύς — «кислый» и γεννάω — «рождаю»).
Атомный номер кислорода — 8; атомная масса — 15,9994. Кислород образует соединения со всеми элементами, кроме гелия, аргона и неона. При нормальных условиях кислород — газ, состоящий из двухатомных молекул.
При 90,18 К кислород конденсируется в бледно-голубую жидкость, при 54,36 К — затвердевает.
Есть и другие аллотропные формы кислорода, в частности трехатомный кислород (формула O3) называется озон — при нормальных условиях газ голубого цвета со специфическим запахом.
Плотность жидкого кислорода — 1,144; температура плавления составляет −218 ° C, температура кипения составляет −183 ° C.
С некоторыми металлами кислород образует пероксиды, надпероксиды, озониды, а с горючими газами — взрывчатые смеси.
Элемент кислород занимает третье место после водорода и гелия по распространенности в Вселенной. Он — самый распространенный химический элемент на Земле — 47 % массы земной коры, 85,7 % массы гидросферы, 23,15 % массы атмосферы, 79 % и 65 % массы растений и животных соответственно.
За объемом кислород занимает 92 % объема земной коры. Известно около 1400 минералов, содержащих кислород, главные из них — кварц, полевые шпаты, слюда, глинистые минералы, карбонаты. Более 99,9 % кислорода Земли находится в связанном состоянии. Кислород — фактор, который регулирует распределение элементов в планетарном масштабе.
его с глубиной закономерно уменьшается. Количество кислорода в магматических породах меняется от 49 % в гранитах до 38-42 % в дунитах и кимберлитах. кислорода в метаморфических породах соответствует глубине их формирования: от 44 % в эклогитах 48 % в кристаллических сланцах. Максимум кислорода — в осадочных породах — 49-51 %.
Исключительную роль в геохимических процессах играет свободный кислород — молекулярный кислород, значение которого определяется его высокой химической активностью, большой миграционной способностью и постоянным, относительно высоким содержанием в биосфере, где он не только расходуется, но и воспроизводится.
Считается, что свободный кислород появился в протерозое в результате фотосинтеза.
В гипергенных процессах кислород — один из основных агентов, он окисляет сероводород и низшие оксиды.
Кислород определяет поведение многих элементов: повышает миграционную способность халькофилов, окисляя сульфиды до подвижных сульфатов, снижает подвижность железа и марганца, осаждая их в виде гидроксидов и вызывая тем самым их разделение.
В водах океана содержание кислорода меняется: летом океан отдает кислород в атмосферу, зимой поглощает его. Полярные регионы обогащены кислородом. Важное геохимическое значение имеют соединения кислорода, в частности вода.
Основной промышленный метод получения кислорода — разделение воздуха методом глубокого охлаждения. Как побочный продукт кислород получают при электролизе воды. Разработан способ получения кислорода методом выборочной диффузии газов через молекулярные сита.
Газообразный кислород применяется в металлургии для интенсификации доменных и сталеплавильных процессов, при выплавке цветных металлов в шахтных печах, бессемеровании штейнов и др. (Более 60 % потребляемого кислорода); как окислитель во многих химических производствах; в технике — при сварке и резке металлов; при подземной газификации угля и т. п.
; озон — при стерилизации питьевой воды и дезинфекции помещений. Жидкий кислород используют как окислитель для некоторых разновидностей ракетного топлива.
кислорода
Более 99,9% кислорода Земли находится в связанном состоянии. Кислород — главный фактор, регулирующий распределение элементов в планетарном масштабе. его с глубиной закономерно уменьшается. Количество кислорода в магматических породах меняется от 49% в кислых эффузивах и гранитах до 38-42% в дунитах и кимберлитах.
кислорода в метаморфических породах соответствует глубинности их формирования: от 44% в эклогитах до 48% в кристаллических сланцах. Максимум кислорода в осадочных породах 49-51%. При погружении осадков происходит их дегидратация и частичное восстановление оксидного железа, сопровождающиеся уменьшением количества кислорода в породе.
При подъёме горных пород из глубин в приповерхностные условия начинаются процессы их изменения с привносом воды и углекислоты и содержание кислорода повышается.
Исключительную роль в геохимических процессах играет свободный кислород, значение которого определяется его высокой химической активностью, большой миграционной способностью и постоянным, относительно высоким содержанием в биосфере, где он не только расходуется, но и воспроизводится.
[править] История
Кислород был открыт в 1773 году шведским химиком К. В. Шееле, и независимо от него в 1774 году — английским ученым Джозефом Пристли. Французский химик Антуан Лавуазье дал новому элементу его название, а в 1777 году создал кислородную теорию дыхания, горения и окисления. В свободном виде известен, как молекулярный кислород (O2) и озон (O3).
Еще в VIII веке установлено наличие в воздухе газа, поддерживающего дыхание и горение. Однако европейцы кислород открыли почти через 1000 лет. Шведский химик К. В. Шееле в 1771 году установил, что воздух состоит из кислорода и азота.
Важным этапом, который способствовал открытию кислорода, были работы французского химика Пьера Байена, опубликовавшего свои работы по окислению ртути и последующего разложения ее оксида.
В 1774 году Дж. Пристли добыл кислород разложением оксида ртути HgO. Но все же главные лица в истории открытия кислорода — это не К. В. Шееле и не Дж. Пристли. Они открыли новый газ — кислород, но несмотря на это до конца жизни оставались ревностными защитниками теории флогистона, которая длительное время тормозила развитие науки.
Особое значение в истории открытия кислорода имеют работы А. Лавуазье. Он в 1775 году установил, что кислород — составная часть воздуха, создал кислородную теорию горения (за 200 лет она не только не была опровергнута, но и получила множество подтверждений своей истинности), которая пришла на смену теории флогистона.
В 1898 году английский ученый Томпсон, лорд Кельвин, утверждал, что человечеству грозит удушье, поскольку в воздух выделяется огромное количество углекислого газа не только от дыхания, но и от промышленных предприятий. Это утверждение опроверг К. А. Тимирязев.
Он доказал, что человечеству не дадут погибнуть зеленые растения, выделяющие кислород в ходе фотосинтеза.
[править] Распространение в природе
Кислород — самый распространенный на Земле элемент, содержание его составляет 47 % по массе (в основном в форме оксидов), в воздухе (тропосфере) кислорода (O2) — 20,93 % по объему, или 23 % по массе. В состав воды входит 88,8 % кислорода, в морской воде — 85,7 %.
Он входит в состав большинства горных пород, почв, а также клеток всех растительных и животных организмов. Кислород в целом составляет 30-85 % массы животных и растительных тканей. Он входит в состав белков, нуклеиновых кислот, жиров, углеводов и т. п.
Свободный кислород играет большую роль в биохимических и физиологических процессах, в частности в дыхании. При недостаточном снабжении организма животных и человека кислородом развивается гипоксия.
Зеленые растения и некоторые бактерии являются источником свободного кислорода на Земле.
Во Вселенной кислород — третий по распространенности химический элемент после водорода и гелия.
Нахождение в природе
Накопление O2 в атмосфере Земли. Зелёный график — нижняя оценка уровня кислорода, красный — верхняя оценка. 1
. (3,85—2,45 млрд лет назад) — O2 не производился
2
. (2,45—1,85 млрд лет назад) O2 производился, но поглощался океаном и породами морского дна
3
. (1,85—0,85 млрд лет назад) O2 выходит из океана, но расходуется при окислении горных пород на суше и при образовании озонового слоя
4
. (0,85—0,54 млрд лет назад) все горные породы на суше окислены, начинается накопление O2 в атмосфере
5
. (0,54 млрд лет назад — по настоящее время) современный период, содержание O2 в атмосфере стабилизировалось
Опасные факторы и меры безопасности
Применение при сварке и резке
Кислород – важнейший газ для сварки и резки. При сжигании горючего газа в воздухе образуется пламя с температурой не более 2000°C, а в технически чистом кислороде она может превышать 2500–3000°C. Именно такая температура пламени практически пригодна для сварки многих металлов.
При газопламенной обработке обычно используется кислород с объемным содержанием 99,2–99,5% и выше. Для неответственных видов газовой сварки, пайки, поверхностной закалки и других способов нагрева газовым пламенем может применяться кислород чистотой 92–98%.
Для сварки и резки используют кислород в газообразном виде, поступающий от баллона, газификационной установки (СГУ-1, СГУ-4, СГУ-7К, СГУ-8К, ГХ-0,75, ГХК-3 и др.) или автономной станции (КГСН-150, К-0,15, К-0,4, К-0,5 и др.). При значительных объемах потребления кислород безопаснее и экономически целесообразнее хранить и транспортировать в жидком, а не газообразном виде, несмотря на неизбежные потери при испарении сжиженного газа.
Превращение жидкого кислорода в газообразный осуществляется в газификационных установках – насосных или безнасосных. Примером насосной установки может служить стационарная установка СГУ-1, предназначенная для газификации непереохлажденного кислорода и наполнения реципиентов и баллонов под давлением до 240 кгс/см 2 (24 МПа).
Наряду с процессами газопламенной обработки кислород также применяется:
Надежный и удобный баллон кислородный новый!
Баллон кислородный новый создан для транспортировки и хранения газообразного вещества.
Стоит отметить, что баллон кислородный новый является классическим типом концентратора химического элемента. Человечество использует специальную емкость на протяжении нескольких десятилетий. Даже ведущие европейские страны продолжают применять такой тип оборудования.
В настоящее время на российском рынке представлен богатый ассортимент кислородного оборудования для бытового, промышленного и клинического использования. Аквалангисты всегда применяют баллон кислородный новый при погружении под воду, мастера во время сварочных, работ, стоматологи при лечении зубов и т. д.
Баллон кислородный новый выполняет широкий спектр серьезных задач в каждой из этих сфер. Именно поэтому к его изготовлению применяется ряд важных требований. Такой тип баллонов производят из цельнотянутых труб с обжатием горловины и днища.
Сорт легированных и углеродистых сталей может быть различным. Чем крепче материал, тем больше емкость сможет выдержать максимальное давление. В конструкции сосуда предусмотрен специальный клапан высокого давления, который обеспечивает эффективное распределение кислорода.
Владелец оборудования должен помнить о повышенной взрывоопасности и пожароопасности нового кислородного баллона. В стандартной емкости давление химического элемента достигает 200 атмосфер.
Для того чтобы не допустить чрезвычайной ситуации, каждый должен выполнить ряд требований.
В первую очередь мастер должен пройти курсы безопасности по использованию специализированного оборудования подобного вида. Заполнять баллон кислородный новый можно только в официальных компаниях, имеющих профиль и все необходимые лицензии.
В процессе эксплуатации необходимо грамотно ухаживать за сосудами: постоянно контролировать уровень замасленности, а также выполнять обезжиривание поверхностей спиртом.
В широком ассортименте продукции каждый найдет баллон кислородный новый!
Хранение и транспортировка кислорода
Кислород газообразный технический и медицинский выпускают по ГОСТ 5583.
Хранят и транспортируют его в стальных баллонах ГОСТ 949 под давлением 15 МПа. Кислородные баллоны окрашены в синий цвет с надписью черными буквами «КИСЛОРОД».
Жидкий кислород выпускается по ГОСТ 6331. O2 находится в жидком состоянии только при получении, хранении и транспортировке. Для газовой сварки или газовой резки его необходимо снова превратить в газообразное состояние.
Где приобрести пропановый баллон
Наша компания предоставляет вам возможность купить пропан по выгодной цене.
Наш регион имеет широкую сеть аттестованных предприятий по продаже и заправке баллонов. Самыми распространенными считаются резервуары, вместимостью 27 и 50 л., но по предварительному заказу Вам в кратчайшие сроки поставят изделия на 5 или 12 л.
При заправке, конечно, быстрее поменять свой баллон на уже заправленный. Однако многие предпочитают немного подождать, чтобы получить обратно собственный. Ведь он точно не пропускает газ и вовремя прошел необходимые испытания. Оператор сам следит, чтобы количество жидкого пропана не превышало 85% геометрической емкости сосуда. Это необходимо для того, чтобы при нагревании внутреннее давление не превысило допустимый порог. Если на дне имеются остатки содержимого (т. н. конденсат), заправщик обязан слить его в специальную емкость.
Правила безопасной эксплуатации пропановых баллонов
- При использовании и хранении нельзя допускать перегрева баллонов (например, надолго оставлять под прямыми солнечными лучами);
- не рекомендуется вытравливать пропан-бутановую смесь до полного опустошения резервуара (при определенных условиях он может всосать воздух, а это опасно);
- при транспортировке обязательно использовать заглушки и предохранительные колпаки;
- в случае обнаружения вмятин или других дефектов, изделие необходимо отправить на внеплановую перепроверку;
- частным лицам разрешается перевозить не более пяти баллонов в одном транспортном средстве (при этом они должны быть отделены прокладками друг от друга).
- необходимо постоянно контролировать состояние балонов, ведь не зря они считаются огне- и взрывоопасными объектами.
Какое давление газа в баллоне с пропаном?
Согласно ГОСТ15860-84 рабочее давление в резервуаре не должно превышать 1,6 МПа. При этом доля пропана в углеводородной смеси должна быть не меньшей, чем 60%. Это очень важно для безопасной эксплуатации газобаллонных установок. Конечно же, рассчитываются изделия на значительно большее давление — более 5,0 МПа. Производственные и периодические испытания проводятся под давлением 3,0 МПа.
Нормы заправки
На станциях заправки газовых баллонов сотрудники знакомы с нормативами. Так как слишком сильно заправленный баллон можно взорваться или у него может оторвать клапан. Так, что если вы заправляетесь у надёжного поставщика вам не о чем волноваться.