Что это такое?
Рафинирование меди или электролиз использует анод, который содержит нечистую медь. Она возникает из-за концентрации руды. Катод состоит из чистого металла (титана или нержавеющей стали). Раствор электролита состоит из сульфата. Поэтому можно утверждать, что рафинирование меди и электролиз – это одно и то же. Электрический ток заставляет ионы меди из анодов поступать в раствор и осаждаться на катод. При этом примеси либо отходят, либо образуют осадок, либо остаются в растворе. Катод становится больше, чем чистая медь, а анод сжимается.
В электролитических ячейках используется внешний источник постоянного тока для реагирования на реакции, которые иначе не были бы спонтанными. Электролитические реакции используются для очистки пластинчатых металлов на многих типах субстратов.
Использование электролитического процесса для очистки металла (рафинирование меди, электролиз металла):
- Поскольку примеси могут значительно снизить проводимость медных проволок, необходимо очистить загрязненную медь. Одним из способов очистки является электролиз.
- Когда в качестве анода при электролизе водного препарата сульфата меди используется полоса из нечистой металлической меди, окисляется медь. Окисление ее протекает проще, чем окисление воды. Поэтому металлическая медь растворяется в растворе в виде ионов меди, оставляя за собой многие примеси (менее активные металлы).
- Ионы меди, образованные на аноде, мигрируют к катоду, где они легче восстанавливаются, чем вода и металлические «пластины» на катоде.
Необходимо пропускать достаточный ток между электродами, иначе в противном случае возникнет не спонтанная реакция. Тщательно регулируя электрический потенциал, металлические примеси, которые достаточно активны для окисления меди на аноде, вещества не уменьшаются на катоде, а металл избирательно осаждается.
Важно! Не все металлы восстанавливаются или окисляются легче, чем вода. Если это так, сначала произойдет электрохимическая реакция, требующая наименьшего потенциала. Например, если бы мы использовали электроды, как анод, так и катод, металлический потенциал был бы окислен на аноде, но тогда вода будет уменьшаться на катоде, а ионы алюминия останутся в растворе.
Чтобы создать электролиз, нужно использовать следующий способ рафинирования меди:
- Налейте раствор медного сульфата в стакан.
- Поместите два графитовых стержня в раствор сульфата меди.
- Присоедините один электрод к отрицательной клемме питания постоянного тока, а другой – к положительной клемме.
- Полностью заполните две маленькие пробирки раствором сульфата меди и поместите пробку на каждый электрод.
- Включите источник питания и проверьте, что происходит на каждом электроде.
- Испытайте любой газ, произведенный с пылающей шиной.
- Запишите свои наблюдения и результаты ваших тестов.
Результаты должны быть такими:
- Появляются бурые или розовые твердые формы в растворе.
- Есть пузыри.
- Пузыри должны быть бесцветными.
- Вещество газообразной формы.
Все результаты записываются, после чего газ гасится шиной. Также существует иной способ очистить металл от примесей и сторонней грязи – это огневое рафинирование меди. Как это происходит, расскажем позже, а сейчас представим другие варианты рафинирования металла.
Рафинированная медь Украины
| 2. Способы производства высококачественной меди |
Металлы являются основным видом продукции металлургического производства. В цветной металлургии в зависимости от применяемой технологии и состава получающихся металлов различают черновые и рафинированные металлы. Товарной продукцией, поступающей к потребителю для дальнейшего использования по прямому назначению, как правило, являются рафинированные металлы.
Черновыми металлами называют металлы, загрязненные примесями. В меди и никеле могут присутствовать как вредные примеси, так и ценные элементы — спутники основного металла. Вредные примеси ухудшают характерные для данного металла свойства (электропроводность, пластичность, коррозионную стойкость и т. п.) и делают их непригодными для непосредственного использования. Наоборот, благородные металлы, селен, теллур, германий, индий, висмут и многие другие представляют самостоятельную ценность, и их необходимо попутно выделить в соответствующий продукт, что имеет большое экономическое значение. Черновые металлы обязательно подвергают очистке от примесей — рафинированию.
Качество черновых металлов в ряде случаев устанавливается отраслевыми стандартами или техническими условиями, которые регламентируют взаимоотношения между производителями чернового металла и заводами, на которые они поступают для рафинирования.
Конечной задачей металлургии меди, как и любого другого металлургического производства, является получение металлов из перерабатываемого сырья в свободном металлическом состоянии или в виде химического соединения. На практике эта задача решается с помощью специальных металлургических процессов, обеспечивающих отделение компонентов пустой породы от ценных составляющих сырья.
Получение металлической продукции из руд, концентратов или других видов металлосодержащего сырья — задача достаточно трудная. Она существенно усложняется для медных и никелевых руд, которые, как правило, являются сравнительно бедным и сложным по составу полиметаллическим сырьем. При переработке такого сырья металлургическими способами необходимо одновременно с получением основного металла обеспечить комплексное выделение всех других ценных компонентов в самостоятельные товарные продукты при высокой степени их извлечения. В конечном итоге металлургическое производство должно обеспечить полное использование всех без исключения компонентов перерабатываемого сырья и создание безотходных (безотвальных) технологий.
Как указывалось ранее, основная масса медных руд состоит из соединений меди, железа и пустой породы, поэтому конечная цель металлургической переработки этих руд сводится к получению металлургического продукта за счет полного удаления пустой породы, железа и серы (в случае переработки сульфидного сырья).
Для получения металлов достаточно высокой чистоты из сложного полиметаллического сырья с высокой степенью комплексности его использования не достаточно применить один металлургический процесс или один металлургический агрегат. Эта задача до настоящего времени реализуется в практических условиях использованием нескольких последовательно проводимых процессов, обеспечивающих постепенное разделение компонентов перерабатываемого сырья.
Весь комплекс применяемых металлургических процессов, подготовительных и вспомогательных операций формируется в технологическую схему участка, отделения, цеха или предприятия в целом. Для всех предприятий, занимающихся переработкой меди, характерны многоступенчатые технологические схемы.
В основе любого металлургического процесса лежит принцип перевода обрабатываемого сырья в гетерогенную систему, состоящую из двух, трех, а иногда и более фаз, которые должны отличаться друг от друга составом и физическими свойствами. При этом одна из фаз должна обогащаться извлекаемым металлом и обедняться примесями, а другие фазы, наоборот, обедняться основным компонентом. Различия некоторых физических свойств получающихся фаз (плотности, агрегатного состояния, смачиваемости, растворимости и т.п.) обеспечивают хорошее отделение их друг от друга простыми технологическими приемами, например, отстаиванием или фильтрацией.
Современный металлургический процесс должен обеспечивать:
- высокую степень комплексности использования перерабатываемого сырья;
- высокую удельную производительность металлургических аппаратов;
- минимальные энергетические затраты;
- максимальное использование вторичных энергоресурсов;
- использование простой, дешевой и удобной в работе, пуске, наладке и ремонте аппаратуры;
- высокую степень комплексной механизации и автоматизации;
- высокую производительность труда;
- безопасные и безвредные условия труда;
- устранение вредных выбросов в атмосферу;
- максимальную экономическую эффективность.
Высокая степень комплексности использования сырья является основным и едва ли не самым важным требованием к современной технологии, причем она должна пониматься в самом широком смысле.
В понятие комплексности использования сырья должно включаться максимально высокое извлечение всех ценных составляющих руды: меди, никеля, цинка, кобальта, серы, железа, благородных металлов, редких и рассеянных элементов, а также использование силикатной части руды.
Перерабатываемые сульфидные руды и концентраты обладают достаточно высокой теплотворной способностью и являются не только источником ценных компонентов, но и технологическим топливом. Следовательно, в понятие комплексного использования сырья должно включаться и использование его внутренних энергетических возможностей.
Медные руды и концентраты имеют одинаковый минералогический состав, и отличаются лишь количественными соотношениями между различными минералами. Следовательно, физико-химические основы их металлургической переработки совершенно одинаковы.
Для переработки медьсодержащего сырья с целью получения металлической меди применяют как пиро-, так и гидрометаллургические процессы.
В общем объеме производства меди на долю пирометаллургических способов приходится около 85 % мирового выпуска этого металла.
Пирометаллургическая технология предусматривает переработку исходного сырья (руды или концентрата) на черновую медь с последующим ее обязательным рафинированием. Если принять во внимание, что основная масса медной руды или концентрата состоит из сульфидов меди и железа, то конечная цель пирометаллургии меди — получение черновой меди — достигается за счет практически полного удаления пустой породы, железа и серы.
Получение меди в промышленных условиях может быть осуществлено несколькими путями (рис. 2.1).
На схеме, приведенной на рисунке, видно, что удаление железа и серы может производиться их окислением в три стадии (обжиг, плавка, конвертирование), в две стадии (плавка, конвертирование) или в одну стадию. За исключением последнего варианта, предусматривающего непосредственную плавку концентратов на черновую медь, технология ее получения характеризуется многостадийностью.
Наиболее распространенная технология предусматривает обязательное использование следующих металлургических процессов: плавку на штейн, конвертирование медного штейна, огневое и электролитическое рафинирование меди.
В ряде случаев перед плавкой проводят предварительный окислительный обжиг сульфидного сырья. Обжиг применяется для частичного удаления серы и перевода сульфидов железа и других элементов в легко шлакуемые при последующей плавке оксиды. В результате обжига большая часть сульфидов переходит в оксиды, часть из которых в виде оксидов улетучивается. Степень удаления некоторых элементов в процессе обжига, % (от их содержания в исходном сырье):
Рисунок 2.1.
Принципиальная технологическая схема пирометаллургического получения меди из сульфидных руд
Примечание:
цифрами обозначены возможные варианты переработки исходного сырья на черновую медь.
Медные штейны, содержащие в зависимости от исходного рудного сырья и технологии переработки от 10…12 до 70…75% меди, преимущественно перерабатывают методом конвертирования.
Основная цель конвертирования — получение черновой меди за счет окисления железа и серы и некоторых других сопутствующих компонентов. Благородные металлы (серебро, золото), основная часть селена и теллура остаются в черновом металле.
Черновая медь, являющаяся конечным продуктом, обычно имеет химический состав, приведенный в табл. 2.1.
Таблица 2.1.
Химический состав черновой меди после конвертирования, %
Таблица 2.2.
Химический состав марок черновой меди, мас. %
Черновую медь выпускают в виде слитков массой до 1200 кг и анодов, которые идут на электролитическое рафинирование.
Рафинирование меди производят огневым и электролитическим способами.
Цель огневого рафинирования на предварительной (перед электрохимической) стадии производства сводится к частичной очистке меди от примесей, обладающих повышенным сродством к кислороду, и подготовке ее к последующему электролитическому рафинированию. Методом огневого рафинирования из расплавленной меди стремятся максимально удалить серу, кислород, железо, никель, цинк, свинец, мышьяк, сурьму и растворенные газы.
Для непосредственного технического применения черновая медь не пригодна, и поэтому ее обязательно подвергают рафинированию с целью очистки от вредных примесей и попутного извлечения благородных металлов, селена и теллура.
Небольшие включения (несколько частиц на миллион частиц меди) таких элементов как селен, теллур и висмут могут значительно ухудшить электропроводность и обрабатываемость меди — свойства, которые особенно важны для промышленности, производящей кабельнопроводниковую продукцию, являющейся крупнейшим потребителем рафинированной меди. Электролитическое рафинирование считается основным процессом, который позволяет получить медь, отвечающую наиболее жестким требованиям электротехники.
Сущность электролитического рафинирования меди заключается в том, что литые анод (отлитый, как правило, из меди огневого рафинирования) и катоды — тонкие матрицы из электролитной меди — по-переменно завешивают в электролитную ванну, заполненную электролитом, и через эту систему пропускают постоянный ток.
В процессе электролитического рафинирования решаются две основные задачи:
- глубокая очистка меди от примесей;
- попутное извлечение сопутствующих ценных компонентов.
Анодная медь является многокомпонентным сплавом и обычно имеет химический состав, приведенный в табл. 2.3.
Таблица 2.3.
Химический состав анодной меди,%
В результате электролитического рафинирования предполагается получить медь высокой чистоты (99,90…99,99% Cu).
Следует отметить, что чем выше в исходной меди содержание благородных металлов, тем ниже будет себестоимость электролитной меди.
Для осуществления электролитического рафинирования меди аноды, отлитые после огневого рафинирования, помещают в электролизные ванны, заполненные сернокислым электролитом. Между анодами в ваннах располагаются тонкие медные листы — катодные основы.
Электролит — водный раствор сульфата меди (160…200 г/л) и серной кислоты (135…200 г/л) с примесями и коллоидными добавками, расход которых составляет 50…60 г/т Cu. Чаще всех в качестве коллоидных добавок используют столярный клей и тиомочевину. Они вводятся для улучшения качества (структуры) катодных осадков. Рабочая температура электролита — 50…55 oС.
При включении ванн в сеть постоянного тока происходит электрохимическое растворение меди на аноде, перенос катионов через электролит и осаждение ее на катоде. Примеси меди при этом в основном распределяются между шламом (твердым осадком на дне ванн) и электролитом. На рис. 2.2. приведена схема процесса электролитического рафинирования.
Рисунок 2.2.
Схема процесса электролитического рафинирования
В результате электролитического рафинирования получают: катодную медь; шлам, содержащий благородные металлы; селен; теллур и загрязненный электролит, часть которого иногда используют для получения медного и никелевого купоросов. Кроме того, вследствие неполного электрохимического растворения анодов получают анодные остатки (анодный скрап).
Электролитическое рафинирование основано на различии электрохимических свойств меди и содержащихся в ней примесей.
Медь относится к группе электроположительных металлов, ее нормальный потенциал +0,34 В, что позволяет осуществлять процесс электролиза в водных сернокислых растворах.
Примеси по электрохимическим свойствам разделяют на четыре группы:
- 1 группа — металлы более электроотрицательные, чем медь (Ni, Fe, Zn);
- 2 группа — металлы, расположенные близко к меди в ряду напряжений (As, Sb, Bi);
- 3 группа — металлы более электроположительные, чем медь (Au, Ag, платиновая группа);
- 4 группа — электрохимически нейтральные химические соединения (Cu2S, Cu2Se, Cu2Te и др.).
Механизм электролитического рафинирования меди включает следующие элементарные стадии:
- электрохимическое растворение меди на аноде с отрывом электронов и образование катиона: Cu — 2е —> Cu2+;
- перенос катиона через слой электролита к поверхности катода;
- электрохимическое восстановление катиона меди на катоде: Cu2+ — 2e —> Cu;
- внедрение образовавшегося атома меди в кристаллическую решетку (рост катодного осадка).
Примеси первой группы, обладающие наиболее электроотрицательным потенциалом, практически полностью переходят в электролит. Исключение составляет лишь никель, около 5 % которого из анода осаждается в шлам в виде твердого раствора никеля в меди. По закону Нернста твердые растворы становятся даже более электроположительными, чем медь, что и является причиной их перехода в шлам.
Особенное поведение по сравнению с перечисленными группами примесей демонстрируют свинец и олово, которые по электрохимическим свойствам относятся к примесям 1 группы, но по своему поведению в процессе электролиза могут быть отнесены к примесям 3 и 4 групп. Свинец и олово образуют нерастворимые в сернокислом растворе сульфат свинца PbS04 и метаоловянную кислоту H2Sn03.
Электроотрицательные примеси на катоде в процессе электролиза меди практически не осаждаются и постепенно накапливаются в электролите. При большой концентрации в электролите металлов первой группы электролиз может существенно расстроиться.
Накопление в электролите сульфатов железа, никеля и цинка снижает концентрацию в электролите сульфата меди. Кроме того, участие электроотрицательных металлов в переносе тока через электролит усиливает концентрационную поляризацию у катода.
Электроотрицательные металлы могут попадать в катодную медь в основном в виде межкристаллических включений раствора или основных солей, особенно при их значительной концентрации в электролите. В практике электролитического рафинирования меди не рекомендуется допускать их концентрацию в растворе свыше следующих значений, г/л: 20 Ni; 25 Zn; 5 Fe.
Примеси II группы (As, Sb, Bi), имеющие близкие к меди электродные потенциалы, являются наиболее вредными с точки зрения возможности загрязнения катода. Будучи несколько более электроотрицательными по сравнению с медью, они полностью растворяются на аноде с образованием соответствующих сульфатов, которые накапливаются в электролите. Однако сульфаты этих примесей неустойчивы и в значительной степени подвергаются гидролизу, образуя основные соли (Sb и Bi) или мышьяковистую кислоту (As). Основные соли сурьмы образуют плавающие в электролите хлопья студенистых осадков («плавучий» шлам), которые захватывают частично и мышьяк.
В катодные осадки примеси мышьяка, сурьмы и висмута могут попадать как электрохимическим, так и механическим путем в результате адсорбции тонкодисперсных частичек «плавучего» шлама. Таким образом, примеси 2 группы распределяются между электролитом, катодной медью и шламом. Предельно допустимые концентрации примесей 2 группы в электролите составляют, г/л: 9 As; 5 Sb и 1,5 Bi.
Более электроположительные по сравнению с медью примеси (3 группа), к которым относятся благородные металлы (главным образом, Au и Ag), в соответствии с положением в ряду напряжений должны переходить в шлам в виде тонкодисперсного остатка. Это подтверждается практикой электролитического рафинирования меди.
Переход золота в шлам составляет более 99,5 % от его содержания в анодах, а серебра — более 98 %. Несколько меньший переход серебра в шлам по сравнению с золотом связан с тем, что серебро способно в небольшом количестве растворяться в электролите и затем из раствора выделяться на катоде. Для уменьшения растворимости серебра и перевода его в шлам в состав электролита вводят небольшое количество ионов хлора.
Аналогично электроположительным примесям ведут себя при электролизе меди химические соединения (примеси 4 группы). Хотя, в принципе, химические соединения и могут окисляться на аноде и восстанавливаться на катоде, что используют в специальных процессах, в условиях электролитического рафинирования меди анодного потенциала недостаточно для их окисления. Поэтому при электролизе меди в электродных процессах они не участвуют и по мере растворения анода осыпаются на дно ванны. В виде селенидов и теллуридов переходят в шлам более чем 99 % селена и теллура.
Таким образом, в результате электролитического рафинирования анодной меди все содержащиеся в ней примеси распределяются между катодной медью, электролитом и шламом.
Плотность тока является важнейшим параметром процесса электролиза. Плотность тока при электролизе обычно выбирают от 220…230 до 300 А/м2 площади катода, и общий расход энергоносителей составляет от 1800 до 4000 МДж/т анодов (электроэнергии 200…300 кВт*ч/т меди).
Электроположительный потенциал меди позволяет выделить медь на катоде из кислых растворов без опасения выделения водорода. Введение в электролит наряду с медным купоросом свободной серной кислоты существенно повышает электропроводность раствора. Объясняется это большей подвижностью ионов водорода по сравнению с подвижностью крупных катионов и сложных анионных комплексов.
В качестве катодной основы (матрицы) применяют в зависимости от системы электролиза тонкие медные, титановые и стальные листы. Аноды обычно отливают массой 250…360 кг. Продолжительность растворения анода от 20 до 28 суток.
В течение этого времени производят дватри съема катодов, масса каждого из которых составляет 100…150 кг. Катоды являются конечным продуктом электролитического рафинирования меди.
В процессе электролиза на поверхности катода могут образовываться дендриты, что уменьшает в данном месте расстояние между катодом и анодом. Уменьшение межэлектродного расстояния ведет к уменьшению электрического сопротивления, а, следовательно, к местному увеличению плотности тока. Последнее, в свою очередь, обусловливает ускоренное осаждение меди на дендрите и ускоренный его рост. Начавшийся рост дендрита в конечном итоге может привести к короткому замыканию между катодом и анодом.
Катоды должны быть плотными, нехрупкими. На поверхности катода не должно быть дендритных наростов пористой меди. Допускается наличие наростов, вросших в тело катода, на катодах, изготовленных из меди марок М0ку, М0к иМ1к. Поверхность катодов и катодных ушек должна быть чистой, хорошо отмытой от электролита, и не должна иметь налета сульфатов меди и никеля.
Катоды из меди марок М00к во избежание загрязнения поверхности поставляют упаковаными в деревянные ящики или металлические контейнеры.
Размеры катодов в соответствии с ГОСТ 546 согласовываются между изготовителем и потребителем. Масса катода составляет от 50 до 120 кг и выше. Катоды содержат от 9 до 20 см3 газов на 100 г вещества. Например, газосодержащие катоды меди марки М0к содержат, % (по массе) О2 — 1…9*10-3; Н2 — 2…7, 5*10-4 и N2 — 0…7*10-3.
Проблема внешнего вида и структурного состояния катода усложняет и удорожает технологию электрохимического рафинирования. В большинстве случаев катоды непосредственно непригодны для изготовления высококачественного проката. Поэтому заметную часть катодной меди заводы производители переплавляют в слитки, которые называют вайербарсами (заготовки для прокатки и волочения). По такой усложненной технологии получают безкислородную медь для изготовления тонкой проволоки.
Электролитическое рафинирование меди позволяет полностью извлекать золото, серебро, платиновые и редкие металлы (Se, Те, Bi и др.) и обеспечивает достаточно глубокую очистку от вредных примесей. Стоимость попутно извлекаемых спутников меди обычно перекрывает все затраты на рафинирование, поэтому этот процесс является очень экономичным.
Золото и серебро извлекают при переработке медных руд с большой полнотой и попутно с медью без организации специальных переделов (кроме необходимой переработки богатых электролизных шламов). Поэтому максимальное вовлечение в попутную переработку вместе с медными рудами золотосодержащего сырья (например, кварцитов) экономически очень эффективно и максимально используется.
Возникает вопрос: почему при наличии в технологической схеме электролитического рафинирования, способного очистить медь от всех вредных примесей и извлечь ценные компоненты, включается дополнительно и огневое рафинирование? Практикой и экономическими расчетами однозначно доказано, что двустадийное рафинирование черновой меди обходится дешевле, чем ее прямая электролитическая очистка.
Связано это с меньшим выходом анодного скрапа, получением более богатых шламов, меньшим загрязнением электролита, меньшими расходами на электроэнергию и рядом других факторов, приводящих в итоге к меньшим общим затратам и более высокому извлечению в товарную продукцию как самой меди, так и ценных ее спутников. Одновременно это приводит к улучшению качества товарной меди.
Более 95 % выплавленной черновой меди в настоящее время подвергают двустадийному рафинированию. Вначале медь рафинируют огневым (окислительным) способом, а затем проводят электролиз. В отдельных случаях, когда медь не содержит благородных металлов, ее очистку ограничивают огневым рафинированием. Обычно достигаемая чистота меди после традиционного огневого рафинирования — 99,9 % Cu (мас.). Полученную в этом случае красную медь используют для проката на лист и для приготовления ряда сплавов.
Возможны три варианта организации рафинирования черновой меди в промышленных условиях:
- Обе стадии рафинирования проводят на том же предприятии, где выплавляют черновую медь. В этом случае на огневое рафинирование медь поступает в расплавленном состоянии.
- Обе стадии рафинирования осуществляют на специальных рафинировочных заводах, на которые черновая медь поступает в слитках массой до 1500 кг. Такая технология требует повторного расплавления чернового металла, но позволяет на месте перерабатывать анодные остатки электролизного передела и технологический брак.
- Огневое рафинирование жидкой черновой меди проводят на медеплавильных заводах, а электролиз анодов осуществляют централизованно на специальных предприятиях. Такой вариант рафинирования черновой меди характерен, в частности, для производства рафинированной меди в США.
Таким образом, двустадийная технология производства «огневое рафинирование — электролиз» позволит получить высококачественную продукцию — катодную медь, но наряду с этим она имеет ряд существенных ограничений. Основное ограничение связано с технико-экономическими показателями процесса, который ориентирован на использование первичной меди, получаемой из руды.
Наличие в руде драгоценных и редких металлов, их извлечение на стадии рафинирования обеспечивают приемлемую стоимость конечной продукции (см. рис. 2.1).
Если в материале, который идет на электролиз, содержание этих примесей мало или они вовсе отсутствуют, экономичность производства катодной меди становится проблематичной.
Например, в Украине катодную медь производит Константиновский металлургический завод (Донецкая область). В последнее время он снизил производство медных анодов на 18 % и при проектной мощности 2,4 тыс.т меди в год обеспечивает медью только собственное производство. Удовлетворить растущие потребности украинской промышленности в качественной меди он не в состоянии.
Имеются и другие ограничения, которые сдерживают расширение производства катодной меди в странах, не имеющих промышленных запасов медьсодержащих руд:
- медь получают в твердом состоянии (катоды), что требует дополнительных энергетических затрат на производство конечной продукции.
- необходимы исходные катодные матрицы — катанные полированные плиты толщиной 3…6 мм;
- требуются значительные производственные площади для размещения электролизных ванн;
- необходимы мощные водоочистные сооружения для регенерации и нейтрализации кислотного электролита;
- увеличивается экологическая нагрузка на окружающую среду, загрязнение кислотными испарениями и другими вредными веществами и стоками.
Соответственно при разработке общей технологии получения качественной меди большее внимание приходилось уделять отладке технологии электролиза для обеспечения максимального извлечения ценных металлов, удаления вредных примесей, снижению техногенной нагрузки на окружающую среду. Технология огневого рафинирования рассматривалась как промежуточная, задача которой получить полупродукт (аноды) с примерно заданным составом.
Увеличение мировых объемов произведенной меди, проблемы, возникающие с добычей и переработкой руды, привели к необходимости расширения использования огневого рафинирования как последнего технологического передела в производстве качественной меди.
В этом случае исходным сырьем будет являться не черновая медь, а вторичное медьсодержащее сырье. В результате огневого рафинирования необходимо получить не полупродукт (аноды), а готовую высококачественную медь, которая идет на изготовление требуемых заказчиком изделий.
Добиться принципиального изменения уровня примесей в меди огневого рафинирования невозможно без глубокого теоретического анализа возможностей окислительного рафинирования. Простое использование уже имеющихся технологических разработок в этой области невозможно из-за принципиальных отличий в составе исходного вторичного сырья. Главное отличие сырья, доступного в Украине, от аналогичного вторичного сырья других стран с развитой медеплавильной промышленностью заключается в значительной доле бытовых отходов и непрогнозируемом соотношении содержания различных примесей.
Медеплавильные заводы за рубежом используют более качественное вторичное сырье с узкими пределами изменения состава. Соответственно, требования к их технологическому процессу менее жесткие. Украинские предприятия работают на низкокачественном сырье, но применяемые технологии должны обеспечить получение такой же высококачественной меди и конкурентоспособной продукции из нее.
На рис. 2.3 представлен типичный вид партии металлолома, поступившей на переработку на Артемовский завод по обработке цветных металлов.
Рисунок 2.3.
Вид партии металлолома, поступившего на ОАО «АЗОЦМ».
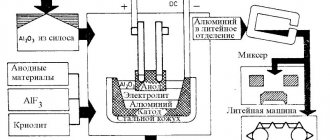
Рассмотрим основные показатели технологии углубленного огневого рафинирования, которую использует одна из ведущих европейских фирм — La Farga Lacambra в Испании. Из лома и отходов меди (преимущественно электротехнической) эта фирма изготавливает жидкую медь марок FRTP и Cu-DHP по BS EN 12163:1998, которая транспортируется по желобам к литейно-прокатному комплексу фирмы Properzi для производства медной катанки, или с помощью ковша транспортируется к газовому миксеру машины вертикального литья круглых заготовок для дальнейшего прессования.
В табл. 2.4 и 2.5 представлены сравнительные данные по качеству сырья и требованиям к нему для украинских производителей и фирмы La Farga Lacambra.
Таблица 2.4.
Сравнение качества сырья украинских производителей и фирмы La Farga Lacambra
Таблица 2.5.
Сравнение требований к качеству сырья украинских производителей и фирмы La Farga Lacambra
Технология огневого рафинирования фирмы La Farga Lacambra имеет ряд существенных недостатков, которые не дают возможность использовать ее металлургическим предприятиям Украины даже при наличии самого современного оборудования:
- Отсутствие возможности удаления из расплава меди никеля с уровнем содержания 600…900 ppm, олова — 800…900 ppm не позволяет перерабатывать по этой технологии лом и отходы, которые собирают в Украине.
- Отсутствует возможность вовлечения в производство луженого и паяного лома и отходов, а также лома бронз и латуней с содержанием меди 92 %.
- Отсутствует удаление неметаллических загрязнений в процессе подготовки сырья к плавке, что приводит к дополнительным потерям меди со шлаками, которые образуют эти неметаллические примеси.
- Отсутствует анализ состава газов. Это не позволяет интенсификацировать процесс восстановления (удаления кислорода) из расплава меди, обеспечить безопасность условий труда и повысить стойкость оборудования (в связи с возможным повышением концентрации СО в атмосфере печи и дымоходах).
- Низкая стойкость футеровки отражательной печи, что связано с агрессивностью флюсов и использованием «мокрого» торкретирования в ходе текущих ремонтов.
- Недостаточно долгий межремонтный период работы печи, связанный с частичным выносом пылефлюсовой смеси, ее налипанием на дымовой шибер и быстрым ее накоплением в камере осаждения.
- Отсутствие возможности выдержать суточный производственный цикл работы комплекса, поскольку емкость печи огневого рафинирования ОАО «АЗОЦМ» значительно больше, чем на фирме La Farga Lacambra, а производительность оборудования и процессы загрузки недостаточно продуктивны.
Для обеспечения потребности украинской промышленности требуется более мощное производство и заметно большая номенклатура марок меди и сплавов из нее, чем на фирме La Farga Lacambra и у других известных производителей, следовательно, технология должна быть гибкой и легко перестраиваться в зависимости от желаний потребителя и имеющегося сырья.
С учетом этих причин предприятиям Украины, которые занимаются изготовлением меди из вторичного сырья, необходима разработка технологии огневого рафинирования, которая не только устраняет недостатки аналогов, но и имеет большую эффективность.
| 2. Способы производства высококачественной меди |
Способы рафинирования меди – как еще могут происходить химические зачистки нужных металлов?
Поскольку электролиз – это воздействие сульфатов и тока, что же такое электролитический способ получения чистой продукции? Совершенно разные вещи, хотя похожи в звучании названий. Однако электрическое рафинирование меди заключается в использовании кислот. Можно сказать, что это окисление металла, но не совсем.
Чистая продукция важна для изготовления электрического провода, поскольку электропроводность меди снижается за счет примесей. Эти примеси включают такие ценные металлы, как:
- серебро,
- золото;
- платина.
Когда они удаляются электролизом и восстанавливаются тем же путем, электроэнергии затрачивается столько, сколько бы хватило на расход электрического питания для снабжения десятков домов. Очищенный компонент позволяет сэкономить энергию, обеспечивая за меньшее время расхода энергии еще больше жилых домов.
При электролитическом рафинировании нечистый состав изготавливается из анода в электролитной ванне из сульфата меди – CuSO4 и серной кислоты H2SO4. Катод представляет собой лист очень чистой меди. По мере пропускания тока через раствор положительные ионы меди, Cu2+ притягиваются к катоду, где они берут на себя электроны и осаждаются, как нейтральные атомы, тем самым создавая на катоде все больше и больше чистого металла. Между тем, атомы в аноде отдают электроны и растворяются в растворе электролита в виде ионов. Но примеси в аноде не идут в раствор, потому что атомы серебра, золота и платины не так легко окисляются (превращаются в положительные ионы), как медь. Таким образом, серебро, золото и платина просто падают с анода на дно резервуара, где их можно очистить.
Но есть и электролитическое рафинирование меди, когда используются резервуары:
- Электролитические очистные резервуары – это отдельный цех в промышленном производстве. Анодные пластины подвешены «ручками» в резервуаре для очистки электролитической меди. Чистые медные катодные листы, подвешенные на сплошных стержнях, вставляются в один и тот же резервуар, один лист между каждым анодом. Когда электрический ток пропускается от анодов через электролит к катодам, медь из анодов перемещается в раствор и высаживается на лист стартера. Примеси из анодов оседают на дно резервуара.
- Литьевая машина с медными анодами (плитами). Он будет плавно превращаться в анодные пластины в пресс-формы. После предварительной обработки происходит удаление олова, свинца, железа, алюминия. Далее начинает заряжаться медный материал в печь, за которым следует процесс плавки.
- Когда примеси удаляются, следует удаление шлака и фаза восстановления с помощью природного газа. Снижение направлено на удаление свободного кислорода. После восстановления процесс заканчивается литьем, когда конечный продукт отливают в виде медных анодов. Такая же машина может использоваться для литья этих анодов во время переработки компонентов или для переработки анодов для металлолома на электролизном медеплавильном заводе.
- Чистые катодные листы. Модифицирующие аноды, извлеченные из рафинирующей печи, превращаются в электролитическую медь с чистотой 99,99 % в процессе электролиза. Во время электролиза ионы меди оставляют нечистый медный анод и, поскольку они являются положительными, мигрируют в катод.
Время от времени чистый металл соскабливается с катода. Примеси из медного анода, такие как золото, серебро, платина и олово, собираются на дне раствора электролита, осаждаются как анодная слизь. Этот процесс и называется электролитическим получением и рафинированием меди.
Производство катодов
Перед загрузкой анодов серию выключают, циркуляцию электролита останавливают. Проверяют уровень электролита в ваннах, излишки удаляют сифоном. На борты ванн укладывают бруски из сухого дерева или винипласта и хорошо Промытые трехгранные медные шины. Аноды взвешивают и загружают по плавкам. С одной стороны аноды опирают на изоляционный брусок, с другой стороны — на шину. Расстояние между анодами устанавливают по мерной рейке. Анод в ванне должен быть установлен строго вертикально. Для скорейшего прогрева электролита циркуляцию включают до окончания операции загрузки анодов.
Катодные основы перед завеской должны быть хорошо выправлены и иметь крепко приклепанные ушки. Перед завеской контакты анодов и трехгранные шины продувают паром. Ломики, на которые подвешивают катодные основы, промывают перед этим горячей водой, подкисленной серной кислотой. Ломики просовывают через ушки катодных основ и при завеске катодов устанавливают одним концом на шину, другим — на изоляционный брусок.
Рис. 97. Инструмент и приспособления, применяемые при электролизе: 1 — кардолента для зачистки контактов; 2 — крючок для правки положения анода а ванне; 3 — крючок для устранения замыканий анода н катода снизу; 4 — переносный индикатор тока (электрощуп); 5 — деревянная пешка подкладывается для выправки положения анода в ванне; 6 — ломик для правки катода; 7 — зубило для съема катодных основ
Прежде чем включить серию, проверяют отсутствие коротких замыканий катодных основ с анодами или стенками ванн, а также правильность расположения ломиков на шинах. Верхние края анодов и катодных основ должны находиться ниже уровня электролита. Серии включают, когда температура электролита становится не ниже 40°. Через каждый час замеряют температуру электролита. Через 3—6 час. производят правку катодов, для чего катоды поштучно вынимают и расправляют, а затем вновь завешивают. Инструмент, используемый при электролизе, приведен на рис. 97. Короткие замыкания обнаруживаются электрощупом, на них указывает падение напряжения, нагревание ломиков и мест контактов. Повышение напряжения указывает на загрязнения контактов. Контакты чистят кардолентой. Устранение замыканий и чистка контактов улучшают процесс электролиза и повышают коэффициент использования тока (выход по току).
Аноды находятся в электролитных ваннах 22—30 дней. Наращивание катодов длится 6—15 дней. Таким образом, одной партии анодов достаточно для образования в 2—4 раза большего числа катодов. При работе серии на третьем или четвертом сроке сработавшиеся аноды заменяют подсадом—годными к использованию анодами, отобранными из анодных остатков. Подсад предварительно выправляют.
Для обеспечения нарашивания меди на ушках, чтобы предупредить обрыв катодов, регулируют уровень электролита в ваннах посредством установки свинцовых колец в лотки ванны. Верхние края катодов при этом должны быть погружены в электролит на 5—10 мм. Катодное отложение меди должно иметь мелкокристаллическую структуру и гладкую поверхность.
Катоды из серий вынимают мостовым краном с применением приспособления для захвата катодов — «бороны».
Некоторое время катоды выдерживают над ванной для стенания электролита и затем подают на промывку водой или обработку паром для удаления электролита и после контроля транспортируют на склад. От каждой серии отбирают два катода в качестве пробы на химический анализ. Перед выгрузкой анодных остатков подачу в ванну электролита прекращают. Анодные остатки отмывают от шлама, сортируют, несработавшиеся возвращают в цикл электролиза в качестве подсада. Отработанные анодные остатки отправляют в плавильный цех. После выгрузки анодных остатков старые изоляционные бруски удаляют.
Требования к качеству медных катодов
- Поверхность катодов не должна иметь скоплений резко выраженных дендритных наростов грибовидной формы, а также крупных наростов пористой меди на кромках. Шишковатости в виде отдельных сферообразных наростов, вросшие в тело катода и не отделяющиеся от него при легких ударах, не являются браковочным признаком. Катоды, полученные в виде мелкокристаллического плотного осадка и имеющие наиболее ровную внешнюю поверхность, обычно отвечают высоким требованиям и, как правило, содержат наименьшее количество водорода и кислорода.
- Катоды не должны быть хрупкими и не должны ломаться от ударов. Хорошего качества медный катод имеет гладкий срез и плотный слой меди, не ломающийся при изгибе. Хрупкость катодов связана с газовой пористостью и прослойками инородных включений в осажденном слое. При изгибе этот слой крошится и отстает от маточного листа; срез образуется шероховатый.
- Поверхность катодов и катодных ушков должна быть чистой, хорошо отмытой от электролита и не должна иметь налета сернокислой меди.
Получение ископаемого – какие виды существуют и все ли они необходимы на практике?
Несколько отличается иной способ очистки металла. Есть еще рафинирование меди огневое и электролитическое, когда один процесс сразу следует за другим. Важным «разделяющим» этапом становится концентрация или концентрирование. После того, как концентрация завершена, следующий этап в создании готовой продукции – огневое рафинирование меди.
Обычно это происходит недалеко шахты, на обогатительной фабрике или плавильном заводе. Благодаря медной очистке нежелательный материал постепенно удаляется, а медь концентрируется с чистотой до 99,99 % марки А. Детали процесса переработки зависят от типа минералов, с которыми связан металл. Медная руда, богатая сульфидами, обрабатывается пирометаллургическим способом.
Переработка и пирометаллургия:
- В пирометаллургии медный концентрат сушат перед нагреванием в печи. Химические реакции, возникающие в процессе нагрева, заставляют концентрат разделяться на два слоя материала: матовый слой и слой шлака. Матовый слой на дне содержит медь, а слой шлака сверху содержит примеси.
- Шлак отбрасывается и матовый слой восстанавливается и перемещается в цилиндрический сосуд, называемый преобразователем. В конвертер добавляются различные химикаты, которые реагируют с медью. Это приводит к образованию превращенной меди, называемой «блистерной». Осажденная она извлекается и затем подвергается другому процессу, называемому огнеочисткой.
- В огнеочистке воздух и природный газ продуваются, чтобы удалить оставшуюся серу и кислород, в результате чего очищенный состав перерабатывается в катод. Металл отливается в аноды и помещается в электролизер. После зарядки чистая медь собирается на катоде и удаляется в виде 99 % чистого продукта.
Переработка и гидрометаллургия:
- В гидрометаллургии медный концентрат подвергается переработке через один из нескольких процессов. Наименее распространенным методом является цементация, где металл осаждается на металлолом в реакции окисления-восстановления.
- Более широко используемый метод очистки – это экстракция растворителем и электролиз. Эта новая технология получила широкое распространение в 1980-х годах, и примерно 20 % мировой меди в настоящее время производится так.
- Экстракция растворителем начинается с органического растворителя, который отделяет металл от примесей и нежелательных материалов. Затем добавляют серную кислоту для отделения меди от органического растворителя, получая электролитический раствор.
- Затем этот раствор подвергают электролизному процессу, который просто ставит медь в растворе на катод. Этот катод может быть продан как есть, но также может быть превращен в стержни или исходные листы для других электролизеров.
Горнодобывающие компании могут продавать медь в концентрате или катодной форме. Как упоминалось выше, концентрат чаще всего рафинируется в другом месте, не на шахтном участке. Производители концентратов продают концентрат-порошок, содержащий от 24 до 40 % меди, в медеплавильные и нефтеперерабатывающие заводы. Условия продажи уникальны для каждого завода, но в целом плавильный завод выплачивает шахтеру примерно 96 % стоимости содержания меди в концентрате, за вычетом платы за обработку и расходов на очистку.
Как правило, плавильные заводы взимают пошлины за проезд, но они также могут продавать рафинированный металл от имени горняков. Таким образом, весь риск (и вознаграждение) от колебаний цен на медь приходится на плечи перекупщиков.
Получение оксида меди
Оксид меди (II) CuO представляет собой кристаллы черного цвета, которые подвергаются кристаллизации в моноклинной сингонии. Плотность соединения составляет 6,51 г/см3, а плавится он при температуре 1447°С в условиях высокого давления. В результате нагревания до 1100°С является выделение оксида меди (I):
- 4CuO = 2Cu2O + O2.
В воде оксид меди не растворяется и не вступает в реакции с ней. Обладает слабыми амфотерными свойствами с преобладанием основных. С водными растворами аммиака реагирует с образованием гидроксида тетраамминмеди (II):
- CuO + 4NH3 + H2O = [Cu(NH3)4](OH)2.
Также легко вступает в реакции с разбавленными кислотами с выделением соли и воды:
- CuO + H2SO4 = CuSO4 + H2O.
Результатом сплавления оксида меди со щелочами является образование купратов:
- CuO + 2KOH = K2CuO2 + H2O.
Чистую медь из оксида можно получить методом восстановления водородом, угарным газом и активными металлами:
- CuO + H2 = Cu + H2O
- CuO + CO = Cu + CO2
- CuO + Mg = Cu + MgO.
Реакция получения оксида меди методом прокаливания гидроксида меди (II) при температуре 200°С:
- Cu(OH)2 = CuO + H2O
Также получить оксид меди можно в процессе окисления металлической меди на воздухе при температуре 400–500°С:
- 2Cu + O2 = 2CuO.
Огневое рафинирование – насколько это опасно?
Самое «ходовое» огневое рафинирование не может быть не опасным, однако в настоящее время метод обработки используется на большинстве промышленных предприятий. Отдельно стоит описать технологию рафинирования черновой меди.
Блистерная медь уже практически чиста (более 99 % меди). Но для сегодняшнего рынка это не очень «чисто». Металл дополнительно очищают, используя электролиз. В промышленном производстве используют метод, который называется огневое рафинирование черновой меди. Чернильная медь отливается в большие плиты, которые будут использоваться в качестве анодов в электролизере. Электролитическое дополнительное рафинирование производит высококачественный металл высокой чистоты, требуемый промышленностью.
В промышленности это осуществляется в массовом масштабе. Даже лучший химический метод не может удалить все примеси из меди, но при помощи электролитического рафинирования можно получить чистую медь на 99,99 %.
- Анодные блистеры погружаются в электролит, содержащий сульфат меди и серную кислоту.
- Между ними расположены чистые катоды, и через раствор проходит ток более 200 А.
В этих условиях атомы меди растворяются из нечистого анода с образованием ионов меди. Они мигрируют к катодам, где осаждаются обратно, как чистые атомы меди.
- На аноде: Cu(s) → Cu2 + (aq) + 2e-.
- На катоде: Cu2 + (aq) + 2e- → Cu(s).
Когда переключатель закрывается, ионы меди на аноде начнут двигаться через раствор к катоду. Атомы меди уже отказались от двух электронов, чтобы стать ионами, и их электроны могут свободно перемещаться в проводах. Закрытие переключателя толкает электроны по часовой стрелке и заставляет оседать в растворе некоторые ионы меди.
Пластина отталкивает ионы от анода к катоду. В то же время она толкает свободные электроны вокруг проводов (эти электроны уже распределены по проводам). Электроны в катоде рекомбинируют с ионами меди из раствора, образуя новый слой атомов меди. Постепенно анод разрушается, а катод растет. Нерастворимые примеси в аноде падают на дно в осадок. Этот ценный биопродукт удаляется.
Золото, серебро, платина и олово нерастворимы в этом электролите, и поэтому не осаждаются на катоде. Они образуют ценный «ил», который накапливается под анодами.
Растворимые примеси железа и никеля растворяются в электролите, который необходимо постоянно очищать, чтобы предотвратить чрезмерное осаждение на катоды, что уменьшит чистоту меди. Недавно катоды из нержавеющей стали заменили медными катодами. Происходят идентичные химические реакции. Периодически катоды удаляются, и очищается чистая медь. Электролитическое получение и рафинирование меди в данных условиях довольно часто встречается на заводах по переработке цветных металлов.
Производство катодных основ
Катодные основы изготовляют из маточных листов, получаемых электролитическим осаждением меди на матрицах. Новые матрицы перед употреблением промывают водой, подкисленной серной кислотой, протирают, сушат, а затем обрабатывают раствором, содержащим 6—8 г/л сернистого натрия. Перед установкой их тщательно протирают тряпкой, после чего наносят равномерный слой смазки, состоящей из 1 части жирового солидола и 6—8 частей керосина.
Медь осаждается электролитическим способом на обеих сторонах матриц слоем 0,25—0,7 мм. Для облегчения сдирки маточных листов матрицы по краям имеют риски, на которых осадок образуется в виде плены, легко счищаемой зубилом. В последнее время матрицы стали изготавливать с фальцами из кислотоупорной пластической массы — фаолита. Если имеются фальцы, осадок меди по краям матриц не образуется, что значительно облегчает сдирку маточных листов.
Матрицы, погнутые или с изогнутыми ломиками, к посадке в ванны не допускаются.
В ваннах матричных серий применяют электролит с повышенным содержанием медного купороса и уменьшенным содержанием серной кислоты. Электролит используется более чистый: с меньшим содержанием примесей, с увеличенным количеством добавок, улучшающих структуру осадка. Температура электролита не должна превышать 56°, так как повышение температуры вызывает растворение смазки, наносимой на матрицы.
Аноды из черновой меди в матричных ваннах служат 13—16 суток. Продолжительность наращивания маточных листов 24 часа. Обычно применяют электролит следующего состава: медный купорос 130—160 г/л, свободная серная кислота 100—160 г/л. В качестве коллоидных добавок в состав электролита вводят столярный клей или желатину и хлор-ион в виде соляной кислоты. Плотность тока должна быть не выше 170 а/м2.
Периодически следует проверять правильность расположения анодов и матриц в ваннах и отсутствие коротких замыканий.
Матрицы с нарощенными осадками вынимают посредством «бороны». Одновременно допускается вынимать не более половины матриц из ванны; количество таких ванн должно быть не более четырех в серии. Вынутые матрицы выдерживают над ваннами для стекания с них электролита, после чего подают на промывку и затем на специальные станки для сдирки листов. На станках матрицы последовательно подаются на вращающуюся рамку, которая позволяет снять листы с обеих сторон матриц без ручного кантования. Листы подрезают по рискам, а если имеются фальцы, сдирку ведут отрывом листов в верхней части матриц. После приклепывания ушков и правки на вальцах катодные основы годны к употреблению.
Матрицы вновь зачищают, погнутые выправляют, затем смазывают и направляют снова на электролитическое получение маточных листов.
Электрохимический вариант очищения металла
Огневая очистка может быть названа химической, потому как в этом процессе происходит химическая реакция с другими веществами и примесями. Выше был приведен пример окислительной реакции. Все виды и способы добычи чистой меди похожи, как и электрохимическое рафинирование меди, где применяются идентичные тактики, но в разной последовательности.
Химическим вспомогательным элементом становится сам побочный продукт:
- Едкий натр.
- Хлор.
- Водород.
Это самый дешевый способ получить дорогое сырье, не тратясь на альтернативную систему добычи компонентов. Помимо этого, добываются ценные металлы, которые благородны по составу и ценны в промышленном изобретении электроприборов.
Медные руды и их месторождения
На настоящий момент получать Cu считается экономически выгодным и целесообразным даже в том случае, если его содержится в породе хотя бы 0.3%.
Чаще всего для выделения меди промышленным способом в природе в наши дни добывают следующие породы:
- борниты Cu5FeS4 — сульфидные руды, называемые по-другому медным пурпуром или пестрым колчеданом и содержащие около 63.3% Cu;
- халькопириты CuFeS2 — минералы, имеющие гидротермальное происхождение;
- халькозины Cu2S, содержащие более 75% меди;
- куприты Cu2O, часто встречающиеся также и в местах залежей самородной меди;
- малахиты, представляющие собой углекислую медную зелень.
Самое большое месторождение медных руд в России находится в Норильске. Также такие породы в больших количествах добывают в некоторых местах на Урале, в Забайкалье, на Чукотке, в Туве и на Кольском полуострове.
Печь меди – металлическая кулинария промышленности
Печь огневого рафинирования меди сконструирована по-особенному и способна обрабатывать медный лом в жидкий металл с контролируемым содержанием примесей. Она предназначена для пирометаллургической переработки лома по экономичной и экологически чистой технологии. Основная технология, предлагаемая для производства расплавленной меди, подходит для производства медной палочки, полосы, заготовки или других медных изделий с использованием лома в качестве сырья (Cu> 92 %).
Потенциал систем сжигания и очистки был рассчитан для цикла очистки (от зарядки до восстановления) в течение 16-24 часов, в зависимости от типа лома. Печи рафинирования меди обладают особой конструкцией и функциями:
- Корпус печи выполнен из стальных сегментов и жестких конструкций типа сечения.
- Печь облицована огнеупорным материалом изнутри.
- Она оснащена гидравлической станцией, работающей в режиме опрокидывания печи с двумя скоростями: скоростью ползучести при наклоне для литья и высокой скоростью во время перемещения, которая не требует особой точности.
- Операции выполняются при помощи двух гидравлических цилиндров, установленных на дне печи. Специальное устройство возвращает печь в горизонтальное положение во время аварийных отключений питания.
- Загрузочный люк материала расположен в боковине печи. Он закрывается дверью, приводимой в движение от гидравлического цилиндра.
- Печь оснащена охлаждаемыми копьями для операций окисления и восстановления меди.
Также есть одна универсальная горелка, потребляющая как жидкое, так и газообразное топливо.
Получение сульфида меди
Сульфид меди(II) или моносульфид меди — CuS, является неорганическим бинарным соединением двухвалентной меди с серой. Он верного цвета, в воде не растворяется , также как и в разбавленных растворах кисло. В природе его можно встретить в виде редкого минерала ковеллина. Получение сульфида меди осуществляется при помощи прямого взаимодействия элементов, а также в результате обменной реакции солей двухвалентной меди с водорастворимыми сульфидами.
- Na2S+CuSO4=CuS+Na2SO4
- CuCl2 + H2S —> CuS + 2HCl
- 2CuS + H2 —>Cu2S + H2S. Эта реакция протекает в условиях высокой температуры от 600 до 700 oC
Получение сухим методом дает сульфиду меди возможность проводить электрический ток. Когда отметка термометра достигает 400 °C, наблюдается заметное разложение сульфида.
Окислительное рафинирование в промышленности
Операция окисления меди проводится после завершения плавки исходного сырья. Процесс осуществляют путем впрыскивания сжатого воздуха в расплав через фурмы. Полученный шлак удаляют вручную с поверхности расплава при помощи специальных граблей и сбрасывают в контейнер. Шлак содержит медь, примеси, свинец, олово и т. д. Процесс восстановления должен проводиться для удаления кислорода из расплава и восстановления оксидов меди. Операция выполняется путем впрыскивания природного газа в расплав.
Из печи, отходящие газы, подаются в систему газоочистки, проходят через пылесборник, который захватывает грубую пыль. Коллектор снабжен вентиляционной трубой в случае аварийного выброса газа в атмосферу. Печь для огнеочистки работает в непрерывном режиме. Цикл работы технологического процесса включает:
- загрузку сырья;
- окисление, шлакообразование, восстановление;
- загрузку рафинированного металла.
Весь последующий процесс называется окислительное рафинирование меди. Он не может быть отделен от общего процесса очистки, так как является частью всего метода получения чистого металла. После того как требуемые параметры будут устранены, расплав меди используется для следующего технологического процесса.
Удаление шламов
Накапливающийся в ваннах шлам не реже 1 раза в 2 месяца удаляют. Ванны отключают от циркуляционной системы; после отстаивания и удаления основной части электролита шламовую пульпу удаляют через отверстие в дне ванны или путем сифонирования, а иногда вычерпывания в специальную шламовую бадью. После фильтрации шламовой пульпы осветленный электролит подают в циркуляционную систему, а отделенный от жидкости шлам поступает на переработку в шламовое отделение для извлечения благородных и других металлов.
Иодидное рафинирование цветных металлов
Ионы меди (II) окисляют иодидные ионы до молекулярного йода, и в этом процессе сами сводятся к иодиду меди (I). Исходная смешанная коричневая смесь разделяется на не совсем белый осадок иодида меди (I) в растворе йода. Используют эту реакцию для определения концентрации ионов меди (II) в растворе. Если добавить в колбу установленный объем раствора, содержащего ионы меди (II), а затем добавить избыток раствора йодида калия, вы получите описанную выше реакцию.
2Cu2+ + 4I- → 2CuI (s) + I2 (водный раствор)
Вы можете найти количество йода, высвобождаемого титрованием раствором тиосульфата натрия.
2S2O2-3 (раствор) + I2 (раствор) → S4O2-6 (водный раствор) + 2I- (водный раствор)
Когда раствор тиосульфата натрия запускается из бюретки, цвет йода исчезает. Когда это почти все исчезнет, добавьте крахмал. Вся реакция иодидного рафинирования меди будет обратимой с йодом для получения глубокого синего крахмал-йодного комплекса, который намного легче увидеть.
Добавляйте последние несколько капель раствора тиосульфата натрия до тех пор, пока синий цвет не исчезнет. Если вы проследите пропорции через два уравнения, вы обнаружите, что для каждых 2 молей ионов меди (II), с которыми вы должны были начать, вам нужно 2 моля раствора тиосульфата натрия. Если вы знаете концентрацию раствора тиосульфата натрия, легко подсчитать концентрацию ионов меди (II). Результатом этой попытки является получение простого соединения меди (I) в растворе.
Получение глицерата меди
Качественная реакция для выявления присутствия глицерина в растворах осуществляется в присутствии сульфата меди (II) и раствора гидроксида натрия. В результате реакции образуется глицерат меди – комплексное соединение сине-василькового оттенка. Химическую реакцию проводят следующим образом:
- к раствору сульфата меди (II) приливают раствор гидроксида натрия, в результате чего происходит окрашивание раствора в синий цвет. Таким образом, наблюдаем выпадения осадка гидроксида меди (II)
- после этого добавляем несколько мл глицерина и перемешиваем раствор. Образовавшийся осадок растворяется с образованием комплексного соединения оттенка индиго. Это и есть глицерат меди.
Уравнение выглядит следующим образом: CH2OH-CHOH-CH2OH + Cu(OH)2—> Cu(-O-CH2-CH-O-)-CH2OH
Фосфористая обработка
Рафинирование меди фосфористой – это фосфорная дезоксидированная жесткая медь, которая представляет собой прочную смолу общего назначения. Она раскисляется фосфором меди, в которой остаточный фосфор поддерживается на низком уровне (0,005-0,013 %) для достижения хорошей электропроводности. Обладает хорошей теплопроводностью и отличными свойствами сварки и пайки. Оксид после рафинирования меди таким способом, оставшийся в твердой смоле меди, удаляется фосфором, который является наиболее часто используемым дезоксидантом.
В таблице показана разные показатели от отожженного (мягкого) до жесткого состояния меди.
| Прочность на растяжение | 220-385 Н/мм2 |
| Прочность на разрыв | 60-325 Н/мм2 |
| Удлинение | 55-4 % |
| Твердость (HV) | 45-155 |
| Электропроводность | 90-98 % |
| Теплопроводность | 350-365 Вт/см |
Ведущие рамы соединяют проводку с электрическими клеммами на поверхности полупроводника и крупномасштабными схемами на электрических устройствах и печатных платах. Материал выбирается так, чтобы соответствовать требованиям процесса и быть надежным при установке и эксплуатации.
Пошаговая инструкция по выплавке меди
Если вы приняли решение организовать техпроцесс по плавлению металла в домашних условиях, в первую очередь, вам следует знать температуру кипения меди. Она составляет 2650°C. При этой температуре металл начинает кипеть и пузыриться. Изделие, отлитое при такой температуре, будет иметь высокое количество пор, что негативно скажется как на его механических, так и на декоративных свойствах.
Если правильно подготовить оборудование и организовать процесс плавки, то в домашних условиях можно получить качественные изделия как для технического, так и для бытового и декоративного применения.
Медная проволока
Для организации техпроцесса понадобятся следующее оборудование и расходные материалы:
- форма, в которую будет заливаться металл;
- газовая горелка;
- горн;
- уголь древесный;
- крюк из железной проволоки;
- пылесос со шлангом;
- щипцы железные (для извлечения тигля из печи);
- тигель для выплавки металла (обычно для таких целей используются керамические или глиняные тигли);
- муфельная печь.
Марки латуни и области применения
От состава зависит марка латуни и область её применения. Например, томпак, принадлежащий к классу деформируемых латуней, в котором содержится больше 95% меди, может легко соединяться со сталью, образуя с ней биметалл. Используется такое соединение в изготовлении знаков отличия и различных предметов искусства и интерьера — статуэток, рамок, подсвечников.
Латуни марки ЛО используются для изготовления конденсаторных трубок, применяемых в разной теплотехнической аппаратуре, например, газовых котлах, автоклавах, сильфонах.
Марка ЛС используется при создании деталей часовых механизмов, переходных и соединительных втулок. Из неё также изготавливают полиграфические матрицы.
ЛМц — содержится в старых советских монетах номиналом до 5 копеек, арматуре, гайках и болтах, а её подвид с приставкой «А» — в деталях речных и морских судов.
Латунь, имеющая маркировку ЛА или ЛЖМ (и её подвиды), также используется для постройки морских судов и самолётов, различных электрических машин и подшипников. Очень распространена в деталях для различной химической техники.
Электролиз расплавов
При электролизе расплава на аноде окисляются анионы кислотных остатков, а на катоде восстанавливаются катионы металлов. Молекул воды в системе нет.
Например: электролиз расплава хлорида натрия. На катоде восстанавли-ваются катионы натрия:
Катод (–): Na + + ē → Na 0
На аноде окисляются анионы хлора:
Анод (+): 2 Cl – – 2ē → Cl2 0
Суммарное уравнение электролиза расплава хлорида натрия:
2 Na + Cl – → 2 Na 0 + Cl2 0
Еще один пример: электролиз расплава гидроксида натрия. На катоде восстанавливаются катионы натрия:
Катод (–): Na + + ē → Na 0
На аноде окисляются гидроксид-ионы:
Анод (+): 4 OH – – 4ē → O2 0 + 2H2O
Суммарное уравнение электролиза расплава гидроксида натрия:
4 Na + OH – → 4 Na 0 + O2 0 + 2H2O
Многие металлы получают в промышленности электролизом расплавов.
Например , алюминий получают электролизом раствора оксида алюминия в расплаве криолита. Криолит – Na3[AlF6] плавится при более низкой температуре (1100 о С), чем оксид алюминия (2050 о С). А оксид алюминия отлично растворяется в расплавленном криолите.
В растворе криолите оксид алюминия диссоциирует на ионы:
На катоде восстанавливаются катионы алюминия:
Катод (–): Al 3+ + 3ē → Al 0
На аноде окисляются алюминат-ионы:
Анод (+): 4Al O 3 3 – – 12ē → 2Al2O3 + 3 O2 0
Общее уравнение электролиза раствора оксида алюминия в расплаве криолита:
2 Al 2 О 3 = 4 Al 0 + 3 О 2 0
В промышленности при электролизе оксида алюминия в качестве электродов используют графитовые стержни. При этом электроды частично окисляются (сгорают) в выделяющемся кислороде:
C 0 + О2 0 = C +4 O2 -2
Методы, используемые для плавления меди дома
Плавка меди в домашних условиях возможна несколькими способами. Для этого понадобятся определенные инструменты:
- сырье;
- жаропрочный тигель;
- огнеупорная подставка;
- проволочный крюк;
- щипцы для извлечения горячего тигля;
- средства защиты: очки, костюм, перчатки.
Плавление меди дома и на производстве происходит одинаково. Этого добиваются следующими методами:
- с помощью муфельной печи;
- с использованием кислородного пламени;
- горном;
- паяльной лампой;
- плавлением в микроволновой печи.
Процесс плавления меди в домашних условиях
С помощью муфельной печи
Литье меди с помощью муфельной печи — довольно простой и удобный метод. Медное сырье измельчают на части, чтобы они быстрее расплавились. Готовый материал кладут в графитовый тигель и помещают в разогретую печь. Форма для литья должна иметь большую температуру плавления, чем цветмет.
Когда сырье станет жидким, тигель с помощью щипцов извлекают из печи. Крюком с поверхности металла убирают оксидную пленку. Затем жидкость наливают в заранее подготовленную форму.
Из чего состоит муфельная печь
Газовая горелка или паяльная лампа
Плавление меди горелкой
Специальную печь может заменить газовая горелка или паяльная лампа. Ее размещают под дном емкости с металлом и следят, чтобы пламя охватывало днище полностью.
При использовании данного метода материал быстро окисляется, поэтому, чтобы не образовалась толстая оксидная пленка, сверху сырье присыпают частицами древесного угля.
Для плавления легкоплавких сплавов из латуни или бронзы вполне достаточно газовой горелки или паяльной лампы.
Горн
Расплавить медь можно с помощью горна. Для этого тигель с измельченным сырьем размещают на раскаленном древесном угле. Чтобы ускорить плавление, используют домашний пылесос, включенный в режиме выдувания. Труба должна иметь металлический зауженный наконечник, так как под воздействием высокой температуры пластик расплавится. Такой метод подойдет для тех, кто регулярно занимается плавлением меди дома.
Чтобы повысить температуру, следует вдувать в горн больше воздуха.
Чертеж передвижного горна
Самостоятельная выплавка меди
Для многих людей плавка меди и изготовление из нее всевозможных изделий является увлекательным хобби. Тем, кто мечтает посвятить плавлению металла свободное время, нужно приготовить для работы такие приспособления:
- муфельная печка;
- чистое сырье;
- жаропрочный тигель;
- огнеупорная подставка;
- крюк из стальной проволоки;
- щипцы для извлечения тигля из печки;
- средства индивидуальной защиты: костюм, очки, перчатки.
Действия выполняют согласно инструкции:
- Надевают специальный костюм.
- Исходное сырье измельчают, кладут в тигель.
- Помещают в печь, устанавливают нужный температурный режим. Нельзя допускать, чтобы металл закипал.
- При достижении заданной температуры открывают дверцу, захватывают тигель щипцами, достают из печи, ставят на огнеупорную подставку.
- Стальным крюком к краям емкости сдвигают, образовавшуюся в результате плавления, окисную пленку.
- Жидкую медную массу заливают в специальную емкость, охлаждают.
- В мощных муфельных печах можно подвергать плавлению красную медь и всевозможные сплавы.
Плавление горелкой
Следует помнить, что при плавлении важна азотная среда. Под легкоплавкие медные сплавы, латунь или некоторые марки бронзы можно использовать обычную газовую горелку. Для этого понадобится:
- исходное сырье;
- специальные формы;
- щипцы для извлечения металла с раскаленной рабочей поверхности;
- горелка высокого давления, работающая на газе;
- средства защиты: костюм, очки, перчатки.
Технология плавления сплавов следующая:
- Сырье сильно измельчают. Сделать это можно при помощи напильника, превратив материал в опилки.
- Кладут в специальную форму, сделанную из термостойкого материала.
- Надевают защитный костюм, очки, толстые перчатки.
- Зажигают горелку.
- Нагревательное устройство направляют свободными движениями по корпусу емкости. Для достижения быстрого результата пламя должно касаться поверхности кончиком синего цвета. В этом месте факела – наибольшая температура.
- После того как твердое тело расплавится, тигель захватывают щипцами.
- Жидкую массу выливают в нужную форму.
Если нет газовой горелки, можно использовать обыкновенную паяльную лампу.
Выполняя литье цветных сплавов, каждый мастер должен помнить о технике безопасности:
- В помещении, где ведутся работы, должна быть хорошая вентиляция.
- Во избежание получения ожогов необходимо работать в средствах индивидуальной защиты.
Оптимальная температура воздуха, допустимая влажность воздуха, чистота рабочего места, низкая концентрация вредных веществ атмосферы, хорошая освещенность пространства – факторы, помогающие избежать травматизма.