Коррозия (от позднелатинского corrōsiōn «грызть, жевать») представляет собой постепенно развивающийся процесс поверхностного повреждения металлов, обладающих способностью активно реагировать с кислородом. Один из наглядных примеров этого явления – коррозия металла из-за образования оксида железа Fe2O3 или ржавчины. Характерно, что два остальных окисла железа – закись FeO и закись-окись Fe3O4 — обладают значительно меньшей корродирующей способностью, причём Fe3O4 при некоторых условиях может даже играть роль твёрдой смазки.
Теория коррозии предполагает, что для начала разрушения металла необходимо наличие четырёх основных компонентов:
- Катода.
- Анода.
- Электрического соединения, которое существует между катодом и анодом.
- Электролита или любой другой токопроводящей среды, облегчающей направленное перемещение ионов.
Обычное образование ржавчины на стали можно рассматривать как электрическую батарейку. Когда атомы металлов подвергаются воздействию окружающей среды, которая содержит кислород, металл производит электроны. Это действие можно локально ограничить, чтобы создать трещину или микроуглубление. С развитием процесса коррозия распространяется на прилегающую территорию, что приведет к общему ухудшению состояния поверхности. Ограниченная (точечная) коррозия способна вызвать усталость металла – снижение его прочностных характеристик, а имеющиеся коррозионные агенты, например, морская вода, могут привести к прогрессирующему росту трещины.
Теория коррозии утверждает также, что интенсификации поверхностного разрушения металла способствуют микроструктурные изменения, возникающие при повышенных температурах, в частности, при сварке. Это объясняется повышенными значениями энергии активации, из-за чего количество ионов, проводящих электрический ток, лавинообразно возрастает.
Определение коррозии
Коррозия — это постепенное разрушение объектов, обычно металлов, вызванное активной окружающей средой-электролитом и химической реакцией окисления.
Суть коррозионного процесса – наличие постоянно действующей анодной реакции. Она вызывается за счёт растворения металла, который генерирует электроны. Часть энергии активации дополнительно расходуется на другой процесс, называемый катодной реакцией. Эти два процесса уравновешивают произведенные заряды. Зоны, вызывающие эти процессы, могут быть расположены близко или далеко друг от друга, в зависимости от ситуации.
Электроны, генерируемые в процессе, должны потребляться посредством катодной реакции. Ионы водорода и электроны вступают в реакцию с образованием атомарного, а затем и газообразного водорода. Однако водород является сильнейшим восстановителем, поэтому дальнейшую коррозию можно предотвратить, создав на поверхности металла тонкую газовую плёнку. Она служит поляризатором, уменьшающим контакт металла с водой и уменьшающим коррозию. Таким образом, всё, что разрушает барьерную плёнку, увеличивает скорость коррозии.
Основными факторами, определяющими интенсивность процесса, являются:
- Скорость;
- Температура;
- Уровень возникающих механических и термических напряжений;
- Характер протекающих химических реакций.
Коррозия сдерживает внедрение в производство новых металлических материалов и причиняет значительный ущерб экономике.
Применение ингибиторов коррозии
По свойствам эти сложные химические составы делятся на две группы – средства, уменьшающие коррозионную активность внешней среды (пассиваторы) и комплексы, образующие на поверхности защищаемого изделия предохраняющий от коррозии слой адсорбирующего типа (адсорбаторы).
Кстати, для тех, кто не знает точно, чем различаются аБсорбция и аДсорбция. В первом случае это поглощение из газовой среды веществ жидкостью, во втором – поглощение веществ из той же среды поверхностным слоем твердого тела.
Очень часто ингибиторы применяют в магистралях и локальных системах отопления. В этом случае существенно уменьшается внутренняя коррозия трубопроводов и радиаторов отопления под действием теплоносителя.
Важно: в автономных замкнутых системах, работающих на дистиллированной воде, применение ингибиторов коррозии обычно не обосновано.
Также ингибиторы, в сочетании с другими компонентами, используются для профилактики и очистки водопроводов, водонагревающих устройств.
Также широко распространено применение ингибиторов в строительстве, в том числе в создании арматуры железобетонных конструкций. Обработка специальным составом препятствует коррозии арматуры в монолите и продлевает срок службы железобетона. Также сохраняется нагрузочная способность конструкции, поскольку целостность арматуры позволяет сохранять нормальный уровень сопротивления нагрузкам.
Используются ингибиторы как в виде жидкостей, так и в виде газов, вводимых в окружающую изделие среду.
Виды коррозии металлов
Классификация всех коррозионных явлений может быть произведена по следующим параметрам:
- По степени равномерности. Различают поверхностную коррозию, которая равномерно уменьшает толщину поверхности, и неравномерную коррозию – точечную или язвенную;
- По интенсивности воздействия на металл. Например, избирательная коррозия разрушает только определённые структурные составляющие, а контактная воздействует на менее коррозионно стойкие («неблагородные») составляющие пар трения;
- При межкристаллитной коррозии разрушение происходит по границам зёрен и распространяется вглубь металла.
- Фреттинг-коррозия, когда два контактирующих между собой тела совершают относительно друг друга колебательные движения малой амплитуды (не более 100 мкм).
При одновременном воздействии растягивающих напряжений и агрессивной среды наблюдается коррозионное растрескивание межкристаллитного или транскристаллитного характера, а при наложении знакопеременных напряжений начинается коррозионно-усталостное разрушение. Защита металлов от коррозии, таким образом, предполагает также и одновременное уменьшение износа деталей.
Далее рассматриваются основные явления, которые происходят в повреждающихся зонах при различных видах коррозии.
Лекция на тему: «Коррозия и защита металлов»
Тема 5. Коррозия и защита металлов
5.1. Определение и классификация коррозийных процессов
Коррозия
– это разрушение металла в результате его физико–химического взаимодействия с окружающей средой. При этом металлы окисляются и образуются продукты, состав которых зависит от условий коррозии.
Химическая энергия реакции коррозионного разрушения металлов выделяется в виде теплоты и рассеивается в окружающем пространстве.
Коррозия приводит к большим потерям. Безвозвратные потери металлов от коррозии составляют 15% от ежегодного их выпуска.
Однако во многих случаях косвенные убытки от коррозии могут значительно превышать прямые потери за счет растворения металла. Замена прокорродировавшего котла или конденсатора на большой теплоэлектростанции может нанести энергосистеме существенный ущерб. Кроме того, к убыткам от коррозии можно отнести также стоимость потерянного продукта, например масла, газа, воды, через систему с прокорродированными трубами или антифриза через прокорродировавший радиатор.
В целом потери народного хозяйства от коррозии исчисляются многими миллиардами рублей ежегодно. Изучение коррозии и разработка методов защиты металлов от неё представляют теоретический интерес и имеют большое народнохозяйственное значение. По механизму протекания коррозионного процесса, зависящему от характера внешней среды, с которой взаимодействует металл, различают химическую и электрохимическую коррозию.
Среда в которой металл подвергается коррозии (коррозирует) называется коррозионной или агрессивной средой.
В случае с металлами, говоря об их коррозии, имеют ввиду нежелательный процесс взаимодействия металла со средой. Физико-химическая сущность изменений, которые претерпевает металл при коррозии является окисление металла.
Любой коррозионный процесс является многостадийным:
1) Необходим подвод коррозионной среды или отдельных ее компонентов к поверхности металла.
2) Взаимодействие среды с металлом.
3) Полный или частичный отвод продуктов от поверхности металла (в объем жидкости, если среда жидкая).
Известно что большинство металлов ( кроме Ag,Pt,Cu,Au) встречаются в природе в ионном состоянии: оксиды, сульфиды, карбонаты и др., называемые обычно руды металлов.
Ионное состояние более выгодно, оно характеризуется более меньшей внутренней энергией. Это заметно при получение металлов из руд и их коррозии. Поглощенная энергия при восстановлении металла из соединений свидетельствует о том , что свободный металл обладает более высокой энергией, чем металлическое соединение. Это приводит к тому, что металл находящийся в контакте с коррозионно-активной средой стремится перейти в энергетически выгодное состояние с меньшим запасом энергии.
То есть можно сказать, что первопричиной коррозии металла является термодинамическая неустойчивость металлов в заданной среде.
Классификация коррозионных процессов.
1. По механизму процесса различают химическую и электрохимическую коррозию металла.
Химическая коррозия — это взаимодействие металлов с коррозионной средой, при котором окисляется металл и восстанавливается окислительные компоненты коррозионной среды протекают в одном акте. Так протекает окисление большинства металлов в газовых средах содержащих окислитель (например, окисление в воздухе при повышении температуры)
Mg+ O -> MgO
4Al + 3O -> 2AlO
Электрохимическая коррозия — это взаимодействие металла с коррозионной средой, при котором ионизация атомов металла и восстановление окислительной компоненты среды происходит не водном акте, и их скорости зависят от электродного потенциала металла. По такому процессу протекают, например, взаимодействие металла с кислотами:
Zn + 2HCl -> Zn +2Cl +H
эта суммарная реакция состоит из двух актов:
Zn -> Zn + 2e
2H + 2e -> H
2. По характеру коррозионного разрушения.
Общая или сплошная коррозия при которой коррозирует вся поверхность металла. Она соответственно делится на равномерную (1а), не равномерную (1б) и избирательную (1в), при которой коррозионный процесс распространяется преимущественно по какой-либо структурной составляющей сплава.
Местная коррозия при которой коррозируют определенные участки металла:
а) коррозия язвами — коррозионные разрушения в виде отдельных средних и больших пятен (коррозия латуни в морской воде)
б) межкристаллическая коррозия при ней процесс коррозии распространяется по границе металл-сплав (алюминий сплавляется с хромоникелем) и другие виды коррозии.
3. По условиям протекания процесса.
а) Газовая коррозия — это коррозия в газовой среде при высоких температурах. (жидкий металл, при горячей прокатке, штамповке и др.)
б) Атмосферная коррозия — это коррозия металла в естественной атмосфере или атмосфере цеха (ржавление кровли, коррозия обшивки самолета).
в) Жидкостная коррозия — это коррозия в жидких средах: как в растворах электролитов, так и в растворах не электролитов.
г) Подземная коррозия — это коррозия металла в почве
д) Структурная коррозия — коррозия из-за структурной неоднородности металла.
е) Микробиологическая коррозия — результат действия бактерий
ж) Коррозия внешним током — воздействие внешнего источника тока (анодное или катодное заземление)
з) Коррозия блуждающими токами — прохождение тока по непредусмотренным путям по проекту.
и) Контактная коррозия — сопряжение разнородных электрохимических металлов в электропроводящей среде.
к) Коррозия под напряжением — одновременное воздействие коррозионной среды и механического напряжения.
Скорость коррозии выражают несколькими способами. Наиболее часто пользуются массовым и глубинным показателями коррозии. Первый из них даёт потерю массы (в граммах или килограммах) за единицу времени (секунду, час, сутки, год), отнесенную к единице площади (квадратный метр) испытуемого образца.
Глубинный показатель коррозии выражается уменьшением толщины металла в единицу времени.
5.2. Химическая коррозия
Наибольшее практическое значение имеет химическая коррозия в среде раскаленных газов, которая называется газовой коррозией.
В процессе окисления на поверхности металла образуется твердая пленка оксидов. Для дальнейшего продолжения коррозии необходимо, чтобы ионы металла или кислород (или оба одновременно) диффундировали через эту пленку. Обычно с поверхности раздела металл – оксид в направлении от металла к внешней поверхности пленки происходит диффузия ионов металла, а не атомов, так как ионы металлов по размерам меньше атомов.
Одновременно в этом же направлении должны перемещаться электроны. Ионы О2– имеют больший радиус, чем атомы, поэтому с поверхности раздела оксид – газ в глубь пленки двигаются не ионы, а атомы кислорода, которые в пленке ионизируются (О + 2е– = О2–) и, встречаясь с ионами металла, образуют оксиды.
Защитные свойства пленок зависит от соотношения между объёмами продуктов коррозии Vок и металла Vме, из которого они образовались:
Если Vок/ Vме1, то образующаяся пленка не может быть сплошной и защищать металл от коррозии. Скорость роста пленки во времени у таких металлов остается постоянной.
Для металлов, у которых в результате химической коррозии получаются сплошные пленки (Vок/Vме1), процесс коррозии будет тормозиться диффузией реагентов через пленку, и по мере утолщения пленки дальнейший рост её будет все время замедляться.
При этом пленка должна иметь некоторую оптимальную толщину, чтобы в достаточной степени тормозить встречную диффузию молекул агрессивного агента и ионов металла.
Скорость коррозии возрастает с увеличением температуры из–за повышения коэффициента диффузии и изменения защитных свойств пленки. Быстрое разрушение защитной пленки часто вызывают резкие температурные изменения. Это связано прежде всего с различными коэффициентами линейного расширения металла и пленки.
До сих пор рассматривалось образование, устойчивость и разрушение защитных оксидных пленок, возникающих на металле при химическом взаимодействии его с кислородом. Но помимо кислорода ряд других газов может обладать сильными агрессивными свойствами по отношению к металлам при повышенных температурах.
Наиболее активными газами являются фтор, диоксид серы, хлор, сероводород. Их агрессивность по отношению к различным металлам, а следовательно, и скорость коррозии последних не одинаковы.
Так, например, алюминий и его сплавы, хром и стали с высоким содержанием хрома устойчивы в атмосфере, содержащей в качестве основного агрессивного агента кислород, но становятся совершенно неустойчивыми, если в атмосфере присутствует хлор. Никель неустойчив в атмосфере диоксида серы, а медь вполне устойчива.
Коррозия низколегированных и углеродистых сталей в выхлопных газах двигателей внутреннего сгорания, в топочных и печных газах сильно зависит от соотношения СО и О2. Повышение содержания О2 увеличивает скорость газовой коррозии и, наоборот, повышение содержания СО ослабляет коррозию. Ряд металлов (СО, Ni, Cu, Pb,Cd, Ti) устойчив в атмосфере чистого водяного пара при температуре выше температуры кипения воды.
5.3. Электрохимическая коррозия
Электрохимическая коррозия возникает при условии, соли неоднородный металл или сплав находится в электролите, т. е. в растворе, содержащим ионы различных веществ. Электролитами обычно являются водные растворы солей, кислот или щелочей.
Было установлено, что при контакте металла и электролита начинает работать большое количество гальванических микроэлементов, в которых перенос электрических зарядов совершается так же, как и в обычных гальванических элементах, где один из электродов (анод) разрушается, поэтому такая коррозия называется электрохимической.
Рассмотрим подробно механизм электрохимической коррозии.
Если сначала отдельно погрузить какой–либо металл в электролит, то практически могут быть два случая: либо часть положительно заряженных ионов металла (катионов) перейдет в раствор и металл зарядится отрицательно, либо часть положительных ионов осядет из раствора на металле и зарядит его положительно.
Электролит при этом заряжается электричеством обратного знака, т.е. в первом случае положительно, а во втором–отрицательно. В обоих случаях металл приобретает определенный электрический заряд, количественно выражаемый его электродным потенциалом.
Значение потенциала определяется соотношением тех сил, которые, с одной стороны, удерживают ионы в кристаллической решетке металла, а с другой–в электролите. Таким образом, электродный потенциал зависит от природы металла, состава электролита, а также от температуры, поскольку последняя влияет на величину указанных сил.
Нам уже известно, что для выбранного электролита все металлы можно расположить в порядке изменения их потенциалов.
Рассмотрим теперь, что произойдет, если два металла, например медь и цинк, обладающие разными потенциалами, погрузить в общий электролит.
В данном случае анодом будет цинк, а катодом–медь. С анода перейдет в раствор большое число ионов металла [Zn++], соответственно на аноде скопится большой избыток электронов.
Если теперь соединить электроды между собой внешним проводником, то при наличии внешнего проводника электроны будут перемещаться по нему от анода к катоду, т. е., по проводнику потечёт электрический ток.
Притекая к катоду (меди), электроны начнут изменять его потенциал в отрицательную сторону; такое явление представляет частный случай поляризации
.
Вообще поляризацией
называется всякое изменение потенциала работающего электрода. Наоборот, восстановление первоначального значения потенциала называют
деполяризацией
, а вещества, способствующие этому, деполяризаторами.
В данном случае таким деполяризатором служит кислород, попадающий в электролит из воздуха путем растворения.
Этот кислород при участии воды может воспринимать электроны, попавшие на катод; при этом образуются гидроксильные ионы [ОН–];
О + Н2О + 2е 2ОН–
Таким образом, в итоге деполяризации, с одной стороны, с катода отводятся электроны, а с другой – вблизи него возникают гидроксильные группы. Оба эти процесса имеют важное значение. Отвод электронов с катода обеспечивает возможность притока к нему новых электронов со стороны анода, а это ведет к дальнейшему переходу ионов анода в раствор, т.е. к разрушению (коррозии) цинка. А образующиеся у катода гидроксильные ионы, перемещаясь в растворе путем диффузии, встречаются с ионами цинка и образуют продукт коррозии––гидрат окиси цинка:
Zn++ + 2OH–Zn (OH)2
Рассмотренный случай представляет собой пример коррозии с кислородной диполяризацией; по такой схеме корродируют стали и алюминиевые сплавы в обычных эксплуатационных средах.
В некоторых условиях процессы на катоде протекают иначе. Притекающие к катоду электроны соединяются с ионами водорода [Н+], всегда находящимися в водных растворах, при этом образуются нейтральные атомы водорода, которые, соединяясь попарно, образуют молекулы водорода, который выделяется с катода в виде газа:
2Н + 2е Н2
Данный случай представляет коррозию с водородной деполяризацией. По такой схеме коррозии, сопровождающейся выделением водорода, разрушаются, например, под действием морской воды магниевые сплавы, сюда же относятся случаи растворения металлов в кислотах.
Как видно, процессы электрохимической коррозии подобны процессам, протекающим в гальванических элементах.
Основным отличием процессов электрохимической коррозии от процессов в гальваническом элементе является отсутствие внешней цепи. Электроны в процессе коррозии не выходят из корродирующего металла, а двигаются внутри металла. Химическая энергия реакции окисления металла передается не в виде работы, а лишь в виде теплоты. Схема электрохимической коррозии железа в контакте с углеродом. На анодных участках происходит реакция окисления железа
Fe – 2eFe2+
На катодных участках происходит восстановление водорода
2Н+ + 2е– Н2
На рисунке представлена схема коррозии металла с энергетически неоднородной поверхностью, имеющей участки железа и углерода
Поэтому катодный процесс в основном будет протекать на этих участках; они называются катодными участками. Наличие участков, на которых катодные реакции протекают быстрее, увеличивает скорость коррозионного процесса. На других участках будет протекать в основном растворение металла и поэтому они называются анодными участками.
Катодные и анодные участки чередуются и имеют очень малые размеры, т. е. речь идет о микроанодах и микрокатодах и соответственно о коррозионных микроэлементах.
Таким образом, при наличии энергетической неоднородности поверхности металла коррозионный процесс заключается в работе числа коррозионных элементов. Коррозионный элемент в отличие от гальванического является короткозамкнутым микроэлементом.
Факторы, влияющие на коррозию
Факторы, влияющие на коррозию, распределяются на внутренние, зависящие от состава и строения имеющихся сплавов, и внешние, определяемые характером эксплуатационной среды.
Внутренние факторы.
Состав сплава — некоторые металлы и сплавы на их основе обладают значительной коррозионной стойкостью. Это прежде всего металлы, которые обладают положительными значениями электродных потенциалов: медь, золото, платина и т.п. Кроме того, к ним относятся металлы, которые при окислении способны образовывать хорошие защитные окисные пленки, например: хром, алюминий и алюминиевые сплавы, медные сплавы.
Наиболее стойкими являются сплавы, имеющие однородное строение, т.к. в этом случае зерна металла или сплава обладают одинаковыми потенциалами и электрохимическая коррозия не сможет развиваться.
Особенно неблагоприятными являются случаи, когда анодные участки располагаются по границам зерен сплава, так как при этом развивается очень опасная межкристаллитная коррозия.
К внутренним причинам, вызывающим коррозию, относятся также внутренние напряжения, возникающие при термической обработке или в эксплуатации, т. к. напряженный металл имеет более отрицательный потенциал.
Внешние факторы
.
К ним относятся состав коррозионной среды и условия коррозии: температура, давление, скорость движения среды. Среда и условия, в которых эксплуатируется авиационная техника являются весьма неблагоприятными, т.к. самолеты круглый год находятся на открытом воздухе, подвергаются действию осадков, пыли, солнечных лучей.
Важнейшим фактором, способствующим коррозии, является влага.
1. Обычно атмосферная влага содержит небольшие примеси солей, кислот, а также окислов азота, образующихся при грозовых разрядах. Часто она бывает загрязнена промышленными газами––сернистым газом (SO2), сероводородом (Н2S), хлористым водородом (HCl), аммиаком (NH3) и др. Все эти вещества, растворяясь в воде, образуют электролиты; т. е. активную коррозионную среду.
Влажный воздух приморских районов всегда содержит много солей, попавших из морской воды.
2. Другим естественным фактором, вызывающим коррозию, является пыль. Даже при отсутствии видимой влаги осевшая на металле пыль может явиться источником коррозии.
Дело в том, что пыль обычно содержит различные соли, обладающие гигроскопичностью и способные поглощать атмосферную влагу. В итоге в месте осевшей пылинки создается коррозийнный очаг, вызывающий местную коррозию металла; образующиеся при этом продукты коррозии также большей частью бывают гигроскопичными.
3. Коррозию способны вызвать различные жидкости, используемые в эксплуатации (охлаждающие, гидросмеси, кислоты и др.).
4. Причиной коррозии является контакт разнородных материалов в конструкции. Например, в контакте с медными сплавами разрушаются стали, алюминиевые и магниевые сплавы; последние разрушаются в контакте со сталью.
Зная потенциалы отдельных сплавов в данной эксплуатационной среде, можно заранее предсказать ход процесса коррозии и выбрать правильный метод защиты.
5.4. Защита металлов от коррозии
Коррозию металлов можно затормозить изменением потенциала металла, пассивированием металла, снижением концентрации окислителя, изменением состава металла и др. При разработке методов защиты от коррозии, используют указанные способы снижения коррозии и условий ее протекания. Выбор способа определяется его эффективностью, а также экономической целесообразностью. Все методы защиты условно делятся на следующие группы:
а) легирование металлов; б) защитные покрытия (металлические, неметаллические); в) электрохимическая защита; г) изменение свойств коррозийной среды; д) рациональное конструирование изделий.
Легирование металлов
Легирование металлов – эффективный (хотя и дорогой) метод повышения коррозионной стойкости металлов. При легировании в состав вводят компоненты, вызывающие пассивацию металла. Пассивностью
металла называется состояние его повышенной коррозионной устойчивости, вызванное торможением анодного процесса. Пассивность в основном вызывается образованием на поверхности металла оксидных или иных защитных слоев. В качестве таких пассивирующих компонентов применяют хром, никель, вольфрам и др.
Защитные покрытия
Слои, искусственно создаваемые на поверхности металлических изделий и сооружений для предохранения их от коррозии, называются защитными покрытиями. Если наряду с защитой от коррозии покрытие служит также для декоративных целей, его называют защитно–декоративным. Выбор вида покрытия зависит от условий, в которых используется металл. Материалами для металлических защитных покрытий могут быть как чистые металлы (цинк, кадмий, алюминий, никель, медь, хром, серебро и др.), так и их сплавы (бронза, латунь и др.). По характеру поведения металлических покрытий при коррозии их можно разделить на катодные и анодные.
К катодным покрытиям относятся покрытия, потенциалы которых в данной среде имеют более положительное значение, чем потенциал основного металла. В качестве примеров катодных покрытий на стали можно привести Cu, Ni, Ag.
При повреждении покрытия (или наличии пор) возникает коррозионный элемент, в котором основной материал в поре служит анодом и растворяется, а материал покрытия – катодом, на котором выделяется водород или поглощается кислород.
- раствор;2- покрытие;3- основной металл; 4- пора)
Следовательно, катодные покрытия могут защищать металл от коррозии лишь при отсутствии пор и повреждений покрытия.
Анодные покрытия имеют более отрицательный потенциал основного металла. Примером анодного покрытия может служить цинк на стали. В этом случае основной металл будет катодом коррозийного элемента, поэтому он не корродирует.
(1- раствор;2- покрытие;3- основной металл;4- пора)
Для получения металлических защитных покрытий применяются различные способы: электрохимический (гальванические покрытия), погружение в расплавленный металл, металлизация, термодиффузионный и химический.
При термодиффузионном
способе нанесения покрытия изделие помещают в смесь, содержащую порошок металла покрытия. При повышенной температуре происходит диффузия наносимого металла в основной металл.
Термодиффузионный способ широко используется для получения жаростойких покрытий алюминием (алитирование), кремнием (силицирование), хромом (хромирование), титаном (титанирование). Жаростойкие покрытия позволяют сочетать высокую жаропрочность основного материала с высокой жаростойкостью поверхностного слоя.
Химический
способ получения металлических покрытий заключается в восстановлении соединений металла с помощью водорода гидрозинa (продукт частичного откисления аммиака N2H4) и других восстановителей.
Неметаллические защитные покрытия могут быть как неорганическими, так и органическими. Защитное действие этих покрытий сводится в основном к изоляции металла от окружающей среды. В качестве неорганических покрытий применяют неорганические эмали, оксиды металлов, соединения хрома, фосфора и др. К органическим относятся лакокрасочные покрытия, покрытия смолами, пластмассами, полимерными пленками, резиной.
Ряд покрытий, получаемых химической обработкой металла, включает защитные покрытия, образующие непосредственно на поверхности металла. Образование на поверхности металлических изделий защитных оксидных пленок в технике называют оксидированием. Некоторые процессы имеют специальные названия. Так, например, процессы нанесения на сталь оксидных пленок иногда называют воронением
, а электрохимическое оксидирование алюминия –
анодированием
. Защитные свойства оксидных пленок повышают пропиткой их маслом.
Фосфатные покрытия на стали получают из растворов ортофосфорной кислоты и ортофосфатов марганца или цинка (например, ZnHPO4 +H3PO4). При реакции образуется пористый кристаллический фосфат металла, хорошо сцепленный с поверхностью стали. Сами по себе фосфатные покрытия не обеспечивают достаточной защиты от коррозии. Их используют в основном в качестве подложки под краску, что повышает сцепление лакокрасочного покрытия со сталью и уменьшает коррозию в местах царапин. Защитные свойства фосфатной пленки, полученной на металле, значительно повышаются после покрытия ее (или пропитки) лаком, маслом, воском.
Лакокрасочные покрытия наиболее распространены и незаменимы. Лакокрасочное покрытие должно быть сплошным, беспористым, газо- и водонепроницаемым, химически стойким, эластичным, обладать высоким сцеплением с материалом, механической прочностью и твердостью. К некоторым покрытиям предъявляются специальные требования: повышенная стойкость при высоких температурах, стойкость против кислот, щелочей, бензина и т.п.
Электрохимическая защита
Этот метод защиты основан на торможении анодных или катодных реакций коррозионного процесса. Электрохимическая защита осуществляется присоединением к защищаемой конструкции металла с более отрицательным значением электродного потенциала––протектора, а также катодной или анодной поляризацией за счет извне приложенного тока. Наиболее применима электрохимическая защита в коррозионных средах с хорошей ионной электрической проводимостью.
Катодная поляризация используется для защиты от коррозии подземных трубопроводов, кабелей. Катодную защиту применяют также к шлюзовым воротам, подводным лодкам, водным резервуарам, морским трубопроводам и оборудованию химических заводов.
Сущность катодной защиты заключается в том, что защищаемое изделие подключается к отрицательному полюсу внешнего источника постоянного тока, поэтому оно становится катодом, а анодом служит вспомогательный, обычно стальной электрод. Вспомогательный электрод (анод) растворяется, на защищаемом сооружении (катоде) выделяется водород. Если вспомогательный анод изготовлен из металла, имеющего более отрицательный потенциал, чем защищаемый металл, то возникает гальванический элемент. При этом отпадает необходимость в наложении тока от внешнего источника. Анод растворяется со скоростью, достаточной для создания в системе необходимого электрического тока.
Подобные вспомогательные электроды называют протекторами
. Для их изготовления большей частью используют магний и его сплавы, цинк, алюминий.
Изменение свойств коррозионной среды
Для снижения агрессивности среды уменьшают концентрацию компонентов, опасных в коррозионном отношении. Например, в нейтральных средах коррозия обычно протекает с поглощением кислорода. Его удаляют деаэрацией (кипячение, барботаж инертного газа) или восстанавливают с помощью соответствующих восстановителей (сульфаты, гидразин и т. п.). агрессивность среды может уменьшаться также при снижении концентрации ионов Н+, т. е. повышении рН (подщелачивании). Для защиты от коррозии широко применяют ингибиторы.
Ингибитором
называется вещество, при добавлении которого в среду, где находится металл, значительно уменьшается скорость коррозии металла. Ингибиторы применяют главным образом в системах, работающих с постоянным или мало обновляемым объемом раствора, например в некоторых химических аппаратах, системах охлаждения, парогенераторах и т. п. Особенно большое применение находят замедлители в процессах травления металлов для удаления с поверхности окалины или ржавчины.
Механизм действия значительного числа ингибиторов заключается в адсорбции ингибитора на корродирующей поверхности и последующем торможении катодных или анодных процессов.
Катодные замедлители уменьшают скорость коррозии за счет снижения интенсивности катодного процесса или сокращения площади катодных участков. К катодным ингибиторам относятся органические вещества, содержащие азот, серу и кислород, например диэтиламин, уротропин, формальдегид, тиокрезол.
В последние годы широко применяют летучие парофазные ингибиторы. Их используют для защиты машин, аппаратов и других металлических изделий во время их эксплуатации в воздушной атмосфере, при перевозке и хранении. Летучие ингибиторы вводятся в контейнеры, в упаковочные материалы или помещаются в непосредственной близости от рабочего аппарата.
Рациональное конструирование изделий
Рациональное конструирование изделий должно исключать наличие или сокращать число и размеры особо опасных с точки зрения коррозии участков в изделиях или конструкциях (сварных швов, узких щелей, контактов разнородных по электродным потенциалам металлов и др.), а также предусматривать специальную защиту металла этих участков от коррозии.
13
Химическая
Химическая коррозия относится к постепенному разрушению поверхности металла из-за реакции поверхности с веществами во внешней среде. Она происходит в результате окисления металла кислотами с образованием оксидов.
Высокотемпературный вариант заключается в воздействии на металл сухих газов. Все металлы в сухом воздухе покрыты очень тонким (2…10 мкм) слоем оксидов. Этот слой образуется при очень высоких температурах, когда реакция с кислородом воздуха идёт без каких-либо ограничений. При комнатной температуре реакция останавливается, поскольку оксидная плёнка становится слишком тонкой. В случае, например, с алюминием, такая плёнка, состоящая из оксида Al2O3,эффективно защищает поверхность алюминиевой посуды, поскольку коррозионная стойкость чистого алюминия невысока.
Химическая коррозия начинается в месте, где металл находится под давлением и изолирован от циркуляции воздуха. Это побуждает ионы металлов растворяться во влажной среде, что в конечном итоге ускоряет реакцию между ними и водой. В результате реакции образуются водные оксиды (известные при взаимодействии с железом как ржавчина) и свободные ионы.
Виды
Коррозионные процессы классифицируются зависимо от разных критериев. Основные из них — цвет, механизм образования ржавчины, тип агрессивной среды, характер разрушения.
По цвету
Зависимо от цвета бывают разные виды ржавчины. Она может быть черной, желтой, коричневой, красной. Оттенок зависит от химической формулы образовавшегося вещества.
Ржавый металл
Желтая
Химическая формула желтой ржавчины — FeO(OH)H2O. Она появляется под воздействием высокой влажности, в среде с малым количеством кислорода. Подобный вид ржавчины можно увидеть под водой.
Коричневая
Химическая формула коричневой ржавчины — Fe2O3. Встречается крайне редко, появляется без воздействия влаги.
Красная
Химическая формула красной ржавчины — Fe2O3•H2O. Образуется при одновременном воздействием воды и кислорода. Встречается чаще других видов. Разрушительный процесс протекает равномерно, постепенно распространяется на всю поверхность.
Черная
Химическая формула — Fe3O4. Появляется без воздействия влаги, в среде с малым количеством кислорода. Часто используется для создания сверхпроводников, поскольку является ферромагнетиком.
По механизму протекания
Виды:
- химическая;
- электромеханическая.
Процессы отличаются по механизму разрушения материала.
Химическая
Процесс разрушения металла, провоцирующий распад металлических связей, развитие химических реакций между атомами материала. Элементы, которые взаимодействуют между собой, пространственно не разделяются. Скорость разрушения детали зависит от скорости протекания химической реакции.
Электрохимическая
Данный процесс разрушения металлических деталей протекает в среде электролитов и сочетается с возникновением тока.
Ржавый корабль
По типу агрессивной среды
Виды:
- Атмосферная.
- Газовая.
- Радиационная.
- Подземная.
- Контактная.
- Биокоррозия.
- Коррозия током.
- Коррозийная кавитация.
- Коррозия под напряжением.
- Фреттинг-коррозия.
Атмосферная
Естественный процесс разрушения. Может протекать в воздушной или газовой атмосфере. Важное условие — повышенный уровень влажности. Чем он выше, тем быстрее разрушится материал.
Газовая
Процесс разрушения металлических деталей, который протекает в условиях газовой среды. Отличается низким уровнем влажности. Процесс образования ржавчины ускоряется при повышении температуры.
Радиационная
Возникает при интенсивном воздействии радиационного излучения. У сплавов высокой плотности протекает медленно.
Подземная
Если металлическая деталь какое-то время полежит под землей, можно заметить на ее поверхностях зеленый налет или другие цветовые искажения. Это следствие окислительный процессов, которые протекают в разных видах грунта.
Контактная
Быстро появляется в местах, где два разных металла соприкасаются друг с другом. Это обуславливается разницей стационарного потенциала в электролите.
Биокоррозия
Процесс разрушения металлических деталей, который обуславливается воздействием разных микроорганизмов, продуктов их жизнедеятельности.
Ржавые обломки судов
Коррозия током
Может происходить при воздействии блуждающего или внешнего тока. Скорость распространения ржавчины зависит от силы тока, длительности, периодичности его воздействия на металлические детали.
Коррозийная кавитация
Один из многочисленных процессов саморазрушения разных видов металлов. Он запускается при воздействии внешней среды, механического повреждении.
Коррозия под напряжением
Процесс разрушения сплавов, который происходит при взаимодействии механического напряжения с коррозийно-активной средой. Этот вид коррозии опасен для металлоконструкций, которые подвержены большим нагрузкам.
Фреттинг-коррозия
Сложный коррозионный процесс, который протекает под воздействием коррозийной среды с различными вибрациями. Чтобы не допустить образования ржавчины, важно снизить коэффициент трения металлических деталей.
По характеру разрушения
Виды:
- сплошная;
- избирательная;
- местная;
- подповерхностная;
- межкристаллическая;
- щелевая.
Они отличаются локализацией, степенью углубления в материал, тяжестью разрушения.
Сплошная
При таком коррозионном процессе ржавчиной покрываются все металлические поверхности. Она может быть равномерной или неравномерной, зависимо от скорости разрушения материала в разных местах детали.
Избирательная
Подобный процесс затрагивает один из элементов металлоконструкции, который не имеет антикоррозийного покрытия, затормаживающего процесс разрушения.
Ржавый автомобиль (Фото: pixabay.com)
Местная
Пятна ржавчины разбросаны по металлической поверхности. Они представляют собой углубления разного размера, одна часть которых могут быть поверхностными, другие сквозными.
Подповерхностная
Появляется под металлическими поверхностями. Она быстро проникает вглубь материала. Данный вид коррозионных процессов характеризуется расслоением металла.
Межкристаллическая
Начинает появляться по границам отдельных зерен материала. Ее крайне сложно выявить по внешнему виду. Быстро ухудшаются показатели плотности, прочности, пластичности. Детали становятся хрупкими.
Щелевая
Образуется на местах соединения двух металлических деталей. Может появляться в технологических зазорах, под техническими прокладками.
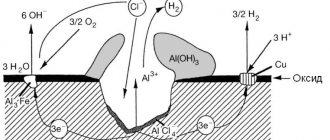
Электрохимическая
Для моделирования процесса необходимо рассмотреть железную пластину, покрытую любым электропроводящим покрытием, например, оксидной окалиной, которая образовалась во время высокотемпературной обработки. При погружении пластины в раствор хлорида натрия, обнаруживается, что, если повредить целостность окалины, в этом месте ржавление железа пойдёт значительно быстрее. Электрохимическая коррозия наиболее достоверно объясняет ржавление железа в аэробных условиях.
Теория электрохимической коррозии предполагает наличие дополнительных химических реакций:
- Fe → Fe ++ + 2e−, — анодная реакция;
- 2e− + O + H2O → 2OH− — катодная реакция.
Когда ионы металла растворяются, их заряд уравновешивается ионами хлорида, которые мигрируют в область атаки, притягиваясь образующимися ионами положительного заряда. Хлорид железа растворяется в воде, но это не создаёт препятствий для дальнейшей коррозии, поскольку раствор хлорида железа вследствие гидролиза очень кислый. По мере того, как ионы Fe ++ удаляются из этого места, они сталкиваются с гидроксильными ионами, которые либо присутствуют в воде естественным образом, либо образуются в результате катодной реакции. Результатом является образование и осаждение гидроксида железа Fe (OH)2. Далее, в присутствии растворённого кислорода, он быстро окисляется до оксигидроксида железа FeOOH.
Таким образом, при электрохимической коррозии происходят три реакции, причём в трёх разных местах. Анодная происходит в зонах потери металла, катодная – там, где растворённый в воде кислород может принимать электроны, а сама твёрдая окалина формируется в местах механических повреждений на поверхности изделия.
В последнее время выделяют ещё один вид коррозии – механохимическую, которая происходит в результате динамического взаимодействия контактирующих элементов окружающей среды в условиях высоких контактных давлений.
Защита металлических материалов от коррозии в нейтральных аэрируемых средах
Применение устойчивых металлов и сплавов
- с повышенной термодинамической устойчивостью, например медь и сплавы на ее основе (латуни и бронзы), являющиеся достаточно устойчивыми в морской воде (jCu= + 0,35B
), медь применяют как в виде чистого металла, так и в виде сплавов с другими металлами – с цинком (латунь), цинком и алюминием, оловом или никелем (специальные латуни), оловом (оловянная бронза), алюминием (алюминиевая бронза), никелем (медно-никелевый сплав), медь широко используется как материал для арматуры водопроводных линий и отопительных систем; - склонные к пассивированию: алюминий (j0Al= — 1,67B
) и его сплавы (AlMn1, AlMn1Mg1, AlMgSi, AlZn5Mg1, AlZnMgCu и др.) пассивирующиеся в кислородосодержащих средах с образованием оксидной пленки из
Al2O3
или
Al2O3∙H2O
(устойчив в средах с
pH= 3-9
); коррозионная устойчивость чистого алюминия понижается при наличии в нем катодных или анодных включений; титан
(jTi= — 1,63B
) и его сплавы, обладающие склонностью к переходу в пассивное состояние в нейтральных и окислительных средах, например в морской воде; легирование титана компонентами, повышающими анодную пассивируемость (Mo, Ta, Nb, Zr, Cr) или катодными добавками (Pd, Pt, Ru, Re), облегчающими переход в пассивное состояние, позволяет получать сплавы с высокой коррозионной устойчивостью не только в нейтральных средах, но и в растворахкислот; никель
(jNi= — 0,25B)
и его сплавы с медью, молибденом и хромом которые в сильноокислительных средах пассивируются; эти сплавы устойчивы в щелочах различных концентраций, в растворах многих солей, в атмосфере и в природных водах; высокие прочностные и коррозионные свойства имеют сплавы никеля с медью – монели, содержащие около 30 % меди и 3…3 % марганца, алюминия, железа; - покрывающиеся защитными пленками вторичных, труднорастворимых продуктов коррозии (ZnвH2O,Pb
в сульфатных растворах).
Удаление из электролита деполяризатора-кислорода (деаэрация электролита, обескислороживание
Деаэрирование применяют для удаления из воды растворенного кислорода.
Различают:
- термическое деаэрирование, при котором воду оборабатывыают паром в отдельном агрегате; в основе метода лежит тот факт, что растворимость кислорода падает с ростом температуры;
- химическое деаэрирование, при котором растворенный в воде кислород удаляется посредством реакции с сульфитом натрия (Na2SO3) или гидразином (N2H4) по следующим уравнениям:
Введение в электролит различных добавок, замедляющих течение коррозии
В одном случае это – торможение анодного процесса за счет введения в электролит веществ – пассиваторов (K2CrO4
,NaNo2
и др.). Кроме того, используются вещества – ингибиторы коррозии (ИК).
Они замедляют коррозию металлов в определенной коррозионной среде и придают им защитную способность при введении в вещества или материалы.
Различают ингибиторы кислотной коррозии, растворов щелочей, неводных сред (бензин, нефть и другие), нейтральных сред и атмосферной коррозии.
В качестве ингибиторов коррозии для нейтральных сред применяют, в частности анодные ингибиторы, влияющие на анодную реакцию.
Некоторые анодные ингибиторы, например хромат-ионы (CrO42-)
и нитрит-ионы
(NO2—)
, а в присутствии воздуха фосфаты и молибдаты, действуют, вызывая образование защитного (пассивного) оксидного слоя на поверхности стали.
Но, если концентрация ингибитора слишком мала, в оксидном слое могут возникать поры и дефекты, где может наблюдаться ускоренная коррозия. Поэтому такие ингибиторы называют «опасными ингибиторами».
Создание на поверхности металлических материалов защитных покрытий:
Металлических (Zn-,Cd-,Ni-,Pb
— покрытия на поверхности стальных изделий);
По способу защитного действия металлические покрытия делятся на катодные и анодные.
Катодные покрытия из Pb,Cu,Ni
созданные на поверхности стальных изделий защищают последние чисто механически, т.к. величина их электродного потенциала
(jп)
больше, чем у стали
(jп>jFe)
. Поэтому главное, предъявляемое к ним требование — их беспористость.
Анодные покрытия из Zn
,Cd
, ввиду того, что
jп<jFe
, защищают изделие не только механически, но главным образом электрохимически, участвуя в анодном процессе вместо защищаемого стального изделия.
Основной метод создания металлических покрытий – гальванический. В последние годы широкое распространение получают методы напыления – плазменное, газофазное, термодиффузионное и др.
Неметаллических неорганических;
- К неметаллическим неорганическим покрытиям относятся оксидные и фосфатные.
- Оксидные покрытия создаются способом оксидирования – создание на поверхности защищаемого металлического изделия оксидной пленки, возникающей в процессе анодного растворения поверхности защищаемого металла.
Например, оксидирование алюминия сводится к реакции вида:
2Al
+ 3H20 =Al2O3+ 3H2.
Оксидирование черных металлов – воронение. Его проводят химическим, термохимическим и электрохимическим способами. На железе и его сплавах образуется пленка магнитного оксида железа Fe3O4 . Ее стойкость невелика, поэтому она выполняет, в основном, декоративные функции.
Фосфатные покрытия создаются в процессе фосфатирования – обработки стальных и алюминиевых изделий в горячем растворе фосфорнокислых солей Fe,Zn .
При этом на поверхности стального изделия образуется пленка труднорастворимых фосфатов (FeHPO4 или Fe3(PO4)2). Пленка пористая и хорошо “впитывает” масло и краску, надежно защищая сталь от коррозии. Фосфатированию главным образом подвергают сталь.
Различают несколько вариантов процесса: чаще всего применяют цинковое фосфатирование, железное фосфатирование или натрийамонийное ; существует также марганцевое фосфатирование.
При цинковом фосфатировании стальная поверхность обрабатывается в ванне, содержащей Н3РО4 ,кислый фосфат, ионы цинка и некоторые добавки, например фториды, ионы никеля и органических соединений.
При обработке происходит окисление и некоторое растворение железа с поверхности, а вблизи нее незначительно повышается рН. В результате на поверхности осаждаются труднорастворимые железо-цинковые или цинковые фосфаты. Масса покрытия в зависимости от условий, колеблется от 0,2 до 30 г/см3.
Само по себе фосфатное покрытие слабо защищает от коррозии, но в сочетании с последующей пропиткой маслом дает хорошую защиту, так как пористое покрытие может поглощать значительное количество масла. Метод применяется для защиты оружия, перфораторов и некоторых деталей машин.
Комбинация фосфатирования с противокоррозионным окрашиванием широко применяется для изделий из холоднокатаных стальных листов, например кузовов автомобилей.
Железное или натрийаммонийное фосфатирование применяется только для сталей. Его проводят в ванне, содержащей натрийдигидрофосфат (NaH2PO4) или аммонийдигидрофосфат (NH4H2PO4) при рН = 4,0…5,5.
Образовавшееся покрытие состоит из фосфата железа (Fe3(PO4)2·8H2O), магнетита (Fe3O4) и некоторых железо-хромистых соединений – результат заключительной промывки раствором, содержащим хромовую кислоту – H2CrO4 и ионы Cr3+.
Оно имеет массу от 0,2 до 1,0 г/м2 и в зависимости от условий может быть желто-зеленым, фиолетовым, синим или серым.
Железное фосфатирование проводят как подготовку под окрашивание для улучшения адгезии лакокрасочного слоя к основе. Метод применим для конструкций из листового металла, например, для бытовых машин.
Методы защиты от коррозии
Ржавчина и другие коррозионные проявления могут приводить к проблемам с безопасностью, нарушать целостность производственного оборудования и расходных материалов. Даже плановое техническое обслуживание по удалению и устранению ржавчины увеличивает эксплуатационные затрат. Отработано ряд способов, используя которые, можно минимизировать коррозию.
Способы удаления коррозии
Если ржавчина уже появилась, удалить ее можно разными способами — механическим, химическим. Также можно воспользоваться народными средствами.
Ржавый замок (Фото: pixabay.com)
Механическая очистка
Подразумевает использование абразивных инструментов. Поврежденные части будут очищаться путем трения.
Щеткой по металлу
Представляет собой классическую ручную щетку со множеством металлических волокон, которыми происходит зачистка. Подходит для частичного удаления последствий коррозии.
Металлические покрытия
Эти методы предотвращения коррозии заключаются в погружении стали в расплав металла, электрический потенциал которого меньше, чем железа (чем больше разница, тем эффективнее покрытие).
Практическое применение находят гальванические покрытия цинком или оловом, а также диффузионные покрытия никелем, хромом, кремнием или алюминием. По сравнению с другими методами защиты от коррозии гальванизация известна более низкими начальными затратами, устойчивостью и универсальностью.
Поскольку расход металла-протектора довольно велик, преимущество получают технологии, отличающиеся экономичностью используемых компонентов и прочностью создаваемых покрытий. Первым в этом списке находится цинкование. Железо в стали вступает в реакцию с цинком, образуя прочное покрытие из сплава, которое служит защитой.
Эффективная защита металла цинковым покрытием
Для продления срока службы металлических изделий и конструкций необходимо обеспечить их защиту от влаги и других внешних воздействий. Чтобы придать металлу антикоррозионные свойства используется защитное покрытие цинком. Такая обработка называется цинкованием. Технологию покрытия различных металлов цинком изобрели более 200 лет назад, и она активно применяется и в настоящее время, благодаря высокой эффективности защиты и долговечности антикоррозионного слоя.
Используются различные способы нанесения – горячее, гальваническое, газодинамическое, диффузное, холодное цинкование. Металл, покрытый тонким слоем цинка (80-200 мкм), не ржавеет более 50 лет. Цинковое покрытие со временем истончается и его необходимо возобновлять. В зависимости от условий эксплуатации металлической конструкции показатель потерь цинковой поверхности составляет 1-6 мкм в год. Для сравнения, лакокрасочные покрытия, которыми защищают металл, необходимо возобновлять не реже 1 раза в 5 лет.
Свойства цинковых покрытий:
- Высокая степень защиты от коррозии.
- Электрохимическая (катодная) защита металлических изделий и конструкций.
Неметаллические покрытия
Один из самых простых способов предотвратить коррозию — использовать защитные покрытия из неметаллов — краски, пластика, воска или порошка. Порошки, включая эпоксидную смолу, нейлон и уретан, наносятся на металлическую поверхность и нагреваются до стадии расплавления, образуя тонкую плёнку.
Краска действует как покрытие, защищающее металлическую поверхность от электрохимического заряда, который исходит от коррозионно опасных соединений. Обычно используют комбинацию различных слоёв краски, которые выполняют разные функции. Грунтовка действует как ингибитор, промежуточный слой увеличивает общую толщину краски, а финишный слой обеспечивает устойчивость к факторам окружающей среды.
Основные методы цинкования
Покрытие металла цинком – это лучший метод защиты железных поверхностей от образования коррозии.
Цинкование выполняется такими способами:
- Горячее цинкование. Погружение железного листового, сортового или фасонного металлопроката в расплавленный цинк, температура которого составляет 460-480 градусов. Эта технология позволяет надолго защищать металл от коррозии, но отличается сложностью и небезопасностью выполнения. К другим недостаткам относятся: ограничение обработки размерами ванн, возможность деформации тонких конструкций и листов при нагреве, повреждение защитного слоя при сварке.
- Холодное цинкование. Считается оптимальным способом защиты металла цинком. Выполняется путем окрашивания металлических поверхностей порошкообразным грунтом с 96-98%-ным содержанием цинка. Покрытие наносится валиком или кистью прямо на месте установки конструкции (т.е. для антикоррозийной защиты не нужно перевозить изделие). Холодное цинкование дает возможность защищать железо от образования ржавчины на протяжении 30-50 лет, под слоем цинкового грунта металл коррозирует в три раза медленнее, по сравнению с другими методами обработки. К другим достоинствам этой технологии относится экономичность (по сравнению с горячим цинкованием). Недостатки: сложность покрытия неравномерных поверхностей и внутренних полостей.
- Газо-термический способ. Нанесение расплавленного цинка на металлическую поверхность в газовом потоке. Такая технология подходит для крупногабаритных металлоконструкций, не помещающихся в ванне с цинковым раствором. Покрытие служит в течение 25-30 лет. Минусами технологии является неравномерность получаемого покрытия, которое дополняется нанесением лакокрасочного покрытия.
- Термодиффузионный способ. Вплавление атомов цинка в железо при высокой температуре (более 2600 градусов). При такой температуре цинк переходит в газообразное состояние, после чего происходит диффузия молекул цинка с металлом. Плюсы метода: высокий класс антикоррозионной защиты, сохранение конфигурации изделий, возможность регулировать толщину цинкового покрытия, отсутствие необходимости очистки отходов. Минусы: неоднородность толщины защитной пленки, низкая производительность и вредность технологического процесса.
- Гальванический способ. Электролитический метод цинкования, позволяющий наносить тонкий (5-40 мкм) слой цинка на обезжиренную металлическую поверхность. Состоит в помещении металла и цинковых пластинок в электролитический раствор и подключении электрического тока. Цинк растворяется в электролите и оседает на железе в виде защитного слоя. Отличается равномерностью и гладкостью слоя покрытия, в том числе метизов сложной конфигурации и пористых поверхностей. Недостатки: высокая себестоимость, необходимость очистки отходов перед сливом в канализацию.
Выбор технологии цинкования зависит от требований к техническим характеристикам покрытия, условий эксплуатации металлоизделий или конструкций. Если у вас есть вопросы о том, как цинк защищает металл от коррозии и какой способ цинкования подойдет для того или иного вида металлопроката, вы может получить консультацию у специалиста нашей компании.
Химические покрытия
Относятся к методам временной антикоррозионной защиты стали, например, во время пластического деформирования при повышенных температурах. Наибольшее распространение получили технологии фосфатирования и оксалатирования.
При фосфатировании поверхность покрывают сплошным слоем фосфатных солей железа и марганца, а при оксалатировании – водорастворимыми солями щавелевой кислоты. Фосфатирование используется для обработки нелегированных сталей, оксалатирование – легированных. Покрытие прочно сцепляется с поверхностью, способствуя снижению трения и уменьшению износа инструмента. После окончания штамповки покрытие удаляют.
Изменение состава технического металла и коррозионной среды
Заключается в специальном легировании стали элементами, повышающими её коррозионную стойкость. Если это возможно, то в механическую систему, которая работает в условиях повышенной температуры и влажности, вводят смазку, содержащую противокоррозионные компоненты (восстановители).
Элементом, который положительно влияет на коррозионную стойкость стали, является хром. Для реализации этого эффекта сталь должна содержать не менее 13% хрома. Каждые дополнительные 5% хрома обеспечивают еще лучшую коррозионную стойкость.
Никель — второй важный элемент для улучшения коррозионной стойкости стали, причём добавка никеля приводит также к стабилизации аустенита. Третьим важным элементом повышения коррозионной стойкости является молибден. Однако его добавки повышают коррозионную стойкость только нержавеющих сталей с достаточным содержанием хрома и никеля.
Электрохимическая защита
Процесс коррозии, которая возникает при контакте двух разных металлов, находящихся в электролите, можно остановить использованием системы катодной защиты. Для реализации метода активные центры на поверхности металла необходимо преобразовать в пассивные путем предоставления электронов из другого источника (обычно используют аноды, прикрепленные к поверхности). Металлы, используемые для анодов — алюминий, магний или цинк.
Катодная защита очень эффективна в бытовой технике, однако аноды необходимо часто проверять, что увеличивает расходы на техническое обслуживание.