Когда металл помещается в почву, он оказывается во враждебной среде, способной спровоцировать появление коррозии.
Если не защитить металл, столкнетесь с проблемой разрушения, потерей целостности стальных опор и другими сложностями.
В этой статье мы подробно расскажем, что такое почвенная коррозия металла, как появляется и какие факторы способны усугубить положение. Также мы затронем и вопросы защиты, позволяющей свести к минимуму негативное воздействие агрессивной среды.
Долговечность металлической винтовой сваи с учетом коррозионных процессов в грунте
Одним из наиболее существенных вопросов, возникающих при применении металлических конструкций в строительстве, является вопрос сопротивления таких конструкций процессам коррозии и связанная с ним долговечность зданий и сооружений.
В настоящее время существует комплекс взаимоувязанных межгосударственных стандартов, устанавливающих общие требования, правила, нормы и методы защиты изделий, конструкций и материалов от коррозии, старения и биоповреждений на всех стадиях жизненного цикла изделий и конструкций исследование и обоснование разработки (Стандарты ЕСЗКС – Единая система защиты от коррозии и старения материалов и изделий) [1, 2, 3, 4].
Назначение ЕСЗКС – обеспечение и сохранение заданного уровня качества изделий, конструкций и материалов средствами и методами защиты от коррозии, старения и биоповреждений с учетом требований безопасности, экологии, совместимости и взаимозаменяемости, а также конкурентной способности изделий и конструкций на мировом рынке.
Помимо стандартов ЕСЗКС, требования к коррозионной стойкости устанавливаются также нормативами на отдельные виды конструкций и их частей в зависимости от действующих коррозионных факторов.
Для подземных сооружений (в т.ч. фундаментов), критериями опасности коррозии являются:
коррозионная агрессивность среды ( грунтов , грунтовых и других вод) по отношению к металлу сооружения (включая биокоррозионную агрессивность грунтов );
опасное действие блуждающего постоянного и переменного токов.
Исходя из этих критериев, следует, что скорость коррозии металла в грунте зависит от:
pH грунта. Чем ниже pH (кислая среда), тем скорость коррозии выше.
электрического сопротивления грунта. Чем выше сопротивление грунта, тем скорость коррозии медленнее.
Также необходимо учитывать наличие антикоррозионного покрытия, препятствующего коррозии.
Исследования по определению электрического сопротивления грунта с учетом возможного повышения влажности и изменения температуры проводились Федеральным дорожным агентством и отражены в руководстве для инженеров транспорта (табл.1).
Источник
4.2. Подземная коррозия
Подземная коррозия металлических конструкций протекает в почвенных или грунтовых условиях и имеет обычно электрохимический механизм. Подземной коррозии подвержены, главным образом, металлические трубопроводы, подземные резервуары, силовые электрические кабели и др. Особенно сильное разрушение наблюдается в условиях совместного воздействия грунта и блуждающих токов.
Различают следующие виды почвенной коррозии:
– Подземная коррозия – коррозия в почве, вызываемая коррозионными элементами, возникающими на металле в местах соприкосновения его с коррозионной средой вследствие неоднородности металла сооружения, неодинакового состава почвы, различия температур, влажности и воздухопроводности почвы на различных участках сооружения.
– Подземная биокоррозия – это коррозия, вызываемая жизнедеятельностью микроорганизмов, воздействующих на металл, обычно процесс завершается электрохимической коррозией.
– Электрокоррозия – коррозия металлических подземных сооружений под действием токов утечки с рельсов электрифицированных железных дорог и других промышленных установок. Она подразделяется на коррозию блуждающими токами и коррозию внешним током.
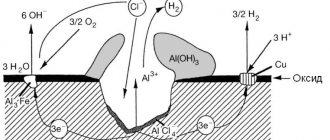
В почве содержатся влага и различные химические реагенты, поэтому она обладает ионной проводимостью и в большинстве случаев, за исключением очень сухих грунтов, механизм подземной коррозии – электрохимический. Наиболее характерным катодным процессом в подземных условиях является кислородная деполяризация. В кислых грунтах (болотистый) может проходить коррозия и с водородной деполяризацией. Рассмотрим пример работы коррозионного элемента в почве.
На аноде протекает реакция окисления железа с образованием гидратированных ионов:
На катоде протекает реакция ионизации кислорода:
В электролите почвы ионы
и
взаимодействуют друг с другом, образуя нерастворимый осадок гидроксида железа, который затем может перейти в оксид железа:
,
.
Анодные и катодные процессы, в большинстве случаев, протекают на различных участках, т.е. поверхность корродирующего металла состоит из некоторого числа коррозионных микроэлементов и общая скорость коррозии зависит от числа таких элементов и интенсивности их работы. Такой механизм коррозии называют гетерогенно-электрохимическим.
Общая скорость коррозии определяется скоростью процесса, протекающего медленнее других. Процесс, кинетика которого определяет общую скорость коррозии, называется контролирующим.
В зависимости от условий возможны следующие виды контроля подземной коррозии металлов: преимущественно катодный контроль – во влажных грунтах; преимущественно анодный контроль – в рыхлых и сухих грунтах; смешанный катодно-омический контроль – при грунтовой коррозии металлических конструкций, вследствие работы протяженных макропар (трубопроводы).
В большинстве случаев коррозия подземных сооружений протекает с преимущественным катодным контролем, обусловленным торможением доставки кислорода к поверхности металла.
Критериями опасности коррозии подземных металлических сооружений, согласно ГОСТ 9.602 – 89, являются:
– Коррозионная агрессивность среды по отношению к металлу конструкции;
– Опасные действия постоянного и переменного блуждающих токов.
Скорость коррозии металла в почве зависит от коррозионной активности почвы, то есть от некоторых ее свойств: структуры, пористости, влажности, минерализации грунтовых вод, кислотности, воздухопроводности, удельного электрического сопротивления и температуры среды.
– Влажность почвы. Наличие влаги делает грунт электролитом и вызывает электрохимическую коррозию металлов. Увеличение влажности грунта ускоряет протекание анодного процесса, снижает сопротивление электролита и затрудняет протекание катодного процесса при значительном содержании воды в почве. Максимальная скорость подземной коррозии наблюдается в почвах, содержащих 15—25% влаги. Для каждой почвы существует определенный интервал влажности, соответствующий максимальной скорости коррозии.
— Воздухопроводность грунтов. Пористые грунты могут сохранять влагу в течение длительного времени и создавать благоприятные условия для аэрации (диффузии кислорода). Повышение воздухопроводности грунтов ускоряет коррозионный процесс вследствие облегчения протекания катодного процесса.
— Электропроводность грунтов. Наличие в почве водорастворимых солей способствует увеличению ее электропроводности. Наиболее сильно влияют на коррозионный процесс ионы
,
,
,
,
,
,
и др. Увеличение засоленности грунта, кроме того, облегчает протекание анодного (депассивация анодных участков поверхности) и катодного процессов.
— Кислотность грунта. Она колеблется в широких пределах (рН 3—9). Очень кислые грунты ускоряют коррозию металлов в результате повышения растворимости вторичных продуктов коррозии и возможной дополнительной водородной деполяризации. По величине рН различают кислые (рН 3—5), нейтральные (рН 6—8) и щелочные (рН 9—10) почвы.
— Наличие микроорганизмов. Микроорганизмы, находящиеся в грунтах, могут вызывать значительное местное ускорение коррозии металлов. Наибольшую опасность представляют анаэробные сульфат-редуцирующие бактерии, которые развиваются в илистых, глинистых и болотистых грунтах. Эти бактерии в процессе жизнедеятельности восстанавливают содержащиеся в грунте сульфаты, потребляя образующийся при катодном процессе водород, до сульфид-ионов с выделением кислорода:
Выделяющийся кислород принимает участие в катодной деполяризации коррозионного процесса. Сульфид-ион является депассиватором, а также связывает ионы железа, образуя малозащитные пленки сульфида, и тем самым облегчает анодный процесс.
— Температура грунта. Температура грунта влияет на кинетику электродных процессов и диффузию, определяющие скорость коррозии. Обычно с увеличением температуры наблюдается экспоненциальное возрастание скорости подземной коррозии металла. Различие температур на отдельных участках протяженных подземных сооружений может привести к возникновению термогальванических коррозионных элементов, усиливающих коррозию.
Удельное электрическое сопротивление почвы является функцией всех рассмотренных свойств почвы и представляет один из наиболее характерных показателей коррозионной активности почв по отношению к стали. В определенных границах существует прямая зависимость: чем меньше удельное электрическое сопротивление, тем больше скорость коррозии. Эта зависимость позволяет приближенно оценить коррозионную активность почв.
Согласно ГОСТ 9.602 – 89, коррозионную активность почв по отношению к стали оценивают:
– по удельному электросопротивлению почвы;
– по средней катодной плотности тока при смещении потенциала катода на 100 мВ отрицательнее потенциала коррозии стали.
В табл. 4.2 приведены удельное электрическое сопротивление грунта и величина средней плотности катодного тока, характеризующие коррозионную активность грунтов по отношению к стали.
Удельное электросопротивление грунта, Ом∙м
Средняя плотность катодного тока,
А/м2
Долговечность металлической винтовой сваи с учетом коррозионных процессов в грунте
Скорость коррозии – многофакторный параметр, который зависит как от внешних условий среды, так и от внутренних свойств материала. В нормативно-технической документации существуют определенные ограничения по допустимым значениям разрушения металла при эксплуатации оборудования и строительных конструкций для обеспечения их безаварийной работы. В проектировании не существует универсального метода определения скорости коррозии. Это связано со сложностью учета всех факторов. Наиболее надежным методом является изучение истории эксплуатации объекта.
Методы оценки
Существует несколько способов оценки скорости разрушения металлов в агрессивных средах:
- Лабораторные – испытания образцов в искусственно смоделированных условиях, близких к реальным. Их преимуществом является то, что они позволяют сократить сроки исследования.
- Полевые – проводятся в естественных условиях. Занимают длительное время. Преимуществом такого метода является получение информации о свойствах металла в условиях дальнейшей эксплуатации.
- Натурные – испытания готовых металлических объектов в естественной среде.
Источник
Критерии
Вам будет интересно:Процессы изобарный, изохорный, изотермический и адиабатный для идеального газа
В настоящее время в проектировании техники используют несколько показателей скорости коррозии:
- По прямому способу оценки: уменьшение массы металлической детали на единицу поверхности – весовой показатель (измеряется в граммах на 1 м2 за 1 час); глубина повреждений (или проницаемость коррозионного процесса), мм/год; количество выделяющейся газовой фазы продуктов коррозии; продолжительность времени, в течение которого появляется первое коррозионное повреждение; число центров коррозии на единицу площади поверхности, появившихся за определенный срок.
- По косвенной оценке: сила тока электрохимической коррозии; электрическое сопротивление; изменение физико-механических характеристик.
Канал ДНЕВНИК ПРОГРАММИСТА
Жизнь программиста и интересные обзоры всего. Подпишись, чтобы не пропустить новые видео.
Первый показатель по прямому методу оценки является наиболее распространенным.
Глубинный показатель коррозии
8,76 — коэффициент для перехода от измерения весового показателя скорости коррозии в расчете на 1 ч к глубинному показателю в расчете на 1 год (24 ч • 360=8760 ч);
v — скорость коррозии, г/(м 2 •ч);
В том случае, если коррозия имеет местный характер, скорость ее не может быть точно охарактеризована весовым или глубинным показателем. При питтинговой коррозии необходимо определять максимальный глубинный показатель. При межкристаллитной коррозии и коррозионном растрескивании скорость коррозии количественно характеризуется механическим показателем коррозии, например, по потере прочности:
σ — предел прочности до коррозии;
σ1 — предел прочности после коррозии, рассчитанный по отношению к первоначальной площади сечения металлического образца;
Источник
Расчетные формулы
В общем случае весовые потери, определяющие скорость коррозии металла, находят по следующей формуле:
где q – уменьшение массы металла, г;
S – площадь поверхности, с которой произошел перенос материала, м2;
Для листового проката и изготовленных из него обечаек определяют глубинный показатель (мм/год):
m – глубина проникновения коррозии в металл.
Между первым и вторым показателями, описанными выше, существует следующая зависимость:
где ρ – плотность материала.
Влияние различных факторов на грунтовую коррозию металлов
Грунтовые условия, в которых эксплуатируются металлические сооружения, весьма неодинаковы. Скорость коррозии металлов в грунте в значительной степени зависит от состава грунта, его влагоемкости (т.е. способности удерживать влагу) и воздухопроницаемости и определяется кинетикой электродных процессов, а в случае работы протяженных коррозионных пар также и омическим сопротивлением грунта. Следует отметить следующие основные факторы, определяющие скорость и характер грунтовой коррозии металлов:
Снижение скорости коррозии металла
Вред, причиняемый коррозией, не сводится только к разрушению самих изделий или деталей из металлов. Кроме того, что при ее воздействии приходят в негодность уже изготовленные предметы, пропадают усилия и труд людей, потраченные на производство. Основная причина расходов — это замена или ремонт деталей, вышедших из строя под влиянием этого процесса.
От того, где и как используются изделия, и от нахождения металла в грунте, на воздухе, при создании подводных трубопроводов или судов, различают два вида воздействия этого процесса:
- Химическое. Коррозия, имеющая название «химическая», наблюдается в сухих газах и веществах, не проводящих электричество. Она происходит в доменных печах, при прокате или ковке стали. К веществам при этом процессе относят сероуглероды, керосин, бензин. Химическая коррозия может наблюдаться в двигателях автомобилей и их бензиновых емкостях, нефтехимическом оборудовании, нефтепроводах.
- Электрохимическое. Электрохимическая коррозия сопровождается образованием электрических токов малого напряжения и протекает по принципу гальваники, когда металл и окружающая среда (морская, речная вода, сырая почва, влажная атмосфера, кислоты, основания) служат катодом и анодом.
В случае равномерной коррозии скорость может быть определена по формуле:
v — скорость коррозии, которую обычно выражают в таких единицах: г/(м2•ч) или мг/(см2•сут);
Δm — убыль (увеличение) массы;
Снижение скорости и уменьшение глубины коррозии является главной целью защиты железа и его сплавов от разрушения, вызванного этим процессом. Уменьшение поражения ржавчиной металлических деталей и конструкций достигается несколькими способами:
- изменением факторов природной среды, действующей на металл;
- путем получения антикоррозийных сплавов;
- нанесением слоя покрытия, не подверженного коррозии;
- напылением на поверхность изделия металлов, имеющих более высокую стойкостью к среде, которая вызывает это явление;
- производится защита электрохимическими способами.
Изменение окружающей среды, вызывающей ржавчину, достигается внесением в нее различных ингибиторов коррозии. Этот способ находит все большее применение для снижения коррозии стали.
Сталь — наиболее распространенный вид металлических сплавов, используемых человеком, который производится путем выплавки и смешивания с различными элементами, создающими необходимые качества получаемого материала. За счет этого коррозия стали может снижаться.
Добавляют химические элементы на стадии получения, причем эти добавки не влияют на общие показатели металла. Этим способом получают легированные, нержавеющие стали.
Покрытия, предотвращающие явление ржавления или замедляющие его, называются антикоррозийными.
Слои могут наноситься лакокрасочным и гальваническим способами. Иногда их совмещают, получая покрытие, при котором коррозия стали снижается до минимума, что расширяет область применения материала.
Электрохимическим предохранением от коррозии является то, которое непосредственно влияет на смену потенциала железной детали в зависимости от области использования. Такая реакция проводится, когда заведомо известно место применения изделия. Она может быть анодной или катодной.
Самое неприятное в происходящем явлении, что ржавление (коррозия стали) является причиной разрушения или снижения прочности уже готовых изделий, которые непосредственно влияют на жизнь человека.
К примеру, аварии на различных трубопроводах, осуществляющих подачу газа, нефти; поломки или крушение разводных мостов, металлических конструкций, подъемных кранов.
Основные факторы, влияющие на скорость коррозии
На скорость разрушения металла влияют следующие группы факторов:
- внутренние, связанные с физико-химической природой материала (фазовая структура, химический состав, шероховатость поверхности детали, остаточные и рабочие напряжения в материале и другие);
- внешние (окружающие условия, скорость движения коррозионно-активной среды, температура, состав атмосферы, наличие ингибиторов или стимуляторов и другие);
- механические (развитие коррозионных трещин, разрушение металла под действием циклических нагрузок, кавитационная и фреттинг-коррозия);
- конструктивные особенности (выбор марки металла, наличие зазоров между деталями, требования к шероховатости).
ОПРЕДЕЛЕНИЕ СКОРОСТИ КОРРОЗИИ ПО ДАННЫМ ФАКТИЧЕСКИХ ИЗМЕРЕНИЙ ТОЛЩИНЫ СТЕНОК
2.1. Результаты периодических измерений толщины стенок сосуда или трубопровода служат основанием для определения скорости коррозии металла в условиях эксплуатации.
2.2. Замеры толщины стенок производятся неразрушающими методами контроля или путем засверловки и измерения толщины стенки мерительным инструментом. Предпочтение следует отдавать ультразвуковой толщинометрии.
2.3. Если результаты измерений толщины стенок неразрушающими методами контроля вызывают сомнение, то измерение следует производить сквозной засверловкой.
2.4. На сосудах и трубопроводах, работающих в средах, вызывающих межкристаллитную коррозию или коррозионное растрескивание под напряжением, сквозные засверловки, с последующей их заделкой методами дуговой сварки, не допускаются.
2.5. Место и способ измерения толщины стенок сосуда или трубопровода определяется по результатам их технического освидетельствования службами технического надзора с учетом особенностей коррозионных поражений в различных частях сосудов и трубопроводов.
2.6. Места расположения точек замеров, способ измерения и результаты измерений должны быть оформлены в коррозионной карте на сосуд или трубопровод и храниться в паспорте (см. карты СЗК-2 и СЗК-3).
Источник
Физико-химические свойства
Вам будет интересно:Такие обычные люди, или значение «почему бы и нет»
Наибольшее значение среди внутренних факторов коррозии имеют следующие:
- Термодинамическая устойчивость. Для ее определения в водных растворах применяют справочные диаграммы Пурбе, по оси абсцисс которых откладывается pH среды, а по оси ординат – окислительно-восстановительный потенциал. Сдвиг потенциала в положительную сторону означает большую устойчивость материала. Ориентировочно она определяется как нормальный равновесный потенциал металла. В реальности материалы корродируют с различной скоростью.
- Положение атома в периодической таблице химических элементов. Металлы, наиболее подверженные коррозии, – это щелочные и щелочноземельные. Скорость коррозии снижается при увеличении атомного номера.
- Кристаллическая структура. Она оказывает неоднозначное влияние на разрушение. Крупнозернистая структура сама по себе не приводит к росту коррозии, но благоприятна для развития межкристаллитного избирательного разрушения границ зерна. Металлы и сплавы с однородным распределением фаз корродируют равномерно, а с неоднородным – по очаговому механизму. Взаимное расположение фаз выполняет функцию анода и катода в агрессивной среде.
- Энергетическая неоднородность атомов в кристаллической решетке. Атомы с наибольшей энергией расположены в углах граней микронеровностей и являются активными центрами растворения при химической коррозии. Поэтому тщательная механическая обработка металлических деталей (шлифовка, полировка, доводка) повышает коррозионностойкость. Данный эффект объясняется также формированием более плотных и сплошных оксидных пленок на гладких поверхностях.
Влияние кислотности среды
Вам будет интересно:Шуточные номинации для учителей на выпускной
В процессе химической коррозии концентрация ионов водорода оказывает влияние на следующие моменты:
- растворимость продуктов коррозии;
- формирование защитных оксидных пленок;
- скорость разрушения металла.
При рН в интервале значений 4-10 единиц (кислый раствор) коррозия железа зависит от интенсивности проникновения кислорода к поверхности объекта. В щелочных растворах скорость коррозии сначала уменьшается из-за пассивации поверхности, а затем, при рН>13 увеличивается в результате растворения защитной оксидной пленки.
Для каждого вида металла существует своя зависимость интенсивности разрушения от кислотности раствора. Благородные металлы (Pt, Ag, Au) устойчивы к коррозии в кислой среде. Zn, Al быстро разрушаются как в кислотах, так и в щелочах. Ni и Cd устойчивы к щелочам, но легко корродируют в кислотах.
Результаты коррозии металла. Методы определения скорости коррозии.
По какому бы типу ни протекала коррозия, в результате ее металл разрушается. Прежде всего страдает внешний вид изделия: гладкая отполированная поверхность становится тусклой, затем шероховатой и, наконец, покрывается различными химическими соединениями — продуктами коррозии. Она проникает и в глубь металлических изделий, окончательно разрушая их.
Метод определения потери веса металла. Потери от коррозии.
Для определения величин коррозийной устойчивости разных металлов, используют несколько шкал оценок. Самый распространенный метод оценки по потере веса металла.
Метод заключается в взвешивании детали до того, как она подвергается коррозии, а затем после удаления коррозии с поверхности детали, по разности веса вычисляют потерю металла.
Принято, например, считать металл вполне стойким, если потери в весе вещества не более 0,1 г с 1 м2/ч поверхности. При потере металла от 3 до 10 г · м2/ч металл считают малостойким, при большей потере — нестойким.
Определение скорости коррозии металла.
Иногда коррозионную стойкость определяют по количеству выделившегося водорода, например, при растворении металла в кислотах.
Образец металла, предварительно обработанный соответствующим образом, погружают в раствор электролита, например кислоты, накрывают воронкой, на которую одета бюретка. Бюретку наполняют тем же раствором кислоты. Выделяющийся газ (обычно водород) через воронку попадает в бюретку и вытесняет из нее раствор кислоты.
По количеству выделившегося водорода, а также по скорости его выделения судят о коррозионной стойкости металла.
Этот метод часто используют для определения скорости протекания химического взаимодействия металла с такими кислотами, как серная, соляная, а также иногда для определения характеристики растворения алюминия и цинка в растворах щелочей и кислот.
Результаты коррозии металла.
Однако методы оценки коррозионных разрушений по потере веса или по выделению водорода не всегда дают представление как о характере самого процесса коррозии, так и о возможных ее последствиях.
Шкала грубой оценки коррозионной стойкости металлов
| Группа стойкости | Глубинный показатель коррозии, мм/год | Балл |
| Совершенно стойкие | 0,001 | 1 |
| Весьма стойкие | 0,001 … 0,005 | 2 |
| 0,005 … 0,010 | 3 | |
| Стойкие | 0,01 … 0,05 | 4 |
| 0,05 … 0,10 | 5 | |
| Пониженно стойкие | 0,1 … 0,5 | 6 |
| 0,5 … 1,0 | 7 | |
| Малостойкие | 1,0 … 5,0 | 8 |
| 5,0 … 10,0 | 9 | |
| Нестойкие | 10,0 | 10 |
Состав и концентрация нейтральных растворов
Скорость коррозии в нейтральных растворах зависит в большей степени от свойств соли и ее концентрации:
- При гидролизе солей в коррозионной среде образуются ионы, которые действуют как активаторы или замедлители (ингибиторы) разрушения металла.
- Те соединения, которые увеличивают pH, повышают также скорость деструктивного процесса (например, кальцинированная сода), а те, которые снижают кислотность, – уменьшают ее (хлористый аммоний).
- При наличии хлоридов и сульфатов в растворе разрушение активизируется до достижения некоторой концентрации солей (что объясняется усилением анодного процесса под влиянием ионов хлора и серы), а затем постепенно снижается из-за уменьшения растворимости кислорода.
Некоторые виды солей способны образовывать труднорастворимую пленку (например, фосфорнокислое железо). Это способствует защите металла от дальнейшего разрушения. Данное свойство используется при применении нейтрализаторов ржавчины.
Классификация видов коррозии и способы защиты от нее
Коррозия представляет собой опасный процесс деградации(то есть разрушения) верхнего слоя металлов под влиянием разнообразных сред. Обычно коррозию провоцирует химическая среда, которая окружает металл.
Вне зависимости от вида конструкции и ее работы, самым простым и понятным методом для ведения борьбы с таким явлением, для «защиты от коррозии» используются защитные краски и специальные лаки.
Основные типы коррозии
Говоря о механизме коррозийного процесса можно заметить 2 главных типа коррозии: химическую и электрохимическую.
Химическая — это явственный итог прохождения реакций, во время которых, после уничтожения металлической связи, части металла и все атомы, которые входят в окислители, создают собой крепкую связь.
Электроток между различными частями поверхности металл не может возникнуть. Данная разновидность коррозии может быть присуща химическим средам, которые не в состоянии передавать электроток.
Коррозия винтовых свай. Как продлить срок службы свайно-винтового фундамента?
Для фундамента на винтовых сваях наибольшую опасность представляют два подвида электрохимической коррозии – почвенная и атмосферная.
Почвенная коррозия – разрушение подземных металлических сооружений под действием почвенного электролита. На поверхности металлических изделий, находящихся в контакте с почвенным электролитом, из-за местных неоднородностей металла или электролита возникает большое количество коррозионных элементов.
Однако нельзя забывать, что почвы и грунты чрезвычайно разнообразны и не только в пределах крупных регионов, но и в пределах одного небольшого участка. То есть на сравнительно небольшой площади могут встречаться грунты с разной степенью коррозионной агрессивности: высококоррозионные (тяжелые глинистые, которые на протяжении долгого времени удерживают влагу), среднекоррозионные (суглинки) и практически инертные в коррозионном отношении (супеси, песчаные грунты).
На разницу протекания коррозионных процессов в разных грунтах указывает и Британский стандарт BS 8004 «Фундаменты» (пункт 10.3.5). В соответствии с данным документом остаточная толщина стальных свай, устанавливаемых в ненарушенные почвы, «остается в пределах допустимых значений толщины даже после многих десятилетий эксплуатации», так как скорость коррозии в данных грунтах не превышает 1-2 мм за 100 лет. В то же время в нарушенных почвах «использование окислительно-восстановительного потенциала, удельного сопротивления грунта и значений рН может иметь определенное значение для прогнозирования скоростей коррозии». Однако даже в этом случае толщину металла следует подбирать исходя из степени агрессивности нарушенных почв.
Замедлители коррозии
Замедлители (или ингибиторы) коррозии различаются по механизму действия на окислительно-восстановительный процесс:
- Анодные. Благодаря им образуется пассивная пленка. К данной группе относятся соединения на основе хроматов и бихроматов, нитратов и нитритов. Последний тип ингибиторов применяется для межоперационной защиты деталей. При использовании анодных замедлителей коррозии необходимо предварительно определить их минимальную защитную концентрацию, так как добавление в небольших количествах может привести к увеличению скорости разрушения.
- Катодные. Механизм их действия основан на снижении концентрации кислорода и соответственно, замедлении катодного процесса.
- Экранирующие. Данные ингибиторы изолируют поверхность металла с помощью образования нерастворимых соединений, отлагающихся в виде защитного слоя.
НАЗНАЧЕНИЕ И ОБЩИЕ ПОЛОЖЕНИЯ
1.1. Настоящая инструкция предназначена для определения фактической скорости коррозии металла стенок корпусов сосудов и трубопроводов, эксплуатирующихся на предприятиях Миннефтехимпрома СССР, с целью установления периодичности их технического освидетельствования в соответствии с требованиями действующих правил и нормативных документов.
1.3. В случае невозможности или затруднения применения методов, изложенных в п. 1.2, скорость коррозии определяется приближенно по образцам-свидетелям или оценкой коррозионности среды по отношению к данному металлу с помощью коррозионных зондов.
1.4. Определение скорости коррозии производится по каждому сосуду и трубопроводу технологической установки, линии, цеху. Для группы сосудов или трубопроводов, работающих на данной технологической установке, линии, цехе в одной к той же среде при одинаковых рабочих условиях и материальном исполнении, определение скорости коррозии производится по выбранному объекту-представителю.
1.5. Скорость коррозии металла стенок корпуса сосудов и трубопроводов подлежит уточнению в каждом случае существенного изменения условий их эксплуатации (рабочей среды, температуры, давления), влияющих на коррозионную активность рабочей среды, либо в случае замены материального оформления.
1.6. На каждом предприятии, владельце сосудов, составляется и утверждается главным инженером перечень сосудов с указанием скорости коррозии металла корпуса. Сведения по скорости коррозии трубопроводов заносятся в паспорт трубопровода.
При выявлении специальных видов коррозионных повреждений типа коррозионное растрескивание, межкристаллитная коррозия или расслоение по толщине стенки сведения об этом также заносятся в паспорт сосуда или трубопровода, а вопросы дальнейшей эксплуатации или ремонта сосудов и трубопроводов с такими повреждениями должны быть согласованы со специализированной организацией.
Способы снижения коррозии: механизм и эффективность
Способность окрашенной поверхности противостоять коррозионным процессам зависит от того, какой механизм коррозии преобладает. Например, при постоянном во времени воздействии химически активной среды существенно изменяется разность потенциалов внешней поверхности металлического изделия и его внутренних объемов. При этом возникают коррозионные токи, усиливающие процесс коррозии (явление, часто вызывающее разрушение стальных труб в подземных трубопроводах). Здесь окрашивание не дает никакого эффекта, поскольку химический состав поверхности, покрытой слоем краски, со временем не меняется.
Покрытие металлами
Иное дело, когда поверхность покрыта металлом, имеющим отрицательный электролитический потенциал по отношению к окислительно-восстановительным процессам. При преобладании окислительных реакций сталь эффективнее защитить путем нанесения поверхностного покрытия, содержащего в себе алюминий и цинк, – металлы, которые по своей кислородной активности стоят «левее» железа.
Такие процессы – цинкование и алюминирование – широко применяются в практике антикоррозионной защиты стальных узлов и отдельных деталей, находящихся в окислительной среде. Окрашивание в данных ситуациях носит вспомогательный характер, для повышения декоративных характеристик поверхности.
В восстановительной среде процесс образования гидридов железа может быть эффективно блокирован созданием поверхностных покрытий из металлов, находящихся «правее» водорода: это медь и все благородные металлы. Меднение, хоть и используется на практике, обычно выполняется для относительно небольших по площади поверхностей, поскольку является весьма затратным процессом в плане финансов. Именно для таких ситуаций можно и нужно применять окрашивание.
Окрашивание
Защитная роль красок состоит в том, что в их составе всегда присутствуют ингибиторы коррозии – компоненты, замедляющие во времени скорость протекания процессов окалинообразования. Химические формулы веществ-ингибиторов разработаны таким образом, что в результате приостанавливается появление ржавчины. Эластичность современных окрашивающих составов позволяет покрытиям успешно противостоять также и поверхностным напряжениям, которые провоцируют начало коррозионных процессов.
Антикоррозионные свойства красок увеличиваются, если в их составе находятся кремнийорганические полимеры, которые повышают способность окрашенной поверхности противостоять перепадам влажности и температуры независимо от времени года. Однако такие краски обладают двумя существенными недостатками:
- ядовиты;
- малоэффективны в условиях электролитического механизма коррозии.
Таким образом, правильно подобранные красящие составы могут достаточно эффективно блокировать коррозионные процессы. Для этого они должны содержать в себе ингибиторы коррозии, иметь достаточную эластичность и механическую прочность, незначительно изменяющуюся со временем.
Механическое воздействие
Повышению коррозии в агрессивной среде способствуют такие типы механического воздействия, как:
- Внутренние (при формовании или термообработке) и внешние (под воздействием приложенной извне нагрузки) напряжения. В результате возникает электрохимическая неоднородность, происходит снижение термодинамической устойчивости материала и формируется коррозионное растрескивание. Особенно быстро происходит разрушение при растягивающих нагрузках (трещины образуются в перпендикулярных плоскостях) в присутствии анионов окислителей, например, NaCl. Типичным примером устройств, подверженных такому типу разрушения, являются детали паровых котлов.
- Знакопеременное динамическое воздействие, вибрации (коррозионная усталость). Происходит интенсивное снижение предела усталости, образуются множественные микротрещины, которые затем сливаются в одну крупную. Число циклов до разрушения в большей степени зависит от химического и фазового состава металлов и сплавов. Такой коррозии подвержены оси насосов, рессоры, лопатки турбин и другие элементы оборудования.
- Трение деталей. Быстрое корродирование обусловлено механическим износом защитных пленок на поверхности детали и химическим взаимодействием со средой. В жидкости скорость разрушения ниже, чем на воздухе.
- Кавитационное ударное воздействие. Кавитация возникает при нарушении сплошности потока жидкости в результате образования вакуумных пузырей, которые схлопываются и создают пульсирующее воздействие. В результате возникают глубокие повреждения локального характера. Данный тип коррозии часто наблюдается в химических аппаратах.
Практика коррозионных испытаний металлов
Индикаторами коррозии являются климатические факторы – температура, состав и относительная влажность окружающей среды, характер распределения внешних нагрузок. Во внимание необходимо принимать также изменение освещенности по времени суток, количество осадков, возможное загрязнение воздуха. Например, в зонах выбросов дымовых отходов вблизи химических комбинатов и металлургических производств, сопровождающихся резким увеличением процентного содержания SO2, коррозионные процессы резко активизируются.
В качестве индикаторов коррозионной активности можно использовать количественные зависимости коррозии от времени:
- Линейные – чаще всего это характерно для металлических поверхностей, не имеющих защитного покрытия.
- Экспоненциально убывающие – встречаются при кислотной коррозии обычных металлов и сплавов.
- Экспоненциально возрастающие – когда на поверхности детали имеется защитное покрытие.
Интенсивность образования ржавчины при таких условиях снижают:
- малая скорость ветра;
- пониженная цикличность во времени изменения показателей относительной влажности;
- характер воздействия коррозионно-активной среды на поверхность.
При слабом ветре или его отсутствии нет условий для перемешивания потока, омывающего контактную поверхность стали. При длительных фазах пониженной и повышенной влажности в течение года пленка поверхностной ржавчины успевает сформироваться, набухнуть и отделиться от основного металла. Толщина поверхности снизится, зато коррозионные процессы вынуждены «запуститься» сначала, а для этого требуется не только время, но и подходящие условия – ветер или изменения в химическом составе воздуха, что бывает далеко не всегда.
Влага, кислота или щелочь могут попадать на поверхность стали в виде капель либо струйным путем. Первый способ характерен для зон с повышенным количеством осадков, а второй – для неблагоприятной окружающей среды, в которой функционирует деталь или металлическая конструкция.
Конструктивные факторы
Вам будет интересно:Копать или капать? Как правильно написать?
При конструировании элементов, работающих в агрессивных условиях, необходимо учитывать, что скорость коррозии возрастает в следующих случаях:
- при контакте разнородных металлов (чем больше разница электродного потенциала между ними, тем выше сила тока электрохимического процесса разрушения);
- при наличии концентраторов механических напряжений (канавки, пазы, отверстия и другие);
- при низкой чистоте обработанной поверхности, так как при этом возникают локальные короткозамкнутые гальванические пары;
- при значительной разнице температуры отдельных частей аппарата (образуются термогальванические элементы);
- при наличии застойных зон (щели, зазоры);
- при формировании остаточных напряжений, особенно в сварных соединениях (для их устранения необходимо предусмотреть термическую обработку – отжиг).