18.02.2022 Автор: VT-METALL
Из этого материала вы узнаете
:
- История открытия сплавов железа с углеродом
- Структурные составляющие сплавов железо-углерод
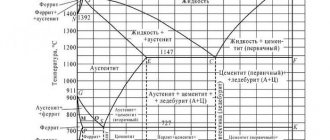
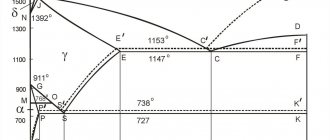
- Диаграмма сплава железо-углерод
- Как читать диаграмму сплава железа с углеродом
- Применение стали из железоуглеродистых сплавов
- Разновидности чугуна из сплава железа с углеродом
- Полиморфные превращения в сплавах железо-углерод
Открытие сплава железа с углеродом явилось одним из самых важных событий в истории развития металлургии. Именно эти два элемента подарили миру наиболее востребованные марки стали и чугуна. Это те сплавы, из которых производится большая часть промышленного оборудования, металлических конструкций, инструмента, изделий бытового назначения.
В зависимости от процентного содержания углерода в железе, а также способа литья эти сплавы приобретают разные свойства: стойкость к коррозии, необычайную прочность, эластичность и т. д. О том, какие сплавы железа и углерода используются сегодня и как их получают, вы узнаете из нашего материала.
История открытия
Впервые на то, что в сплавах (сталях и чугунах) есть определенные (особые) точки, указал великий металлург и изобретатель — Дмитрий Константинович Чернов (1868 год). Именно он сделал важное открытие о полиморфных превращениях и является одним из создателей диаграммы состояния железо-углерод. По мнению Чернова, положение этих точек на диаграмме имеет прямую зависимость от процентного содержания углерода.
И что самое интересное, именно с момента этого открытия и начинает свою жизнь такая наука, как металлография.
Диаграмма сплавов железа с углеродом является результатом кропотливого труда ученных нескольких стран мира. Все буквенные обозначения главных точек и фаз в диаграмме являются интернациональными.
Описание
Концентрация углерода в цементите — 6,67% по массе — предельная для железоуглеродистых сплавов. Цементит — метастабильная фаза; образование стабильной фазы — графита во многих случаях затруднено. Цементит имеет орторомбическую кристаллическую решётку, очень твёрд и хрупок, слабо магнитен до 210 °C.
В зависимости от условий кристаллизации и последующей обработки цементит может иметь различную форму — равноосных зёрен, сетки по границам зёрен, пластин, а также видманштеттову структуру.
Цементит в разных количествах, в зависимости от концентрации, присутствует в железоуглеродистых сплавах уже при малых содержаниях углерода. Формируется в процессе кристаллизации из расплава чугуна. В сталях выделяется при охлаждении аустенита или при нагреве мартенсита. Цементит является фазовой и структурной составляющей железоуглеродистых сплавов, составной частью ледебурита, перлита, сорбита и троостита. Цементит — представитель так называемых фаз внедрения, соединений переходных металлов с лёгкими металлоидами. В фазах внедрения велики доля как ковалентной, так и металлической связи.
Твёрдость по Бринеллю больше 800 кг/мм2. Первичный цементит кристаллизуется из жидкого сплава Вторичный цементит — из аустенита Третичный цементит — из феррита
Это интересно: Цементация стали в домашних условиях графитом и другими методами — разбираем досконально
Структуры на диаграмме железо-углерод
Напомним о 2 кристаллических формах железа:
- α-железо. Имеет объемноцентрированную кубическую (ОЦК) решетку;
- γ-желез. Имеет гранецентрированную кубическую (ГЦК) решетку.
Кристаллическая решетка железа Полиморфное превращение одной формы в другую при проведении термообработки сталей происходит при прохождении сплавами линии GSK.
Выделим 4 фазы в системе железо-углерод:
- Жидкая фаза. Концентрация углерода не ограничена;
- Феррит – это твёрдый раствор углерода в α-железе. Максимальная концентрация углерода – всего лишь 0,025% (точка P). При комнатной температуре – не выше 0,006%. Феррит мягок и пластичен.
- Аустенит – твёрдый раствор углерода в γ-железе. Максимальная концентрация углерода — 2,14 % (точка E). Аустенит имеет невысокую твёрдость, пластичен, не магнитится.
- Цементит — химическое соединение железа с углеродом (карбид железа, Fe3C). Концентрация углерода, соответственно, постоянная – 6,67 % углерода. Цементит очень твёрд, хрупок, непластичен.
В зависимости от условий образования выделяют:
- первичный цементит (образуется из жидкости);
- вторичный цементит (выделяется из аустенита вокруг его зерен);
- третичный цементит (выделяется из феррита по границам его зерен);
- эвтектоидный цементит (является составной частью перлита);
- эвтектический цементит (является составной частью ледебурита).
Необходимо так же выделить 2 структурные составляющие железоуглеродистых сплавов:
- Перлит (эвтектоид) – механическая смесь 2 фаз – пластинок/зерен феррита и цементита. Перлит образуется в результате перлитного превращения аустенита («свободного» или входящего в состав ледебурита) с концентрацией углерода 0,8% при прохождении ниже линии PSK:
А0,8→Ф0,025 + Ц6,67
Структура перлита. Ф — феррит, Ц — цементит
Железо при этом переходит из γ-формы в α-форму. Механические свойства сильно зависят от размера (дисперсности) частичек, из которых состоит данный перлит.
- Ледебурит (эвтектика) – механическая смесь 2 фаз – пластинок/зерен аустенита и цементита. Ледебурит образуется из жидкой фазы с концентрацией углерода 4,3% при прохождении ниже линии ECF:
Ж4,3→А2,14 + Ц6,67
Структура ледебурита. Ц — цементит, А — аустенит.
Повторяясь, напомним, что при прохождении сплавов ниже линии PSK (727°С) аустенит, входящий в состав ледебурита, претерпевает перлитное превращение, разделяясь на феррит и цементит. Ледебурит тверд и хрупок.
При комнатной температуре железоуглеродистые сплавы могут иметь различную структуру, а значит и свойства, хотя и состоят всегда всего из 2 фаз: феррита и цементита.
Цементит: формы существования
Так называют соединение углерода и железа. Это компонент чугуна и некоторых сталей. В него входит 6,67% углерода.
В его кристалл входит несколько октаэдров, они расположены друг по отношению к другу с некоторым углом. Внутри каждого из них расположен атом углерода. В результате такого построения получается следующая картина – один атом вступает в связь с несколькими атомами железа, а железо в свою очередь связано с тремя атомами этого элемента.
Кристаллическая решетка цементита
У этого вещества имеются все свойства, которые присущи металлам – электропроводность, своеобразным блеском, высокая теплопроводность. То есть, смесь железа и углерода, ведет себя как металл. Этот материал обладает определенной хрупкостью. Большая часть его свойств определена сложным строением кристаллической решетки.
Этот материал плавится при 1600 градусах Цельсия. Но на этот счет существует несколько мнений, одни исследователи считают, что его температура плавления лежит в диапазоне от 1200 до 1450, другие определяют, что верхний уровень равен 1300 °С.
Первичный цементит
Металлурги разделяют три типа этого вещества – первичный, вторичный, третичный.
Диаграмма железо-цементит
Первичный, получается из жидкости при закалке сплавов, которые содержат в себе 5,5% углерода. Первичный имеет форму в виде крупных пластин.
Вторичный
Этот элемент получается из аустенита при охлаждении последнего. На диаграмме этот процесс этот процесс можно видеть по диаграмме Fe – C. Цементит представлен в виде сетки, размещенной по границам зерен.
Третичный
Этот тип, является производным от феррита. Он имеет форму иголок.
В металлургии существуют и другие формы цементита, например, цементит Стеда и пр.
Другие структурные составляющие в системе железо углерод
Перлит
Перлит – это механическая смесь, которая состоит из феррита и цементита. Ледебурит представляет собой переменный раствор.
Перлит
При температуре от 1130 и до 723 °С в его состав входят аустенит и цементит. При более низких температурах он состоит из аустенит заменяет феррит.
Некоторые элементы диаграммы железо-углерод
Выделим несколько границ на диаграмме железо-углерод:
- линия ACD. Линия ликвидус. При охлаждении сплавов ниже нее начинается их кристаллизация;
- линия AECF. Линия солидус. При охлаждении сплавов ниже нее весь сплав переходит в твердое состояние;
- линия ECF. Иногда называется линией ледебуритного превращения. При охлаждении сплавов с содержанием углерода выше 2,14% ниже нее жидкая фаза превращается в ледебурит;
- линия PSK. Линия перлитного превращения. При охлаждении сплавов ниже нее аустенит превращается в перлит.
Отметим несколько важных точек на диаграмме:
- точка E. Точка максимального насыщения аустенита углеродом – 2,14%, при температуре 1147°С;
- точка P. Точка максимального насыщения феррита углеродом – 0,025%, при температуре 727°С;
- точка S. Точка «0,8% С-727°С» превращения аустенита с концентрацией углерода 0,8% в перлит (эвтектоид) той же средней концентрации;
- точка C. Точка «2,14 % С-1147°С» превращения жидкости с концентрацией углерода 2,14% в ледебурит (эвтектику) той же средней концентрации.
Часто значения температур, при которых происходят структурные изменения конкретного сплава обозначают буквами A:
- A1 – линия PSK;
- A2 – линия MO – точка Кюри, в которой происходит изменение магнитных свойств сплавов;
- A3 – температуры, соответствующие линии GS;
- Acm – температуры, соответствующие линии SE.
Поскольку температуры фазовых переходов при нагреве и охлаждении слегка отличаются, то часто вводят дополнительные буквенные обозначения:
- с – для температур фазовых переходов при нагреве;
- r – при охлаждении,
например, Ac1 или Ar1.
Значение линий диаграммы
Границы, пересекающиеся друг с другом, отмечают определенные области на диаграмме. Внутри каждой зоны может существовать отдельная фаза или две фазы. На границе происходит фазовый переход. Эти области являются фазовыми полями, они указывают фазы, присутствующие для определенного состава и температуры сплава.
На диаграмме имеется несколько характерных линий, обозначаемых как A1, A2, A3, A4 и ACM. При повышении или понижении температуры металла на этих границах происходит фазовый переход. Обычно при нагревании сплава его температура повышается, но вдоль этих линий нагрев приводит к перестройке структуры в другую фазу, и, таким образом, температура перестаёт расти до тех пор, пока фаза полностью не изменится. Этот процесс называется термической остановкой.
Элементы легированной стали — никель, марганец, хром, и молибден — влияют на положение этих границ на фазовой диаграмме. Границы могут сдвигаться в любом направлении в зависимости от используемого элемента. Например, на диаграмме состояния железа и углерода добавление никеля понижает границу A3, а добавление хрома увеличивает её.
Применение диаграммы состояния железоуглеродистых сплавов
Диаграмму состояния сплавов системы железо—цементит применяют для определения режима термической обработки сплава, температуры нагрева металла под ковку и температурного предела ковки, а также температуры плавления, что необходимо для назначения режима заливки жидкого сплава в формы.
Термическая обработка производится путем нагрева металлических сплавов до определенных температур, выдержки при этих температурах и последующего быстрого или медленного охлаждения с целью изменения свойств сплава в желаемом направлении.
Термическая обработка железоуглеродистых сплавов имеет ряд разновидностей, основанных на том, что неустойчивая при низких температурах структура аустенита в зависимости от скорости охлаждения сплава превращается в структуры, обладающие различными свойствами. Продуктами распада аустенита являются мартенсит, троостит, сорбит и перлит.
Мартенсит — продукт закалки аустенита и его превращения в феррит без выделения углерода из раствора. Поэтому мартенсит — это сильно пересыщенное углеродом α-железо с кпженной кристаллической решеткой. Эго обусловливает высокую его твердость (НВ 600—700) и прочность, повышенную и ость и наличие внутренних напряжений. Эта структура образуется при больших скоростях охлаждения — закалки (180 ÷ сек для углеродистой стали). Мартенсит по своей природе неустойчив и при нагреве до температуры свыше 70° стремится перейти в другие структуры.
Трооститом называется механическая смесь феррита цементита очень высокой степени дисперсности. Твердость троостита НВ 350÷500. Эта структура образуется при скорости закалки углеродистой стали около 80°/сек. Игольчатый троостит иногда называют бейнитом.
Сорбит — это более грубая механическая смесь зерен феррита и цементита, однако достаточно дисперсная. Она с трудом различается под обычным микроскопом. Твердость сорбита 250÷350. Эта структура образуется при скоростях закалки углеродистой стали менее 50°/сек. По сравнению с трооститом copбит имеет более высокую вязкость, а по сравнению с перлитом — большую твердость.
Перлит представляет собой более или менее грубую механическую смесь феррита и цементита. Перлит образуется при малых Скоростях охлаждения стали, нагретой до аустенитного состояния.
Троостит, сорбит и перлит можно получить путем отпуска мартенсита при возрастающих температурах отпуска. В этом случае они имеют отличные, часто более высокие механические свойства, чем при охлаждении аустенита с разными скоростями.
Таким образом, путем изменения режима термической обработки можно получать различные физико-механические свойства и структуры стали. К операциям термической обработки относятся отжиг, нормализация, закалка и отпуск.
Отжиг — фазовая перекристаллизация — заключается в нагреве доэвтектоидной стали выше линии А3, а заэвтектоидной — выше линии Аст с последующим медленным охлаждением вместе с печью. Если нагреть сталь выше А1, но ниже, А3 (или Аст), то полной перекристаллизации не произойдет. Tal кая термическая обработка называется неполным отжигом. При отжиге состояние стали приближается к равновесному. Поэтому структура отожженной стали состоит либо из феррита и перлита (доэвтектоидные стали), либо из перлита и вторичного цементита (заэвтектоидные стали).
Температурные пределы полного отжига, неполного отжига, высокого отпуска и нормализации, нанесенные на участке диаграммы состояния железо — цементит
Отжиг снижает твердость и повышает вязкость стали, улучшает ее обрабатываемость, снимает внутренние напряжения, а также устраняет структурную неоднородность и стабилизирует физические свойства.
Нормализация отличается от отжига повышенной скоростью охлаждения (на спокойном или движущемся воздухе). Нормализацию применяют для размельчения зерна металла и повышения его прочности.
Закалкой называется нагрев стали выше критической точки А3 (рис. 9) с последующим быстрым охлаждением в воде, масле или других охлаждающих средах. Обычно цель закалки — получение мартенситной структуры, подвергаемой затем отпуску. Неполная закалка происходит в случае, если доэвтектоидная сталь была нагрета до температуры, лежащей выше точки Аи но ниже точки А3. Феррит, содержащийся в такой стали наряду с аустенитом, закалки естественно не принимает. Заэвтектоидные стали закаливают с температур выше А1, но ниже Асm, так как нецелеобразно растворять при нагреве твердые включения вторичного цементита.
Температурные пределы ковки и горячей штамповки, нанесенные на участке диаграммы состояния железо — цементит.
При отпуске сталь нагревают до температуры ниже А1, выдерживают при этой температуре и медленно охлаждают вместе с печью. Низкий отпуск (175—250°) служит для повышения язкости стали при сохранении высокого предела прочности и твердости, уменьшения внутренних напряжений и получения более устойчивых структур. Высокий отпуск (до 700°) применяют для повышения пластичности и обрабатываемости стали и снижена прочности и твердости.
Ковку, горячую штамповку и прокатку стали производят при сравнительно высоких температурах. Нагрев стали производят до температуры на 100—150° ниже линии солидуса.
Окончание обработки стали давлением должно происходить и температурах, близких к А3, для доэвтектоидной стали, мшчание процесса при слишком низких температурах ведет к рочечности структуры стали, к снижению ее пластичности, копчание процесса при слишком высоких температурах ведет росту зерна стали (перегрев) и повышению ее хрупкости. Перерой можно исправить термической обработкой (отжигом, нормализацией).
При нагреве стали до температуры, близкой к линии солидуса АЕ, происходит окисление металла вдоль границ зерен, рпультате чего связь между последними нарушается и механическая прочность катастрофически падает. Такое явление называют пережогом, причем его нельзя исправить какой-либо следующей термической обработкой.
Разновидности сталей с доборной обработкой
Жаростойкие стали предназначаются для работы в хим и газовых средах при высочайшей температуре и слабонагруженном состоянии. Маркируются они аналогично нержавейки, но в отличие от нее проходят специальную закалку, чтоб получить нужные характеристики. Жаропрочная сталь употребляется в работе с неизменными высочайшими температурами. Она способна долгое время выдерживать эксплуатацию при 1700 градусов по Цельсию. Типы данной стали совпадают с 2-мя прошлыми видами, а маркируется с помощью буквенно-циферных обозначений, которые демонстрируют уровень разных примесей в сплаве и очень допустимые рабочие температуры. Все перечисленные разновидности употребляются и для маркировки листовой стали.
Интересно почитать: Производство стали в кислородных конвертерах
Свою маркировку имеют и виды стали, которые подверглись доборной обработке уже опосля выплавки. Покрытыя цинком сталь покрывается слоем цинка, который защищает от появления коррозии. Данный тип интенсивно употребляется в автопромышленность уже много лет. Его наиболее широкому распространению мешает относительная накладность производства.
Марки покрытой цинком стали обозначаются буквенной аббревиатурой, которая охарактеризовывает предназначение материала, его способность к вытяжке и равномерность покрытого цинком покрытия. Эти характеристики определяют возможность внедрения оцинковки на том либо ином производстве. Их не настолько не мало, потому можно просто выучить все сокращения и без заморочек ориентироваться по мере необходимости покупки.
Швеллер представляет собой сортовой прокат с П-образным сечением. Он употребляется для производства различных сборных и сварных конструкций на строй объектах. Маркировка швеллера соответствует марки стали, из которой он был сделан. Он предназначен для работы под действием высочайшей перегрузки, потому для производства употребляют самые твердые сорта. Остальные материалы, сделанные на металлической базе, также часто сохраняют ее марку или не имеют такой совершенно. Познание черт марок стали поможет создать верный выбор при покупке продукции для непосредственно поставленной цели.
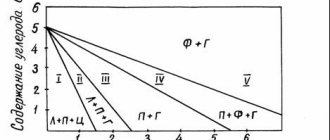
Классификация железоуглеродистых сплавов
Различные комбинации этих элементов приводят к получению большого количества сплавов, которые можно разделить на три большие группы:
- Техническое железо.
- Стали.
- Чугуны.
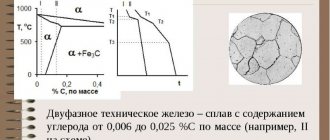
Техническое железо
К техническому железу относят материалы, в которых содержится менее 0,02% углерода. К сталям относят, материалы, в которых углерод находится в пределах от 0,02 до 2,14%. И в группу чугунов входят материалы, количество углерода в которых превышает 2,14%.
Применение стали и чугуна в быту
Сталь, как материал, так тесновато вошла в нашу жизнь, что мы даже не подозреваем этого. Человек уже много веков пользуется металлическими изделиями в быту. Раз в день любой из нас сталкивается с разными видами металлов и сплавов, почти все из которых находятся у нас дома либо на придомовой местности.
Фазы диаграммы железо-углерод
В системе железо — углерод существуют следующие фазы: жидкая фаза, феррит, аустенит, цементит, графит.
Жидкая фаза. В жидком состоянии железо хорошо растворяет углерод в любых пропорциях[источник не указан 1441 день] с образованием однородной жидкой фазы.
Феррит — твёрдый раствор внедрения углерода в α-железе с объёмно-центрированной кубической решёткой.
Феррит имеет переменную, зависящую от температуры предельную растворимость углерода: минимальную — 0,006 % при комнатной температуре (точка Q), максимальную — 0,02 % при температуре 700 °C (точка P). Атомы углерода располагаются в центре грани или (что кристаллогеометрические эквивалентно) на середине рёбер куба, а также в дефектах решетки.
При температуре выше 1392 °C существует высокотемпературный феррит с предельной растворимостью углерода около 0,1 % при температуре около 1500 °C (точка H).
Свойства феррита близки к свойствам чистого железа. Он мягок (твёрдость по Бринеллю — 130 НВ) и пластичен, ферромагнитен (при отсутствии углерода) до точки Кюри — 770 °C.
Аустенит (γ) — твёрдый раствор внедрения углерода в γ-железе с гранецентрированной кубической решёткой.
Атомы углерода занимают место в центре гранецентрированной кубической ячейки. Предельная растворимость углерода в аустените — 2,14 % при температуре 1147 °C (точка Е). Аустенит имеет твёрдость 200—250 НВ, пластичен, парамагнитен. При растворении других элементов в аустените или в феррите изменяются свойства и температурные границы их существования [3] .
Цементит (Fe3C) — химическое соединение железа с углеродом (карбид железа), со сложной ромбической решёткой, содержит 6,67 % углерода. Он твёрдый (свыше 1000 HВ), и очень хрупкий. Цементит — метастабильная фаза и при длительном нагреве самопроизвольно разлагается с выделением графита.
В железоуглеродистых сплавах цементит как фаза может выделяться при различных условиях:
- цементит первичный (выделяется из жидкости),
- цементит вторичный (выделяется из аустенита),
- цементит третичный (из феррита),
- цементит эвтектический и
- эвтектоидный цементит.
Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зёрен аустенита (после эвтектоидного превращения они станут зёрнами перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зёрен [4] .
Эвтектический цементит наблюдается лишь в белых чугунах. Эвтектоидный цементит имеет пластинчатую форму и является составной частью перлита. Цементит может при специальном сфероидизируюшем отжиге или закалке с высоким отпуском выделяться в виде мелких сфер. Влияние на механические свойства сплавов оказывает форма, размер, количество и расположение включений цементита, что позволяет на практике для каждого конкретного применения сплава добиваться оптимального сочетания твёрдости, прочности, стойкости к хрупкому разрушению и т. п. [5]
Графит — фаза состоящая только из углерода со слоистой гексагональной решёткой. Плотность графита (2,3 г/см3) намного меньше плотности всех остальных фаз (около 7,5—7,8 г/см3) и это затрудняет и замедляет его образование, что и приводит к выделению цементита при более быстром охлаждении. Образование графита уменьшает усадку при кристаллизации, графит выполняет роль смазки при трении, уменьшая износ, способствует рассеянию энергии вибраций.
Графит имеет форму крупных крабовидных (изогнутых пластинчатых) включений (обычный серый чугун) или сфер (высокопрочный чугун).
Графит обязательно присутствует в серых чугунах и их разновидности — высокопрочных чугунах. Графит присутствует также и в некоторых марках стали — в так называемых графитизированных сталях.
Применение стали в быту
Разная сталь применяется при производстве посуды и утвари для кухни: темный металлической прокат, эмалированная сталь, нержавеющая сталь, сталь листовая покрытыя цинком. К бытовым кухонным железным принадлежностям относятся все виды устройств, которые употребляются на разных шагах изготовления еды: кухонная мясорубка, устройство с помощью которого шинкуют овощи, бытовые кухонные весы, подвесная либо настольная сушилка для тарелок и вилок, ложек и т.д.
Посуда для кухни
Кухонное оборудование: духовки, микроволновки, посудомоечные машинки, пароварки и пр. – все имеют корпус почти всегда из листа холоднокатаного.
На кухне используются хозяйственные ножики различного предназначения: хлебный ножик, ножик для разделывания мяса, ножик для вырезки сыра и масла, ножик для очистки фруктов и овощей и различные модели раскладных ножей.
К столовым кухонным устройствам относим различные виды ложек и вилок. Ложки разделяются по размеру и предназначению: столовые, десертные, чайные и кофейные ложки. Вилки делятся на два вида: столовые и буфетные. Также употребляются в быту столовые кухонные наборы, куда входят ножики, вилки и ложки.
Посреди хозяйственных ножниц существует некоторое количество видов: кухонные, портновские, ножницы для маникюра, ножницы, применяемые в парикмахерских и т.д.
Металлоизделия и инструменты, которые употребляются для ремонта и строительства
- разные изделия для крепежа: гайки, гвозди, болты, шурупы и т.д;
- фурнитура для окон и дверей: ручки, петли, замки, шпингалеты и т.д;
- железные инструменты, которые употребляются для обработки дерева: пилы, топоры и т.д;
- строй инструменты для обработки железных частей: зубила, зажимные тиски, кувалды, молотки, наковальни, ножовки, ратфили, сверлильные инструменты и устройства для нарезания резьбы;
- инструменты, нужные для монтажа: плоскогубцы, отвертки, кусачки, клещи;
- строительное оборудование, которое содержит элементы из стали: дрель, перфоратор, шуруповерт и т.д.;
- садовый инвентарь: лопаты, грабли, вилы, косы, мотыги, серпы и т.д.
Садовый металлической инвентарь
Нагревательные и осветительные приборы
- газовые кухонные плиты;
- водонагреватели для дома;
- котлы электронные для помещений;
- отопительные котлы, которые работают на жестком и водянистом горючем;
- керосиновые лампы и уличные фонари.
Дымоходы
В устройстве дымоходов применяется труба профильная, в тч из специальной жаростойкой стали, которая имеет устойчивость к высокотемпературной коррозии.
Мебель
Разная железная фурнитура употребляется в мебельных системах. Главным элементом фурнитуры является маленькая труба профильная железная, уголок железный и полоса железная. Нередко употребляется железный декор в мебели.
Чтение диаграммы железо-углерод
Состав сплава с данным исходным содержанием углерода при заданной температуре мы можем увидеть, двигаясь по вертикальной линии, соответствующей содержанию углерода в сплаве.
Рассмотрим, например, область AEC. С ней соседствуют области аустенита AESG и жидкой фазы. Сплавы в ней состоят из жидкой фазы и образующегося твердого аустенита. Как определить концентрацию углерода в разных фазах для данного сплава? Рассмотрим для примера сплав с исходной концентрацией углерода 2,5% при температуре 1250°С.
Проведем из этой точки графика «2,5% C – 1250°С» горизонтальную прямую. Пересечение этой прямой с линией AE, граничащей с областью аустенита, покажет концентрацию углерода в аустените при данной температуре (~1.5%).
Пересечение этой же горизонтальной прямой с линией AС, граничащей с областью жидкой фазы, покажет концентрацию углерода в жидкой фазе при данной температуре (~3.5%).
Именно таким образом мы можем определить концентрацию углерода в фазах любого сплава при заданной температуре:
- в жидкой фазе и аустените в области AEC;
- в жидкой фазе в области CDF (концентрация углерода в цементите, конечно, постоянна – 6,67%);
- в аустените в области SEFK;
- в феррите в области QPKL;
- в феррите и аустените в области GPS.
Как видим, при концентрации углерода выше 2,14% насыщение охлаждаемого расплава углеродом всегда стремится к 4,3% (по линиям AC и DC) по мере приближения к температуре 1147°С (уровень ECF). Далее происходит превращение жидкости в ледебурит (эвтектику). Естественно, с этим же средним содержанием углерода.
По мере приближения к температуре 727°С (уровень PSK) концентрация углерода в аустените («свободном» и/или входящем в состав ледебурита) стремится к 0,8% (по линиям GS и ES). Далее происходит превращение аустенита в перлит (эвтектоид). Перлит, конечно, имеет среднее содержанием углерода 0,8%.
Марки нержавеющей стали
Всего же выделяют 5 видов нержавейки. Аустенитные стали характеризуются высочайшим содержанием хрома (20-25%) и никеля (18%). Они отлично противостоят коррозии даже в критериях завышенных температур. Ферритные стали различаются наличием магнитных параметров и низким содержанием углерода. Хром занимает около 17% в сплаве, а никель отсутствует или его толика составляет наименее 0,1%.
Дуплексные стали являются смешанным видом, владеющим качествами 2-ух прошлых марок. Мартенситные стали содержать всего 12% хрома и довольно высочайший уровень углерода. Этот вид употребляется для производства столовых устройств и хирургических инструментов. Упрочненные стали имеют в составе доп сплавы (титан, ниобий и остальные), повышающие крепкость сплава. Их используют в критериях, когда эксплуатируемый материал будет находиться под действием физической перегрузки, к примеру в элементах шахтной укрепляй.
Свойства технически чистого железа
Магнитные свойства железа при различных температурах:
- менее 768° С – ферромагнитно;
- более 768° С – парамагнитно.
А температурную точку 768° С называют точкой магнитного превращения, или точкой Кюри.
Свойства технически чистого железа:
- твердость – 80 НВ;
- временное сопротивление — 250 МПа;
- предел текучести – 120 МПа;
- относительное удлинение 50 %;
- относительное сужение – 80 %;
- высокий модуль упругости.
Аустенит в сталях
Наличие аустенита в стальных сплавах придает им определенные свойства. Детали и узлы, произведенные из подобных сталей, предназначаются для работы в средах, содержащие агрессивные компоненты, например, на предприятиях, перерабатывающих разные кислоты.
Стали этого класса отличаются высоким уровнем легирования, во время кристаллизации формируется гранецентрированная решетка. Такая структура не подвержена изменению даже под воздействием глубокого холода.
Стали этого типа можно разделить на два типа отличающиеся друг от друга составом. В первых, содержатся такие вещества как железо, никель, хром. При этом общее количество добавок не может превышать 55%. Ко второй группе относят никелевые и железоникелевые композиции. В никелевых композициях, его содержание превышает 55%. В железоникелевых составах соотношение никеля и железа составляет 1:5, а количество никеля начинается от 65%.
Такое количество никеля обеспечивает повышенную пластичность, а хром, в свою очередь обеспечивает высокую коррозионную стойкость и жаропрочность. Применение других легирующих материалов позволяет выплавлять сплавы с уникальными эксплуатационными свойствами. Металлурги, составляя рецептуру сплавов, руководствуются будущим назначением сталей.
Для получения легированный сталей применяют ферритизаторы, которые придают постоянство аустенитам, к таким веществам относят ниобий, кремний и некоторые другие. Кроме них применяют углерод, марганец – их называют аустенизаторами.
Компоненты в системе железо углерод
Аустенит
Атомы размещается в гранецентрированной ячейке. Твердость аустенита имеет твердость 200 … 250 единиц по Бринеллю. Кроме того у него хорошая пластичность и он отличается парамагнитностью.
Железо
Железо – это материал, относящийся к металлам. Его натуральный цвет – серебристо-серый. В чистом виде он очень пластичен. Его удельный вес составляет 7,86 г/куб. см. Температура плавления составляет 1539 °C. На практике чаще всего применяют техническое железо, в составе которого присутствуют следующие примеси – марганец, кремний и многие другие. Массовая доля примесей не превышает 0,1%.
Железо
У железа есть такое свойство как полиформизм. То есть, при одном и том же химическом составе, это вещество может иметь разную структуру кристаллической решетки и соответственно разные свойства. Модификации железа называют соответственно – Б, Г, Д. Все эти модификации существуют при разных условиях. Например, тип Б, может существовать только при температуре 911 °С. Тип Г может существовать в диапазоне от 911 до 1392 °С. Тип Д существует в диапазоне от 1392 до 1539 °С.
Каждый из типов обладает своей формой кристаллической решеткой, например, у типа Б решетка представляет собой куб, решетка типа Г имеет гранецентрированную кубическую форму. Решетка типа Д, имеет форму объемно центрированного куба.
Еще одно свойство состоит в том, что при температуре ниже 768 железо ферримагнитно, а при ее повышении это свойство теряется.
Точки полиморфной и магнитной трансформации называют критическими. На таблице они обозначены следующим образом – А2, А3, А4. Цифровые индексы показывают тип трансформации. Для более полного различия превращения железа из одного вида в другой к обозначению добавляют индексы с и r. Первый говорит о нагреве, второй об охлаждении.
Полиморфные модификации железа
При высоких параметрах пластичности, железо не обладает высокой твердостью, по шкале Бринелля она равна 80 единиц.
Железо имеет возможность образовывать твердые растворы. Их можно разделить на две группы – раствор замещения и внедрения. Первые состоят их железа и других металлов, вторые из железа и углерода, водорода и азота.
Углерод
Другой компонент системы – углерод. Это – неметалл и он обладает тремя модификациями в виде алмаза, графита и угля. Он плавится при 3500 °С.
Аллотропные модификации углерода
В сплаве железа, этот элемент находится в виде твердого раствора, его называют цементит или в виде графита. В таком виде он присутствует в сером чугуне. Графит, не отличается ни пластичностью, ни прочностью.
Цементит
Цементит (Fe3C) – химическое соединение железа с углеродом (карбид железа), содержит 6,67 % углерода. Более точные исследования показали, что цементит может иметь переменную концентрацию углерода. Однако в дальнейшем, при разборе диаграммы состояния, сделаем допущение, что Fе3С имеет постоянный состав. Кристаллическая решетка цементита ромбическая, удельный вес 7,82 г/см3 (очень близок к удельному весу железа). При высоких температурах цементит диссоциирует, поэтому температура его плавления неясна и проставляется ориентировочно – 1260° С. Аллотропических превращений не испытывает. Кристаллическая решетка цементита состоит из ряда октаэдров, оси которых наклонены друг к другу. При низких температурах цементит слабо ферромагнитен, магнитные свойства теряет при температуре около 210° С. Цементит имеет высокую твердость (более 800 НВ, легко царапает стекло), но чрезвычайно низкую, практически нулевую, пластичность.
Цементит способен образовывать твердые растворы замещения. Атомы углерода могут замещаться атомами неметаллов: например, азотом; атомы железа – металлами: марганцем, хромом, вольфрамом и др. Такой твердый раствор на базе решетки цементита называется легированным цементитом.
Если графит является стабильной фазой, то цементит – это метастабильная фаза. Цементит – соединение неустойчивое и при определенных условиях распадается с образованием свободного углерода в виде графита. Этот процесс имеет важное практическое значение при структурообразовании чугунов.
Первичный цементит
Металлурги разделяют три типа этого вещества – первичный, вторичный, третичный.
Разновидности чугуна из сплава железа с углеродом
Выделяют два основных вида чугуна – литейный и предельный. Первый вид принято использовать в производстве и промышленной сфере. Второй находит применение в создании стали кислородно-конвертерным путем. В получившемся соединении доля марганца и кремния крайне мала.
Литейный чугун также имеет несколько разновидностей
:
- Половинчатая
. Такой чугун имеет специальные свойства, так как часть углерода из состава имеет форму цементита, а другая часть – форму графита. - Белая
. Здесь углерод находится в виде карбида железа. Название произошло от белого оттенка разлома. Белый чугун не находит применения в чистом виде, но активно используется при создании ковкого чугуна. - Серая
. Отлив на изломе серебристый, поэтому такой чугун называют серым. Сфера использования материала достаточно широкая, в том числе и потому, что чугун легко обрабатывать резцами. - Высокопрочная
. Данная разновидность способна увеличить прочность любого материала, куда она будет добавлена. Материал получают из серого чугуна и небольшого количества магния. - Ковкая
. Как и в случае высокопрочной разновидности, в основе находится серый чугун. Повысить пластичность помогает процесс отжига.
Другие структурные составляющие в системе «железо-углерод»
Кроме компонентов и фаз в системе сплавов «железо-углерод» присутствуют другие структурные составляющие — перлит и ледебурит.
Перлит
Перлит — эвтектоид, механическая смесь феррита и цементита, полученная в результате распада аустенита при охлаждении сплавов ниже 727° С. При медленном охлаждении перлит присутствует во всех сплавах с концентрацией углерода от 0,02 до 6,67%. Под микроскопом перлит может выглядеть либо как пластины, либо как зерна — зернистый перлит. Его вид, также как и механические свойства, зависит от скорости охлаждения сплава и вида его термической обработки.
Ледебурит в сталях
Ледебурит — эвтектика, механическая смесь аустенита и цементита, выделяющаяся из жидкости при охлаждении сплавов ниже 1147° С. Принципиальное отличие эвтектикой составляющей от эвтектоидной заключается в том, что первая выделяется из жидкости, а вторая из твердого раствора, в случае железоуглеродистых сплавов — из аустенита. Название данная структурная составляющая получила в честь имени немецкого ученого-металлурга Ледебура.
Шестигранник горячекатаный конструкционный
Маркировка металлов – один из главных характеристик, но, чтоб разобраться в их обилии, не непременно быть отличником по химии. Подобрать нужный по предназначению вид не так и трудно, довольно просто знать несколько главных моментов.
Систематизация железного сплава
Что влияет на свойство стали?
Углеродистая высококачественная сталь по ГОСТ обязана соответствовать содержанию не наименее 45% железа. Содержание углерода быть может от 0,1% до 2,4%. В единичных вариантах, по спец. заказу добавляют 3-3,4%. Чем больше содержание углерода, тем выше крепкость и твердость стали, но, при всем этом, понижается ее вязкость и пластичность.
В древности, индийцы и жители страны восходящего солнца получали железные слитки случайным соотношением главных компонент, что полностью не допустимо, в современном производстве. В высококачественных конструкционных сталях строго регламентированы добавки, такие как:
- · кремний
- · марганец
- · хром
- · никель
- · медь
- · Фосфор
- · Сера
От их содержания зависит классификационная группа высококачественной готовой стали:
- · Обычная (марка Ст, до 0,05% содержания P и S).
- · Высококачественная (марка Сталь, до 0,035 % — P и S).
- · Качественная (марка А, до 0,025 % — P и S).
- · Особовысококачественная (марка Ш, до 0,015 % — P и S).
Таковым образом, углеродистая конструкционная сталь приобретает новейшие высококачественные свойства. От ее физических, хим и механических характеристик зависит, где (в которой сфере, отрасли) будет употребляться этот высококачественный сплав и способности его предстоящей обработки.
Употребляются углеродистые высококачественные конструкционные стали по двум фронтам:
- · Машиностроительная ветвь
- · Строительная сфера
Таблицы хим состава дозволят буквально найти маркировку стали и возможность использования по предназначению. Содержание углерода в высококачественной конструкционной углеродистой стали по ГОСТ для строительства начинается от 0,3% в общем составе.
Марки машиностроительной стали
Основой для их производства является железоникелевая либо никелевая добавка. Не считая этого, для получения особых параметров, хим состав имеет незначимые количества принципиальных определяющих веществ. Исходя из этого, определены последующие группы стали:
- · Для производства изделий способом литья
- · Автоматные (А12,А20, А35)
- · С завышенной износостойкостью
- · С исключительной жаростойкостью (с добавлением кремния – 12Х17, 15Х28, 15Х6СМ, 20Х20Н14С2)
- · Шарикоподшипниковые
- · Пружинные
- · Криогенные (устойчивые к низким температурам регламентируются ГОСТом 5632)
- · Жаропрочные высококачественные конструкционные стали (из группы мартенситных, перлитных и аустенитных сталей).
Сплавы для строительной отрасли
Чтоб получить неплохую свариваемость метала количество углерода при изготовлении обязано быть в спектре от 0,1 до 0,2% с незначимым добавлением хрома, марганца и кремния. При всем этом сплав приобретает:
- · лучшую ковкость
- · жидкотекучесть
- · высшую твердость
- · ударную вязкость
- · лучший баланс удлинения и прочности
К группы таковых сплавов относятся марки 14Г2, 15ХСНД, 10Г2С1, 18Г2, 18Г2С, 25Г2С, 35ГС. Почаще всего их создают в виде проката, прута, листа и полос.
Если у вас все еще остались вопросцы, то спецы с радостью посодействуют сориентироваться в выборе изделий из высококачественной стали.
Чугуны
Сплавы на диаграмме железо-углерод, которые содержат углерода более, чем 2,14 %, называются чугунами. Они обладают высокой хрупкостью. Поперечное сечение такого чугуна имеет светлый тон, а потому его называют белым чугуном.
На диаграмме это точка С, называемая эвтектикой, с соответствующим содержанием углерода 4,3 %. При кристаллизации образуется смесь, состоящая из аустенита и цементита, в совокупности называемая ледебуритом. Фазовый состав постоянен.
При концентрации углерода менее 4,3 % (доэвтектический чугун) при кристаллизации выделяется аустенит из раствора. Далее из него выделяется Ц2. А при 727° С аустенит превращается в перлит. Структурное состояние такого чугуна следующее: крупные участки перлита темного тона.
В заэвтектическом белом чугуне (углерода более 4,3%) при охлаждении структурирование происходит с образованием кристаллов Ц1. Далее превращения осуществляются уже в твердом состоянии. Структура представляет собой ледебурит, который является фоном для полей перлита темного тона. А крупные пласты – это Ц1.
Строение и свойства
При повышении температуры аустенитные стали превращаются в жидкий раствор с определённым процентным отношением железа и углерода. Если температура раствора превышает линию так называемого ликвидуса (это около 1700 °C),образовавшийся расплав становится статически неустойчивым. Его состояние оценивают по двум составляющим:фазовой и структурной.
Для первой составляющей основным показателем является фаза состояния полученной смеси. Она определяет состояние металла по следующим показателям:
- раствора углерода в железе;
- количество различных образований (непосредственно феррит, в том числе высокотемпературный, аустенит, цементит).
Структурная составляющая часть образца определяется как гомогенная или квазигомогенная форма. Общая структура образовавшегося феррита составляет равноосные кристаллы. В трёхмерном пространстве решётка ферритной фазы представляет объёмно-центрированный куба. Эти кристаллы определяют твёрдость феррита и способность углерода в нём растворяться. Опыт показывает, что при температуре равной 727 градусов в феррите растворяется только 0,02% углерода.
Кроме этого к основным свойствам феррита относятся:
- обладает сильными ферромагнитными свойствами (до температуры 770 °С — точка Кюри);
- является теплопроводным элементом;
- хорошим проводником электрического тока;
- обладает повышенной пластичностью.
К основным недостаткам относятся невысокая прочность и недостаточная твёрдость. Последний показатель зависит от величины образованного зерна и находится в интервале от 65 до 130 НВ.
В зависимости от этапа проходящих превращений ферритная фаза находится в следующих состояниях:
- как основа кристаллической решётки образовавшегося сплава;
- второе или избыточное состояние (располагается по границам так называемых перлитных образований);
- элемент феррито-графитного эвтектоида.
Каждое состояние требует точного определения и выявления возникающих преобразований. От них во многом зависят характеристики конечного продукта.Полное отсутствие ферритного образования или незначительное его содержание проявляется с образованием горячих трещин. Завышенное содержание этого показателя снижает пластичность, ударную вязкость и антикоррозийную стойкость.
Выводы
Достичь абсолютного равновесия, как физического, так и химического, невозможно, кроме как в специальных лабораторных условиях.
На практике равновесие может быть приближено к абсолютному, но при определенных условиях: достаточно медленного повышения или понижения температуры сплава, который будет длительно выдерживаться по времени.
Источники
- https://FB.ru/article/340918/diagramma-jeleza-ugleroda-diagramma-sostoyaniya-sistemyi-jelezo-uglerod
- https://PokVorota3.ru/prokat/zhelezo-uglerod-2.html
- https://intehstroy-spb.ru/spravochnik/diagramma-sostoyaniya-zhelezo-uglerod-2.html
- https://NiceSpb.ru/materialy/diagramma-zhelezo.html
- https://pressadv.ru/stali/zhelezo-uglerod.html
- https://wiki2.org/ru/%D0%94%D0%B8%D0%B0%D0%B3%D1%80%D0%B0%D0%BC%D0%BC%D0%B0_%D1%81%D0%BE%D1%81%D1%82%D0%BE%D1%8F%D0%BD%D0%B8%D1%8F_%D1%81%D0%BF%D0%BB%D0%B0%D0%B2%D0%BE%D0%B2_%D0%B6%D0%B5%D0%BB%D0%B5%D0%B7%D0%BE-%D1%83%D0%B3%D0%BB%D0%B5%D1%80%D0%BE%D0%B4
- https://generator98.ru/raboty-so-stalyu/tablica-zhelezo-uglerod.html
Физика 8 класс. Плавление и кристаллизация
Физика 8 класс Конспект ПлавлениеПлавление и кристаллизация. Удельная теплота плавления.
Задачи на тему Тепловые явления
Переход вещества из твердого состояния в жидкое называется плавлением.
Плавление кристаллических тел происходит только при определенной температуре.
Температуру, при которой вещество плавится, называют температурой плавления вещества.
Чтобы провести процесс плавления, сначала надо нагреть твердое тело до температуры плавления.
Если тело нагреть до температуры плавления и убрать нагреватель (перестать подводить тепло к телу) — то плавления не происходит.
Чтобы осуществить плавление тела, надо выполнить два условия: 1. нагреть тело до температуры плавления 2. продолжить передачу теплоты
Температура плавления — важная тепловая характеристика вещества. У разных веществ температура плавления различна.
Плавление металла
Переход вещества из жидкого состояния в твердое называют отвердеванием или кристаллизацией.
Чтобы началась кристаллизация расплавленного (жидкого) тела, оно должно остыть до определенной температуры.
Температура, при которой вещество отвердевает (кристаллизуется), называют температурой отвердевания или кристаллизации.
График плавления и отвердевания кристаллических тел.
График плавления и отвердевания
Опыт показывает, что вещества отвердевают при той же температуре, при которой плавятся.
Чтобы осуществить процесс отвердевания нужно выполнить два условия: 1. охладить жидкость до температуры отвердевания (плавления) 2. продолжать отводить тепло до тех пор, пока вся жидкость не отвердеет.
Физическая величина, показывающая, какое количество теплоты необходимо сообщить кристаллическому телу массой 1 кг, чтобы при температуре плавления полностью перевести его в жидкое состояние, называется удельной теплотой плавления.
Удельную теплоту плавления обозначают буквой λ, измеряют в Дж/кг.
Чтобы вычислить количество теплоты Q, необходимое для плавления кристаллического тела массой m, взятого при его температуре плавления и нормальном атмосферном давлении,
нужно удельную теплоту плавления λ умножить на массу тела:
где Q– количество теплоты, m– масса тела.
Температура плавления и кристаллизации для данного вещества при неизменном внешнем давлении равны.
Кристаллизация
Количество теплоты, выделяющееся при кристаллизации вещества, при неизменном внешнем давлении равно количеству теплоты, полученному этим веществом при плавлении.
Задачи
Испарение и конденсация
Конспект составлен на основании теоретического материала учебника «Физика 8 класс» А.В. Перышкин, «Физика 8 класс»А.В.Грачев.
Скачать конспект:
teoriya_8_plavleniekristallizacziya
Физика 8 класс. Количество теплоты. Удельная теплоемкость. Топливо.
Физика 8 класс. Кипение. Конденсация.
Физика 8 класс. Испарение. Насыщенный пар. Влажность воздуха.
Физика 8 класс. Тепловые явления. Внутренняя энергия.
Полиморфные превращения
Более подробно о каждой фазе чуть ниже в статье. А если кратко, то осуществление главных превращений происходит при особых температурах.
Состояние железа обозначают как α-феррум (при температуре менее 911° С) . Кристаллическая решетка – объемный гранецентрированный куб. Или ОЦК. Дистанция между атомами такой решетки достаточно высокая.
Железо приобретает модификацию гамма, то есть обозначается как γ-феррум (911-1392° С) . Кристаллическая решетка – гранецентрированный куб (ГЦК). В этой решетке дистанция между атомами ниже, чем в ОЦК.
При переходе α-феррума в γ-феррум объем вещества становится меньшим. Причиной тому является кристаллическая решетка – ее вид. Потому что решетка ГЦК имеет более упорядоченное состояние атомов, чем ОЦК.
Если переход осуществляется в обратном направлении – из γ-феррума в α-феррум, то объем сплава увеличивается.
Когда температура достигает значения 1392° С (но менее температуры плавления железа 1539° С), то α-феррум превращается в δ-феррум, но это не является ее новой формой, а лишь разновидностью. К тому же δ-феррум является неустойчивой структурой.