Аргон является одним из наиболее распространенных химических элементов, представленных в атмосфере планеты Земля, занимая третье место после азота и кислорода. В то же время получение аргона – это ответственный и сложный с технологической точки зрения процесс, справиться с которым могут только настоящие профессионалы. Его особенность заключается в том, что в сфере промышленности этот инертный газ получают путем разделения воздуха на азот и O2.
Но есть и определенная сложность – температура кипения этого вещества находится между температурами кипения этих двух газов. Если быть более точным, то она менее чем на 3 градуса отличается от значения, при котором происходит закипание O2. Из-за этого разделить две фракции ректификационным методом невероятно сложно. Ведь Ar будет просто распределяться между другими веществами-компонентами воздуха, присоединяясь к кислороду в большинстве случаев.
Но широкое распространение Ar и его востребованность в самых различных сферах деятельности заставили человечество разрабатывать все более новые способы и технологические методы, позволяющие сделать процесс получения аргона более простым, удобным и эффективным. При этом многие из них связаны с получением технических газов, прошедших глубокую очистку (по теме особо чистых газообразных веществ вы можете прочитать наш отдельный материал).
История открытия
Предыстория открытия Ar началась в 1785 году. Выдающийся ученый и естествоиспытатель из Великобритании Генри Кэвендиш исследовал состав воздуха. Он подвергал азот окислению и взвешивал получившиеся окислы. По окончании опыта в сосуде оставался газ. Кэвендиш определил его объем в 0,8% от начального объема воздуха.
Состав этого газа ученый определить не смог. Спустя столетие к проблеме вернулись сэры Джон Рэлей и Уильям Рэмзи. В ходе проведенных опытов они обнаружили, что азот, выделенный из воздуха, имеет большую плотность, нежели азот, получаемый в ходе реакции разложения нитрита аммония.
в 1884 году им удалось выделить из воздуха некий газ, более плотный, чем азот. Это вещество имело одноатомную молекулярную структуру и было крайне инертным — т.е. не реагировало с другими веществами.
На заседании Королевского Общества новому газу было присвоено название «аргон», что в переводе с древнегреческого значило «спокойный, ленивый»
Преимущества и недостатки сварки в среде аргона
У аргонной сварки есть как плюсы, так и минусы, которые надо учитывать при выборе данного способа. Ее преимуществами являются:
- Отсутствие деформации заготовок из-за высокой температуры, поскольку не требуется значительно разогревать края деталей.
- Аргон – инертный газ, следовательно, он тяжелее воздуха. Значит, кислород не сможет проникнуть в сварочную ванну.
- Дуга имеет большую тепловую мощность, сварка происходит с высокой скоростью и хорошим качеством, если мастер имеет достаточную квалификацию.
- Несмотря на некоторые особенности аргонной сварки, процесс этот несложный, ему легко обучиться.
- Аргонной сваркой можно соединять металлы, которые невозможно соединить иным способом.
Недостаток аргонной сварки – невозможность ее проведения на открытом воздухе при наличии сильного ветра. Аргон разносится ветром, следовательно, плохо защищает шов, поэтому последний может быть некачественным. В закрытых помещениях сварку необходимо проводить только с использованием принудительной вентиляции. Кроме того, если необходимо применить высокоамперную сварочную дугу, то следует заранее решить, каким образом будет происходить охлаждение шва при проведении работ.
Аргон в природе
Ввиду практически полной инертности Ar представлен в естественной среде исключительно в несвязанном виде. Его процентная доля в различных частях Земли равна приблизительно:
- земная кора — 0,00012%;
- морская вода — 0,00045%;
- атмосфера — 0,926%.
Доля Ar в воздухе выше, чем суммарная доля всех остальных инертных газов. Основным источником для его добычи служит наша атмосфера.
Содержание газов в атмосфере
В коре Земли аргон содержится также в виде радиоактивного изотопа Аргон-40 и появляется в ходе реакции распада изотопов Калия.
Современная наука вместе с остальными инертными газообразными элементами относит Ar к VIII группе периодической системы.
Типы оборудования для аргонодуговой сварки
Существует несколько видов аргонной сварки, которые зависят от уровня механизации процесса:
- ручная;
- механизированная;
- автоматизированная;
- роботизированная.
Для каждого способы сварки необходимо определенное оборудование, соответственно, и стоимость работ различается.
При ручном способе сварки применяют неплавящиеся вольфрамовые электроды, подача проволоки осуществляется самим мастером, горелка для аргонодуговой сварки перемещается.
Механизированный способ характеризуется подачей присадочных прутков в автоматическом режиме, при этом мастер сам держит горелку.
Автоматизированная сварка полностью под контролем оператора – подача проволоки и перемещение горелки происходят автоматически.
Роботизированный процесс исключает и присутствие оператора.
Как добывают аргон
Благодаря значительному с промышленной точки зрения содержанию аргона в воздухе его получают в качестве дополнительного продукта криогенной ректификации O2 и N2.
Технология основана на том факте, что температура кипения (или сжижения) Ar лежит между температурами N2 и O2.
Перед началом процесса воздух подвергается тщательной очистке от пыли в многоступенчатых фильтрах, осушается от водяных паров, а далее мощными компрессорами сжимается до тех пор, пока не перейдет в жидкое состояние. Жидкость перегоняют в ректификационной колонне, чтобы разделить ее на отдельные вещества.
Установка для добычи аргона
Первым испаряется азот при -195 °С, его пары собираются на соответствующей тарелке ректификатора и отводятся в отдельный резервуар. Следующим по высоте (и при температуре кипения -185 °С) отбирается аргонная фракция, содержащая 12% Ar, менее полпроцента азота и кислород. Она подается в следующую ректификационную колонну, в которой процентная доля Ar доводится до 85, оставшееся приходится на кислород со следами азота. Такое вещество называется сырым аргоном, исходным материалом для получения очищенного газа.
В промышленности применяется несколько методов очистки сырого аргона от примесей.
Водород, добавляемый в состав сырья, окисляется на катализаторе и нагреве до 500 °С, таким образом, из состава смеси выводится кислород. Образовавшийся на катализаторе водяной пары удаляют при посредстве влагоотделителя. Газ после этого осушают. Аргон с оставшимся в нем азотом вновь ректифицируют.
Применяются и альтернативные методы получения Ar. Во время синтеза аммиака из азота и водорода в химических реакторах Ar получают как сопутствующий продукт производства. Технологический компонент это синтеза — продувочный газ — содержит до 20% Ar. Из этого газа и извлекают самый спокойный элемент. Стоимость производства, складывающаяся в основном из затрат на охлаждение и нагрев компонентов, делится между аммиаком и аргоном, и получается существенно ниже.
Качество газа, получаемого любым методом, определяется технологией очистки его от небольших количеств остаточного N2, O2, водяных паров и H2.
Аппарат, получающий ионные пучки аргона
Где применяется аргон
Аргон получил большое распространение в промышленности. Инертные свойства этого газа особенно востребованы в различных производственных процессах, где необходимо вытеснить один из самых активных элементов – кислород. Использование аргона очень дёшево, в сравнении с другими инертными летучими веществами, поэтому газ незаменим в том случае, когда требуется защитная среда при сваривании металлов, а также вытеснение влаги и кислорода в ёмкостях, где хранятся пищевые продукты.
Наполнение колб ламп накаливания инертным газом, позволяет значительно увеличить ресурс работы осветительного прибора. Кроме повышенного срока использования такие элементы обладают большей яркостью. Используется инертный газ и при производстве люминесцентных ламп. Применение аргона позволяет облегчить запуск разряда электрической дуги, а также значительно увеличить ресурс электродов.
При изготовлении стеклопакетов, инертным газом заполняются полости между стёклами, что позволяет значительно улучшить теплоизоляционные свойства. Учитывая тот факт, что аргон является абсолютно прозрачным, использование его никак не ограниченно даже при изготовлении многослойных конструкций.
Инертный газ аргон используется также в установках плазменной резки металлов. Преимущество использования этого газа заключается в том, что для возникновения дуги не требуется слишком высокого напряжения, поэтому такие установки могут иметь очень простую конструкцию. При генерации плазмы с использованием аргона образуется минимальное количество вредных газообразных веществ во время выполнения резки, поэтому этот метод идеально подходит для ручных приборов.
Благодаря возможности образовывать плазму при относительно невысоком напряжении, этот благородный газ используется в медицине для проведения аргоновой коагуляции. Такой метод успешно используется для удаления новообразований, а также для остановки кровотечений.
Аргон применяется и в химической промышленности. Благодаря отсутствию взаимодействия с другими элементами этот газ используется для получения сверхчистых веществ, а также для их анализа. В металлургической промышленности благородный газ позволяет обрабатывать такие металлы, как: титан, тантал, ниобий, бериллий, цирконий и др. Кроме этого, газ используется для перемешивания расплавленных веществ и снижения окисления хрома при производстве хромированной стали.
Общая характеристика Ar
Ar входит в группу инертных газов. Заряд его ядра — 18, под таким же номером элемент располагается в таблице Менделеева.
Из всех участников VIIIA группы он является наиболее часто встречающимся в природе. Объемная доля Ar в атмосфере -0,93%, массовая доля составляет 1,28%.Элемент является газом без цвета, вкуса и запаха. Химически не активен – аргон не вступает в реакцию и практически не соединяется ни с какими элементами или веществами, за исключением CU(Ar)O, и гидрофторида аргона.
Весьма плохо растворим водой, чуть большая растворимость наблюдается при взаимодействии с органическими растворителям.
Свойства аргона (таблица): температура, плотность, давление и пр.
| Название | Аргон |
| Латинское название | Argon |
| Английское название | Argon |
| Символ | Ar |
| Атомный номер (номер в таблице) | 18 |
| Тип | Неметалл |
| Группа | Инертный (благородный) газ |
| Открыт | Уильям Рамзай, Джон Уильям Стретт (лорд Рэлей), Великобритания, 1894 г. |
| Год открытия | 1894 г. |
| Внешний вид и пр. | Инертный газ без цвета, вкуса и запаха |
| Происхождение | Природный материал |
| Содержание в атмосфере и воздухе (по массе) | 1,292 % |
| Содержание в земной коре (по массе) | 0,00015 % |
| Содержание в морях и океанах (по массе) | 0,000045 % |
| Содержание во Вселенной и космосе (по массе) | 0,02 % |
| Содержание в Солнце (по массе) | 0,007 % |
| Атомная масса (молярная масса) | 39,948(1) а. е. м. (г/моль) |
| Электронная конфигурация | 1s2 2s2 2p6 3s2 3p6 |
| Электронная оболочка | K2 L8 M8 N0 O0 P0 Q0 R0 |
| Радиус атома (вычисленный) | 71 пм |
| Ковалентный радиус* | 106 пм |
| Радиус Ван-дер-Ваальса | 188 пм |
| Электроны, Протоны, Нейтроны | 18 электронов, 18 протонов, 22 нейтронов |
| Семейство (блок) | элемент p-семейства |
| Период в периодической таблице | 3 |
| Группа в периодической таблице | 18-ая группа (по старой классификации – главная подгруппа 8-ой группы) |
| Степени окисления | 0 |
| Валентность | 0 |
| Электроотрицательность | 4,3 (шкала Полинга) |
| Энергия ионизации (первый электрон) | 1520,57 кДж/моль (15,7596117(5) эВ) |
| Электродный потенциал | 0 |
| Энергия сродства атома к электрону | 0 кДж/моль |
| Плотность* | 0,001784 г/см3 (при 0 °C и иных стандартных условиях, состояние вещества – газ), 1,3954 г/см3 (при температуре кипения -185,848 °C и иных стандартных условиях, состояние вещества – жидкость),1,65 г/см3 (при -233 °C и иных стандартных условиях, состояние вещества – твердое тело) |
| Температура плавления* | -189,34 °C (83,81 K, -308,81 °F) |
| Температура кипения* | -185,848 °C (87,302 K, -302,526 °F) |
| Удельная теплота плавления (энтальпия плавления ΔHпл)* | 1,18 кДж/моль |
| Удельная теплота испарения (энтальпия кипения ΔHкип)* | 6,53 кДж/моль |
| Молярная теплоёмкость* | 20,85 Дж/(K·моль) |
| Молярный объём | 24,2 см³/моль |
| Теплопроводность | 17,72·10-3 Вт/(м·К) (при стандартных условиях), 0,0164 Вт/(м·К) (при 300 K) |
| Структура решётки | Кубическая гранецентрированная |
| Параметры решётки | 5,260 Å |
| Температура Дебая | 85 К |
| Название пространственной группы симметрии | Fm_ 3m |
| Номер пространственной группы симметрии | 225 |
| Номер CAS | 7440-37-1 |
Примечание:
206* Ковалентный радиус аргона согласно [1] составляет 106±10 пм.
401* Плотность аргона согласно [3] и [4] [Россия] составляет 0,0017839 г/см3 (при 0 °C /20 °C и иных стандартных условиях, состояние вещества – газ).
402* Температура плавления аргона согласно [3] и [4] составляет -189,35 °C (83,8 K, -308,83 °F) и -189,6 °C (83,55 K, -309,28 °F) соответственно.
403* Температура кипения аргона согласно [3] и [4] составляет -185,85 °C (87,3 K, -302,53 °F) и -185,9 °C (87,25 K, -302,62 °F) соответственно.
407* Удельная теплота плавления (энтальпия плавления ΔHпл) аргона согласно [3] и [4] составляет 7,05 кДж/моль и 1,19 кДж/моль соответственно.
408* Удельная теплота испарения (энтальпия кипения ΔHкип) аргона согласно [3] и [4] составляет 6,45 кДж/моль и 6,51 кДж/моль соответственно.
410* Молярная теплоемкость аргона [3] составляет 20,79 Дж/(K·моль).
Виды аргона
Говоря о видах, или сортах Ar, надо понимать, что это одно и то же химическое вещество. Виды различаются по степени очистки от примесей.
- Высший сорт. Содержание Ar не менее 99,99% . Этот сорт особо высокой чистоты применяется для ответственных сварочных работ, таких, как сварка материалов, химически активных в нагретом состоянии: некоторые цветные сплавы, прежде всего титановые, нержавеющая сталь и др. Используется также для сварки высоконагруженных изделий из конструкционной стали.
- Первый сорт. Содержание Ar не менее 99,98%, Применяется при сварке сплавов на основе алюминия с другими металлами и сплавами, для менее активных цветных металлов.
- Второй сорт. Содержание Ar не менее 99,95%. Используется при сваривании деталей из жаростойких стальных сплавов, алюминия и конструкционных сталей. Применение чистого Ar в этих случаях нежелательно, поскольку приводит к повышенной пористости материала шва и не позволяет защитить сварочную ванну от повышенной влажности и других загрязнений. Во избежание возникновения такого дефекта в состав смеси защитных газов добавляют углекислый газ и кислород, связывающие выделяющийся при сварке водород и другие примеси. Образующиеся в ходе этих реакций шлаки всплывают на поверхность сварочной ванны и после застывания удаляются вместе с окалиной.
Производство аргона
Технический газ аргон получают в качестве побочного продукта производственного процесса, в ходе которого кислород отделяют от азота. Для этого применяются специальные камеры с использованием воздухоразделительных аппаратов с двукратной ректификацией. Аргон обладает большими летучими свойствами, чем кислород, и меньшими, чем азот. Поэтому в процессе разделения воздуха на кислород и азот аргон остается в средней фракции. Из средней точки верхней колонны аппарата аргон направляют в специальные камеры для сжатия и хранения.
При первичном отборе массовая доля аргона в отобранной фракции составляет ничтожно малые показатели, всего около пяти процентов. Это так называемый сырой аргон. После последующей конденсации и очистки удается получить чистый аргон с массовой долей содержания его во фракции около 99,99 процентов. Практикуется так же способ извлечения аргона в процессе утилизации отходов аммиачного производства. В этом случае аргон получают из азота, оставшегося после связывания его с молекулами водорода.
Физические и химические свойства
Свойства аргона типичны для члена VIII группы.
При обычной температуре Ar пребывает в газообразном состоянии. Молекула включает в себя единственный атома, химическая формула весьма простая: Ar. Температура кипения весьма низка : -185,8 °С при атмосферном уровне давления.
Растворимость в воде низкая — всего 3,29 мл на 100 мл жидкости
Плотность аргона при нормальных условиях составляет 1,78 кг/м3. Молярная теплоемкость газа- 20,7 Дж/Кмоль.
Характеристики аргона и других инертных газов
Газ практически полностью инертен. На сегодняшний день ученым удалось получить лишь два его соединения — CU(Ar)O, и гидрофторид аргона. Соединения существуют лишь при сверхнизких температурах. Предполагается, что Ar может входить в состав неустойчивых в нормальном состоянии молекул эксимерного типа. Такие молекулы могут существовать лишь в возбужденном состоянии, например, в ходе электроразряда высокой интенсивности. Такие соединения возможны с ртутью, кислородом и фтором.
Электроотрицательность по шкале Полинга равна 4,3.
Как степень окисления, так и электродный потенциал имеют нулевое значение, что характерно для инертного газа.
Ионный радиус составляет 154, радиус ковалентности — 106 Пм. Ионизационный порог- 1519 кдж/моль
Атомная и молекулярная масса
Такие важные параметры, как атомная и молекулярная массы, показывают, насколько масса молекулы вещества и масса его атома соответственно превышают значение, равное одной двенадцатой доле массы атома водорода.
Ввиду того, что молекула Ar состоит из единственного атома, молекулярная и атомная масса аргона идентичны и составляют 39,984.
Структура аргона и его свойства
Изотопы
В природных условиях Ar встречается в качестве трех устойчивых изотопов
- 36Ar– процентная доля этого изотопа составляет 0,337% в ядре 18 протонов и 18 нейтронов;
- 38Ar- его доля всего 0,063%, в ядре 18 протонов и 20 нейтронов;
- 40Ar – наиболее распространен, его доля составляет 99,6%, в ядре так же 18 протонов, но уже 22 нейтрона.
Искусственным путем удавалось получать изотопы с массовым индексом от 32 до 55, наиболее стабильным из них оказался 39Ar, период полураспада которого составляет 268 лет.
Большая процентная доля 40Ar среди изотопов, встречающихся в природе, вызвана постоянным образованием его в ходе реакции распада изотопа калий-40. На 1000 кг калия в ходе таких реакций за год образуется не более 3100 атомов 40Ar. Но, поскольку эти реакции идут постоянно в течение сотен миллионов лет, изотоп накопился в природе в существенных объемах.
Доминирование тяжелого изотопа в природе обуславливает тот факт, что атомный вес Ar превышает атомный вес калия, находящегося в таблице следом за ним. При создании Периодической системы такого противоречия не было, поскольку аргон был обнаружен и свойства его были исследованы значительно позже, в первом десятилетии XX века. Первоначально Ar был помещен в первую группу таблицы, восьмая группа была выделена позднее.
Ионы
Как и другие инертные газы (такие, как He и Ne), Ar подвержен ионизации. При возбуждении атомов и сообщении им высоких энергий возникают молекулярные ионы Ar2+.
Молекула и атом
Для инертных газов эти понятия идентичны, поскольку эти элементы не желают вступать в химическую связь даже с себе подобными. Молекула включает в себя один атом, химическая формула газа не отличается от обозначения элемента: Ar.
Молярная масса
Молярная масса аргона составляет 39,95 г/моль.
Существуют несколько методов ее вычисления:
- С применением относительной атомной массы M и коэффициента пропорциональности к, выражающего соотношение между относительной массой и молярной. Этот коэффициент является универсальной константой и равен для всех элементов. Молярная масса M выражается как произведение коэффициента пропорциональности на относительную массу.
- С использованием молярного объема. Потребуется найти объем, занимаемый при обычных условиях некоторой массой газа, далее рассчитать массу 22,4 литров вещества при таких же условиях.
- С применением уравнения Менделеева-Клапейрона, моделирующего идеальный газ.
pV = mRT / M,
проведя преобразования, получим выражение для молярной массы:
M=mRT/pV
где
- p – давление в паскалях,
- V –объем в кубометрах
- m – масса в граммах,
- Т — температура в Кельвинах,
- R – константа, значение которой 8,314 Дж/(моль×К).
Что представляет собой аргон?
Это одноатомный инертный газ, который не имеет какого-либо запаха, цвета и вкуса. Он является одним из основных компонентов воздуха, а также в больших количествах содержится в атмосфере нашей планеты. Температура его кипения составляет минус 185.9 градусов по Цельсию, при этом такая отметка находится очень близко от отметки кипения O2. Следует обратить внимание, что, находясь в воздухе в больших концентрациях, он может быть опасен для человека, так как вытесняет кислород и приводит к проявлению симптомов кислородного голодания.
Согласно государственным стандартам (ГОСТ) находящийся в газообразном состоянии Ar должен храниться и транспортироваться в специально предназначенных для этого газовых баллонах, сделанных с применением стального сплава. Чистое вещество должно находиться в емкостях, обладающих соответствующим окрасом и маркировкой – баллон серого цвета с зеленой надписью: «Аргон чистый».
Область применения
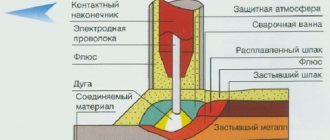
Шире всего аргон применяется при сварочных работах. Он используется для создания защитной атмосферы вокруг сварочной ванны, вытесняя из рабочей зоны O2 и N2, содержащиеся в атмосфере. Особенно важно это для сварки цветных металлов, многие из которых, к примеру, Ti, отличаются высокой химической активностью в нагретом состоянии. Незаменим инертный газ также для неразъемного соединения нержавеющих и высоколегированных сплавов.
Также широко применяется при монтаже высоконагруженных строительных конструкций, таких, как каркасы высотных зданий, фермы мостов и многих других. Здесь его применение обеспечивает высокое качество, однородность и долговечность ответственных соединений. В строительной индустрии аргонная сварка доминирует среди других методов.
Сварка аргоном
Аргонно-дуговая сварка
Не менее широко применяется аргонная сварка в машиностроении, прежде всего химическом и пищевом. Швы получаются долговечные и надежные, даже в условиях воздействия агрессивных сред.
Нефтяная и газовая отрасли также применяют аргонная сварку при монтаже трубопроводов, газоперекачивающих станций и нефтеперегонных комбинатов.
Используется метод также в атомной промышленности, в транспортном машиностроении и в аэрокосмической отрасли.
В домохозяйствах аргонная сварка распространена не так широко. Это объясняется:
- высокой стоимостью оборудования и расходных материалов;
- необходимостью достаточной квалификации сварщика;
- меньшими нагрузками, испытываемыми домашними конструкциями;
- более низкими требованиями к прочности и долговечности сварных соединений.
Если в домохозяйстве возникает эпизодическая потребность в таких сварочных работах, то дешевле, быстрее и надежнее пригласить сварщика-специалиста.
Стеклопакет с аргоном
Принцип действия стеклопакета с аргоном
Характерным свойством Ar является его более высокая плотность по сравнению с воздухом. Поэтому максимальная эффективность аргонной сварки достигается при нижнем сварочном положении. В этом случае инертный раз растекается по поверхности детали и образует защитное облако значительной протяженности, позволяя вести сварку, как большими токами, так и на большой скорости. При сварке в наклонном и верхнем положении приходится учитывать «проваливание» аргона сквозь воздух. Чтобы компенсировать это явление, либо увеличивают подачу газа, либо проводят работы в герметичном помещении, заполненным инертным газом. В обоих случаях себестоимость работ возрастает.
Поскольку потенциал ионизации Ar невысок, его использование обеспечивает идеальные геометрических характеристик сварочного шва, прежде всего, профиля. Возбужденная электродуга в аргоновой атмосфере также отличается высокой стабильностью своих параметров. С другой стороны, низкое значение потенциала ионизации обуславливает и более низкое напряжение розжига и поддержания дуги. Это сокращает ее тепловыделение и усложняет провар толстых листов металла.
Более высокая температура дуги в аргоновой атмосфере существенно повышает проплав сварочного шва. Это позволяет проводить сварку за один проход при условии точного соблюдения параметров зазора между заготовками.
В случае применения TIG-метода сварочных работ аргоновая атмосфера защищает от коррозионного влияния не только зону сварки, но и окончание неплавкого электрода.
В ряде специфических случаев в состав защитной газовой смеси добавляют гелий.
Кроме применения при сварочных работах, аргон используется:
- Как плазмоообразующее веществона установках плазменного раскроя металла.
- Для создания инертной среды в упаковках пищевых продуктов. Он вытесняет из пакетов и контейнеров кислород воздуха и водяные пары, пагубно влияющие на срок годности продуктов. Продукты в защитной атмосфере хранятся в несколько раз дольше, чем в обычной упаковке. Применяется этот метод и для упаковки медицинских изделий и препаратов, позволяя сохранить их в должной стерильности и химической чистоте.
- В качестве активного агента в противопожарных установках. Аргон вытесняет кислород (или другой газ) из очага горения, прекращая его.
- Для создания защитной среды в технологических установках при обработке полупроводниковых устройств, создании микросхем и других электронных компонентов или материалов высоких степеней чистоты.
- Наполнитель электроламп.
- В рекламных люминесцентных трубках.
Применение
Применения аргона:
- в аргоновых лазерах
- в лампах накаливания и при заполнении внутреннего пространства стеклопакетов
- в качестве защитной среды при сварке (дуговой, лазерной, контактной и т. п.) как металлов, так и неметаллов
- в качестве плазмаобразователя в плазматронах при сварке и резке
- в пищевой промышленности аргон зарегистрирован в качестве пищевой добавки E938, в качестве пропеллента и упаковочного газа
- в качестве огнетушащего вещества в газовых установках пожаротушения
Биологическая роль
Аргон не играет никакой биологической роли.
Физиологическое действие
Инертные газы обладают физиологическим действием, которое проявляется в их наркотическом воздействии на организм. Наркотический эффект от вдыхания аргона проявляется только при барометрическом давлении свыше 0,2 МПа.. Содержание аргона в высоких концентрациях во вдыхаемом воздухе может вызвать головокружение, тошноту, рвоту, потерю сознания и смерть от асфиксии (в результате кислородного голодания).
Периодическая система химических элементов Менделеева
Классификация хим. элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона/
Периодическая система элементов
| IA | IIA | IIIB | IVB | VB | VIB | VIIB | —- | VIIIB | —- | IB | IIB | IIIA | IVA | VA | VIA | VIIA | VIIIA | |
| Период | ||||||||||||||||||
| 1 | 1 H Водород | 2 He Гелий | ||||||||||||||||
| 2 | 3 Li Литий | 4 Be Бериллий | 5 B Бор | 6 C Углерод | 7 N Азот | 8 O Кислород | 9 F Фтор | 10 Ne Неон | ||||||||||
| 3 | 11 Na Натрий | 12 Mg Магний | 13 Al Алюминий | 14 Si Кремний | 15 P Фосфор | 16 S Сера | 17 Cl Хлор | 18 Ar Аргон | ||||||||||
| 4 | 19 K Калий | 20 Ca Кальций | 21 Sc Скандий | 22 Ti Титан | 23 V Ванадий | 24 Cr Хром | 25 Mn Марганец | 26 Fe Железо | 27 Co Кобальт | 28 Ni Никель | 29 Cu Медь | 30 Zn Цинк | 31 Ga Галлий | 32 Ge Германий | 33 As Мышьяк | 34 Se Селен | 35 Br Бром | 36 Kr Криптон |
| 5 | 37 Rb Рубидий | 38 Sr Стронций | 39 Y Иттрий | 40 Zr Цирконий | 41 Nb Ниобий | 42 Mo Молибден | (43) Tc Технеций | 44 Ru Рутений | 45 Rh Родий | 46 Pd Палладий | 47 Ag Серебро | 48 Cd Кадмий | 49 In Индий | 50 Sn Олово | 51 Sb Сурьма | 52 Te Теллур | 53 I Иод | 54 Xe Ксенон |
| 6 | 55 Cs Цезий | 56 Ba Барий | * | 72 Hf Гафний | 73 Ta Тантал | 74 W Вольфрам | 75 Re Рений | 76 Os Осмий | 77 Ir Иридий | 78 Pt Платина | 79 Au Золото | 80 Hg Ртуть | 81 Tl Таллий | 82 Pb Свинец | 83 Bi Висмут | (84) Po Полоний | (85) At Астат | 86 Rn Радон |
| 7 | 87 Fr Франций | 88 Ra Радий | ** | (104) Rf Резерфордий | (105) Db Дубний | (106) Sg Сиборгий | (107) Bh Борий | (108) Hs Хассий | (109) Mt Мейтнерий | (110) Ds Дармштадтий | (111) Rg Рентгений | (112) Cp Коперниций | (113) Uut Унунтрий | (114) Uuq Унунквадий | (115) Uup Унунпентий | (116) Uuh Унунгексий | (117) Uus Унунсептий | (118) Uuo Унуноктий |
| 8 | (119) Uue Унуненний | (120) Ubn Унбинилий | ||||||||||||||||
| Лантаноиды * | 57 La Лантан | 58 Ce Церий | 59 Pr Празеодим | 60 Nd Неодим | (61) Pm Прометий | 62 Sm Самарий | 63 Eu Европий | 64 Gd Гадолиний | 65 Tb Тербий | 66 Dy Диспрозий | 67 Ho Гольмй | 68 Er Эрбий | 69 Tm Тулий | 70 Yb Иттербий | 71 Lu Лютеций | |||
| Актиноиды ** | 89 Ac Актиний | 90 Th Торий | 91 Pa Протактиний | 92 U Уран | (93) Np Нептуний | (94) Pu Плутоний | (95) Am Америций | (96) Cm Кюрий | (97) Bk Берклий | (98) Cf Калифорний | (99) Es Эйнштейний | (100) Fm Фермий | (101) Md Менделевий | (102) No Нобелей | (103) Lr Лоуренсий | |||
Химические семейства элементов периодической таблицы
| Щелочные металлы | Щёлочноземельные металлы | Лантаноиды | Актиноиды | Переходные металлы |
| Лёгкие металлы | Полуметаллы | Неметаллы | Галогены | Инертные газы |
Зависимость давления аргона в баллоне от температуры
По мере нагрева давление газообразного вещества в замкнутом объеме повышается. В таблице приведены примерные значения давления в баллоне в зависимости от температуры окружающего воздуха.
| T, °C | P, Мегапаскаль |
| -40 | 10,45 |
| -30 | 11,33 |
| -20 | 12,21 |
| -10 | 12,92 |
| 0 | 13,74 |
| +10 | 14,62 |
| +20 | 15,33 |
| +30 | 16,03 |
Следует учитывать, что баллонное давление изменяется не мгновенно, а по мере его прогрева или охлаждения.
Сферы применения аргонной сварки
Для чего используют аргонную сварку? Она необходима в случаях, когда сварочные швы должны быть выполнены безукоризненно. Особенно часто с ее помощью соединяют трудно свариваемые материалы и заготовки с тонкими стенками. Данный вид сварки востребован в авиа- и ракетостроении, автомобильной промышленности. Посредством такого соединения изготавливают важные узлы из алюминия и его сплавов.
Чаще всего аргонодуговую сварку применяют при работе с алюминием, который является трудно свариваемым, часто трескается, дает сильную усадку. Кроме того, в расплавленном состоянии этот металл легко окисляется, покрываясь тугоплавкой пленкой, которая препятствует образованию шва. И только сварка в среде аргона поможет получить швы высокого качества.
Особенно востребована такая сварка на автомобильных СТО, где с помощью такого способа соединения период эксплуатации деталей значительно продлевается.
Для чего используют аргонную сварку на станциях техобслуживания автомашин? Она может применяться при ремонте радиаторов, разных частей коробок переключения передач, трубок от кондиционеров и прочих элементов, сделанных из алюминия и его сплавов. Пайку и плазменное напыление, как и иные способы сварки, невозможно было бы использовать для таких работ, поскольку детали имеют технические особенности.
Получение Аргона
3.3 Получение Аргона.
Земная атмосфера содержит 66 · 1013 т аргона. Этот источник аргона неисчерпаем, тем более что практически весь аргон рано или поздно возвращается в атмосферу, поскольку при использовании он не претерпевает никаких физических или химических изменений. Исключение составляют весьма незначительные количества изотопов аргона, расходуемые на получение в ядерных реакциях новых элементов и изотопов. Получают аргон как побочный продукт при разделении воздуха на кислород и азот. Обычно используют воздухоразделительные аппараты двукратной ректификации, состоящие из нижней колонны высокого давления (предварительное разделение), верхней колонны низкого давления и промежуточного конденсатора-испарителя. В конечном счете азот отводится сверху, а кислород – из пространства над конденсатором. Летучесть аргона больше, чем кислорода, но меньше, чем азота. Поэтому аргонную фракцию отбирают в точке, находящейся примерно на трети высоты верхней колонны, и отводят в специальную колонну. Состав аргонной фракции: 10…12% аргона, до 0,5% азота, остальное – кислород. В «аргонной» колонне, присоединенной к основному аппарату, получают аргон с примесью 3…10% кислорода и 3…5% азота. Дальше следует очистка «сырого» аргона от кислорода (химическим путем или адсорбцией) и от азота (ректификацией). В промышленных масштабах ныне получают аргон до 99,99%-ной чистоты. Аргон извлекают также из отходов аммиачного производства – из азота, оставшегося после того, как большую его часть связали водородом. Аргон хранят и транспортируют в баллонах емкостью 40 л, окрашенных в серый цвет с зеленой полосой и зеленой надписью. Давление в них 150 атм. Более экономична перевозка сжиженного аргона, для чего используют сосуды Дюара и специальные цистерны. Искусственные радиоизотопы аргона получены при облучении некоторых стабильных и радиоактивных изотопов (37Cl, 36Аr, 40Аr, 40Са) протонами и дейтонами, а также при облучении нейтронами продуктов, образовавшихся в ядерных реакторах при распаде урана. Изотопы 37Аr и 41Аr используются как радиоактивные индикаторы: первый – в медицине и фармакологии, второй – при исследовании газовых потоков, эффективности спетом вентиляции и в разнообразных научных исследованиях. Но, конечно, не эти применения аргона самые важные.
3.4 Физиологическое действие инертных газов.
Естественно было ожидать, что столь химически инертные вещества, как инертные газы, не должны влиять и на живые организмы. Но это не так. Вдыхание высших инертных газов (конечно в смеси с кислородом) приводит человека в состояние, сходное с опьянением алкоголем. Наркотическое действие инертных газов обуславливается растворением в нервных тканях. Чем выше атомный вес инертного газа, тем больше его растворимость и тем сильнее его наркотическое действие.
Теперь о влиянии аргона на живой организм. При вдыхании смеси из 69% Ar, 11% азота и 20% кислорода под давлением 4 атм возникают явления наркоза, которые выражены гораздо сильнее, чем при вдыхании воздуха под тем же давлением. Наркоз мгновенно исчезает после прекращения подачи аргона. Причина – в неполярности молекул аргона, повышенное же давление усиливает растворимость аргона в нервных тканях. Биологи нашли, что аргон благоприятствует росту растений. Даже в атмосфере чистого аргона семена риса, кукурузы, огурцов и ржи выкинули ростки. Лук, морковь и салат хорошо прорастают в атмосфере, состоящей из 98% аргона и только 2% кислорода.
IV Применение инертных газов.
Гелий является важным источником низких температур. При температуре жидкого гелия тепловое движение атомов и свободных электронов в твердых телах практически отсутствует, что позволяет изучать многие новые явления, например сверхпроводимость в твердом состоянии.
Газообразный гелий используют как легкий газ для наполнения воздушных шаров. Поскольку он негорюч, его добавляют к водороду для заполнения оболочки дирижабля.
Так как гелий хуже растворим в крови, чем азот, большие количества гелия применяют в дыхательных смесях для работ под давлением, например при морских погружениях, при создании подводных тоннелей и сооружений. При использовании гелия декомпрессия (выделение растворенного газа из крови) у водолаза протекает менее болезненно, менее вероятна кессонная болезнь, исключается такое явление, как азотный наркоз, – постоянный и опасный спутник работы водолаза. Смеси He–O2 применяют, благодаря их низкой вязкости, для снятия приступов астмы и при различных заболеваниях дыхательных путей.
Гелий используют как инертную среду для дуговой сварки, особенно магния и его сплавов, при получении Si, Ge, Ti и Zr, для охлаждения ядерных реакторов.
Другие применения гелия – для газовой смазки подшипников, в счетчиках нейтронов (гелий-3), газовых термометрах, рентгеновской спектроскопии, для хранения пищи, в переключателях высокого напряжения. В смеси с другими благородными газами гелий используется в наружной неоновой рекламе (в газоразрядных трубках). Жидкий гелий выгоден для охлаждения магнитных сверхпроводников, ускорителей частиц и других устройств. Необычным применением гелия в качестве хладагента является процесс непрерывного смешения 3He и 4He для создания и поддержания температур ниже 0,005 K
Области применения ксенона разнообразны и порой неожиданны. Человек использует и его инертность и его чудесную способность вступать в реакцию со фтором. В светотехнике признание получили ксеноновые лампы высокого давления. В таких лампах светит дуговой разряд в ксеноне, находящемся под давлением в несколько десятков атмосфер. Свет в ксеноновых лампах появляется сразу после включения, он ярок и имеет непрерывный спектр — от ультрафиолетового до ближней области инфракрасного. Ксеноном пользуются и медики — при рентгеноскопических обследованиях головного мозга. Как и баритовая каша, применяющаяся при просвечивании кишечника, ксенон сильно поглощает рентгеновское излучение и помогает найти места поражения. При этом он совершенно безвреден. Активный изотоп элемента № 54, ксенон — 133, используют при исследовании функциональной деятельности легких и сердца.
Продувкой аргона через жидкую сталь из нее удаляют газовые включения. Это улучшает свойства металла.
Все шире применяется дуговая электросварка в среде аргона. В аргонной струе можно сваривать тонкостенные изделия и металлы, которые прежде считались трудносвариваемыми. Не будет преувеличением сказать, что электрическая дуга в аргонной атмосфере внесла переворот в технику резки металлов. Процесс намного ускорился, появилась возможность резать толстые листы самых тугоплавких металлов. Продуваемый вдоль столба дуги аргон (в смеси с водородом) предохраняет кромки разреза и вольфрамовый электрод от образования окисных, нитридных и иных пленок. Одновременно он сжимает и концентрирует дугу на малой поверхности, отчего температура в зоне резки достигает 4000—6000° С. К тому же эта газовая струя выдувает продукты резки. При сварке в аргонной струе нет надобности во флюсах и электродных покрытиях, а стало быть, и в зачистке шва от шлака и остатков флюса.
Неон и аргон используются, как наполнители в неоновых лампах и лампах дневного свата Криптоном наполняют обычные лампы с целью уменьшения испарения и увеличения яркости свечения вольфрамовой нити. Ксеноном наполняют кварцевые лампы высокого давления, являющиеся наиболее мощными источниками света. Гелий и аргон используется в газовых лазерах.
Список использованной литературы
1. Петров М.М., Михилев Л.А., Кукушкин Ю.Н. “Неорганическая химия”
2. Гузей Л.С. Лекции по общей химии”
3. Ахметов Н.С. “Общая и неорганическая химия”
4. Некрасов Б.В. “Учебник общей химии”
5. Глинка Н.Л. “Общая химия
6. Ходаков Ю.В. “Общая и неорганическая химия”
… превращения изолированных молекул. Но это — тема для отдельной статьи. Для нашей же истории важно, что такая матричная изоляция неожиданно для всех привела в совершенно новую область химии инертных газов. И случилось это в результате одной встречи на международной конференции по матричной изоляции в США, которая произошла в 1995 году. Именно тогда научный мир впервые узнал о существовании новых …
… в воде (3,29 см3 в 100 г воды при 20°C). Еще лучше растворяется аргон во многих органических жидкостях. Зато он практически нерастворим в металлах и не диффундирует сквозь них. Как все инертные газы, аргон диамагнитен. Это значит, что его магнитная восприимчивость отрицательна, он оказывает большее противодействие магнитным силовым линиям, чем пустота. Это свойство аргона (как и многие другие) …
… сварки являются невысокая производительность при использовании ручного варианта. Применение же автоматической сварки не всегда возможно для коротких и разноориентированных швов. 5. Технология ручной сварки неплавящимся электродом в инертных газах Аргонная сварка может быть ручной, когда горелка и присадочный пруток находятся в руках сварщика, и автоматической, когда горелка и …
… СЭУ. Обоснование актуальности выполняемой разработки. Анализ специальной литературы, патентный поиск. Расчет элементов системы инертных газов. Составить схему СИГ. Выполнить чертеж общего вида скруббера для СИГ. Выводы и предложения по результатам разработки. РАЗРАБОТКА ТЕХНОЛОГИИ МОНТАЖА (ИЗГОТОВЛЕНИЯ, СБОРКИ ИЛИ ИСПЫТАНИЯ) ЭЛЕМЕНТА СЭУ.Разработка технологического …
Как сделать аргонную сварку своими руками из инвертора
Аргонная сварка является незаменимым методом, с помощью которого можно создавать неразъемные соединения изделий из цветных металлов, титана, нержавеющей стали и других сплавов. К тому же, данный вид сварки отличается хорошим качеством шва и высокой производительностью. Универсальные возможности аргоновой сварки привлекают и домашних мастеров. Но данное оборудование имеет высокую стоимость, и для домашнего использования практически не покупается. Поэтому все больше мастеров начинают задумываться о изготовлении агрегата аргонной сварки своими руками.
Технология и применение аргонной сварки
Аргоновая сварка немного напоминает обыкновенную дуговую, но для защиты сварочной ванны в ней используется защитный газ — аргон. Данный инертный газ имеет ряд присущих только ему свойств.
- Поскольку аргон тяжелее воздуха на 38%, он хорошо проникает в сварочную ванну и защищает ее от газов, находящихся в атмосфере. Благодаря этому сварочный шов получается без образования оксидной пленки, что улучшает качество соединения.
- Аргон присутствует в воздухе, поэтому он является побочным продуктом, образующимся при получении кислорода и азота из атмосферы, и является самым недорогим среди защитных газов для сварки.
Процесс сварки в среде аргона происходит по следующему принципу. Буквально за 1 секунду до розжига дуги в горелку подается аргон. Сварщик подносит электрод к детали, приготовленной для соединения, и нажимает кнопку включения. Но поскольку для розжига дуги в среде защитного газа требуется его высокая ионизация, то в работу вступает осциллятор.
Осциллятор — это прибор, вырабатывающий высокочастотные и высоковольтные импульсы, способные ионизировать газ и зажечь дугу между электродом и заготовкой.
После розжига дуги в место соединения деталей подается присадочная проволока вручную или в автоматическом режиме. Детали свариваются за счет плавления присадки, металл которой попадает на расплавленные кромки соединяемых заготовок.
Традиционно под аргоновой сваркой подразумевают соединение металлов с помощью неплавящегося вольфрамового электрода, создающего дугу, и присадки в виде металлического прутка или проволоки. Данный тип сварки имеет международное обозначение “TIG”.
Применяется аргонная сварка в следующих сферах.
- Каркасное строительство. Сварные швы способны выдерживать постоянные нагрузки.
- Стыковка труб как стальных, так и из цветных металлов, в том числе труб из различных сплавов.
- Соединение разнородных металлов.
- Сращивание практически любых металлов между собой: титана, меди, алюминия, нержавейки, бронзы, латуни, чугуна и т.д. Особенно это важно для автомобилестроения.
- Изготовление декоративных и ювелирных изделий.
Элементы для сборки самодельного аппарата
Чтобы собрать оборудование для аргоновой сварки, потребуются следующие элементы:
- сварочный аппарат постоянного тока или инверторного типа;
- осциллятор;
- блок защиты инвертора;
- горелка;
- баллон с аргоном;
- газовый редуктор;
- газовый шланг;
- сварочные кабели.
Источник тока
В качестве источника тока для TIG сварки можно взять обычный сварочный трансформатор и на его выходе приспособить диодный мост для выпрямления тока. Также можно использовать сварочный выпрямитель. Но для обоих типов аппаратов потребуется добавить еще и осциллятор, который будет способствовать бесконтактному розжигу дуги.
На просторах интернета можно прочитать, что проще всего сделать аргонную сварку из инвертора. Но здесь имеется несколько нюансов. Существуют инверторы, в которых уже встроена возможность для TIG сварки. В таком случае достаточно подсоединить к аппарату рукав с горелкой для аргоновой сварки, подсоединить шланг к баллону с аргоном, и агрегат готов к работе. Но сначала нужно переключить его в режим TIG и выставить необходимую силу тока.
Следует заметить, что в таких инверторах уже встроен осциллятор и необходимая защита.
Инверторы без встроенной функции TIG сварки использовать для этой цели не получится. Даже если к нему подключить внешний осциллятор, то инвертор просто сгорит. Чтобы этого не произошло, понадобится небольшая переделка инвертора, которая заключается в добавлении в его схему блока защиты. Данный блок можно собрать вместе с осциллятором на одной плате и поместить ее в отдельный корпус. Получится небольшая приставка к инвертору.
Осциллятор и блок защиты
Как уже говорилось выше, для сварочного инвертора потребуется специальная приставка для TIG сварки. Ее можно собрать своими руками по схеме, предоставленной ниже.
Данная схема включает блок защиты (расположен слева) и осциллятор. Последний можно приобрести в Китае или собрать самостоятельно. Как собирается приведенная выше схема, можно узнать, посмотрев это видео.
Горелка
Для аргоновой сварки используется специальная горелка, состоящая из керамического сопла и держателя вольфрамового электрода.
Также на горелке расположены кнопка пуска и вентиль для подачи газа. Горелку можно собрать из комплектующих, которых достаточно на китайских сайтах, или там же купить уже готовую (собранную).
Баллон с аргоном
В целях безопасности все баллоны с газом принято окрашивать в разные цвета и наносить на них надписи тоже различных цветов. Ниже приведен рисунок, на котором показаны все разновидности газовых баллонов с соответствующей их содержимому маркировкой и цветом.
Как видно из рисунка, для аргона используют баллоны черного цвета (с белой полосой) либо серого цвета (с зеленой полосой и надписью). Для TIG сварки применяют очищенный аргон. Поэтому понадобится приобрести баллон серого цвета с зеленой надписью “Аргон чистый”.
Совет! Для профессионального использования используются баллоны емкостью около 50 литров, имеющие большой вес. Но для бытового использования будет достаточно баллона на 10 литров, который можно перемещать самостоятельно.
Редуктор
Поскольку газ в баллоне находится под большим давлением, то чтобы подать его на горелку, потребуется редуктор. Данный прибор показывает давление в баллоне и позволяет регулировать скорость потока газа по шлангу, ведущему к горелке.
Редуктор должен подбираться строго под определенный газ, то есть в данном случае – под аргон. Обычно прибор имеет такой же цвет, как и баллон с газом.
Шланг и сварочные кабели
Если собирать рукав для аргоновой сварки самостоятельно, то он получится толстым и плохо гнущимся, поскольку в него нужно поместить электрический кабель и газовый шланг. К тому же, потребуется отдельно приобретать разъемы для подключения к горелке и к инвертору (если использовать инвертор с возможностью TIG сварки). Готовый рукав для аргоновой сварки можно купить там же, где и горелку.
Алгоритм сборки сварочного аппарата
Сборка оборудования для аргоновой сварки из инвертора достаточно проста.
- Подключите к инвертору защитный блок с осциллятором согласно схеме, приведенной выше.
- Кабель массы необходимо подсоединить к клемме осциллятора со знаком “+“. Кабель, который идет к горелке, подключается к клемме со знаком “-”. Для сварки алюминия кабели подключаются наоборот.
- Подсоедините к рукаву с кабелем и газовым шлангом горелку.
- Прикрутите к баллону с аргоном редуктор.
- Газовый шланг необходимо подсоединить к редуктору, установленному на баллоне с аргоном.
- Подключите инвертор к сети 220 В, а осциллятор к блоку питания на 6 В.
После этого собранный своими руками сварочный аппарат TIG будет готов к работе. Но предварительно его следует правильно настроить.
Настройка готового оборудования
Самодельная установка для аргоновой сварки требует следующих настроек.
- Заточите вольфрамовый электрод на точиле, чтобы он стал похож на иглу. Делается это для того, чтобы дуга концентрировалась на конце иглы и не “гуляла” в разные стороны.
- Возьмите горелку и установите в нее вольфрамовый электрод. Диаметр электрода должен соответствовать цанге, в которой он закрепляется.
- Откройте вентиль на горелке и отрегулируйте необходимую скорость потока аргона с помощью редуктора (будет достаточно расхода 12-15 л/мин.), после чего снова закройте вентиль на горелке.
- Включите осциллятор и поднесите горелку с электродом к металлу, к которому подключен кабель массы.
- При нажатии кнопки включения между металлом и электродом на расстоянии около 0,5 мм должна появиться дуга.
- Включите подачу газа и снова нажмите на кнопку. В этом случае дуга должна поджигаться уже на расстоянии 10 мм и более.
После проведения вышеописанных несложных настроек можно сказать, что аппарат c функцией TIG полностью готов к работе.
Техника безопасности при дуговой сварке в аргоне
Применяя в работе сжиженные газы, необходимо строго соблюдать правила техники безопасности. Назовем основные ее требования при использовании аргона:
- не положено проводить сварку вблизи легковоспламеняющихся веществ;
- необходимо удалить все посторонние предметы;
- следует использовать только сертифицированные материалы и исправное оборудование;
- перед началом работ надо пройти предварительный инструктаж, получить базовые теоретические знания;
- в ходе работы обязательно использовать маску либо защитные очки, желательно «хамелеоны».
Несмотря на то, что аргон достаточно безвреден для человеческого организма, его лучше не вдыхать, так как он более легкий, чем кислород, а потому просто выталкивает его. После попадания аргона в легкие человек начнет задыхаться. Осуществлять сварку следует в помещении, имеющем хорошую естественную вентиляцию, в противном случае для моментального удаления продуктов сгорания надо позаботиться о качественной постоянной вентиляции.