Что такое никелирование?
Никелирование — процесс нанесения тонкого слоя металлического никеля на изделие для придания ему необходимых свойств.
Покрытия широко применяются в качестве подслоя при покрытии драгоценными металлами, а также для улучшения электропроводности, повышения твердости, защиты в щелочных средах и придания высокодекоративного внешнего вида.
Никель — серебристо-белый металл с сильным блеском. Атомная масса никеля 58,69 г/моль, плотность 8,9 г/см3. Имеет электрохимический эквивалент 1,095 г/(А*ч), его стандартный потенциал равен -0,25 В.
Никелевые покрытия легко пассивируются на воздухе и под действием сильных окислителей. Благодаря этому покрытие обладает высокой коррозионной стойкостью. При толщине покрытия 125 мкм основной металл уже предохранен от воздействия промышленных газов и растворов. В менее агрессивных средах достаточно 50-100 мкм. Никель полностью устойчив в щелочах и органических кислотах окислительного характера.
| Обозначение | Н. б — блестящее Н — матовое Nickel coating — анл. обозначение |
| Толщина | 6-50мкм (возможна и большая толщина) |
| Микротвердость | 3420-6900 МПа |
| Удельное электрическое сопротивление при 18оC | 7,23-10-8 Ом⋅м. |
| Допустимая рабочая температура | 650оC |
| Коэффициент светоотражения | до 75% |
В гальванической паре «никель-сталь» никель является катодным покрытием и, следовательно, может обеспечивать защиту только при условии отсутствия оголенных мест и пор. Поэтому необходимо получать покрытия с минимальной пористостью. В паре никель-медь никель является анодом.
Твердость никеля, полученного из электролитов без органических добавок, к которым относятся блескообразователи, смачиватели и выравнивающие добавки, обычно колеблется в пределах 3000-4000 МПа. При введении добавок твердость повышается до 6000-7000 МПа. Прочность на разрыв соответственно изменяется от 60 до 175 кгс/мм2.
Покрытия имеют пониженную пластичность, но после отжига при 900о С их пластические свойства значительно улучшаются.
Имеются сведения о возможности применения покрытий в оборудовании, связанном с переработкой молока.
На рисунке 1 приведена микроструктура поверхности матового покрытия на изделии.
Рисунок 1 — Микроструктура поверхности матового никелевого покрытия.
Как увеличить срок службы покрытия?
Полученное покрытие имеет пористую структуру. Поэтому металл изделия подвержен коррозии. Чтобы снизить риск ее возникновения, слой никеля покрывают смазочными составами. После их нанесения предмет погружают в емкость с рыбьим жиром. Спустя 24 часа, его излишки убирают при помощи растворителя.
Если изделие имеет крупные габариты, и погрузить его в емкость невозможно, то его поверхность просто натирают рыбьим жиром. Данную процедуру потребуется проводить дважды, с промежутком времени около 12 часов. Через 48 часов после обработки остатки жира нужно удалить.
Никелирование защищает металл от коррозии
Выполнить никелирование стали в домашних условиях можно двумя способами. Данный процесс является несложным, но требует тщательной подготовки и предельной аккуратности при выполнении. Необходимо приобрести качественные компоненты для приготовления раствора, заранее подготовить рабочую зону, емкости, инструменты и устройства.
В процессе работы важно соблюдать меры безопасности: защитить глаза и кожные покровы от попадания химических веществ, обеспечить достаточную вентиляцию помещения, предотвратить возможность воспламенения смеси и электрической установки.
Видео по теме: Химическая металлизация — никелирование
Полезные статьи
Процесс хромирования металлических изделий в домашних условиях
Травление нержавеющей стали в домашних условиях
Технология выполнения цинкования в домашних условиях
Электролиты для нанесения.
Для никелирования применяют сульфатные, хлоридные, сульфаминовые, борфторидные, щавелевокислые и другие электролиты, в которых никель находится в виде двухвалентного катиона. Разработано большое количество составов и режимов осаждения, позволяющих получать осадки никеля с различными физико-химическими свойствами.
Чаще всего используют сульфатный электролит Уоттса, так как вещества, которые в него входят, наиболее доступны, он прост в приготовлении и обслуживании.
Основным компонентом сульфатного электролита является сульфат никеля NiSO4•7H2O. Технический сульфат никеля марки СН-1 представляет собой кристаллы зеленого цвета. Растворимость без подогрева достигает 300 г/л.
Кроме никелевых солей, являющихся источниками катионов никеля, в состав электролита входят компоненты, предназначенные для того, чтобы повысить электропроводность, стабилизировать кислотность (буфферные добавки), улучшить растворимость анодов (хлориды), придать блеск осадкам, предотвратить различные дефекты, встречающиеся при никелировании.
Если концентрация NiSO4•7H2O не превышает 300 г/л, в электролит для увеличения электропроводности иногда вводят Na2SO4•10H2O и MgSO4•7H2O. Сульфат натрия обладает значительно большей электропроводностью, однако магний включается в никелевые покрытия, при этом они становятся более мягкими и светлыми.
В качестве буферного соединения наиболее широко применяется борная кислота. Борная кислота регулирует рН не только в общем объеме электролита, но и в прикатодном слое, у которого вследствие разряда и выделения водорода непрерывно повышается уровень рН. При рН>4 осаждение происходит через пленку образующегося гидроксида никеля. Для электролитов с низким значением рН более эффективными являются добавки фторидных соединений.
Электролитическое никелирование
Суть технологии электролитического никелирования металлических деталей, имеющей и другое название – «гальваническое никелирование», можно рассмотреть на примере того, как выполняется омеднение поверхности изделия из металла. Такую процедуру можно проводить как с применением электролитического раствора, так и без него.
Деталь, которая будет в дальнейшем обрабатываться в электролитическом растворе, подвергается тщательной обработке, для чего с ее поверхности при помощи наждачной бумаги удаляют оксидную пленку. Затем обрабатываемое изделие промывается в теплой воде и обрабатывается содовым раствором, после чего снова промывается водой.
Крупные детали лучше очищать пескоструйным аппаратом
Сам процесс никелирования выполняется в стеклянной емкости, в которую заливается водный раствор (электролит). В составе такого раствора содержится 20% медного купороса и 2% серной кислоты. Обрабатываемую деталь, на поверхность которой необходимо нанести тонкий слой меди, в растворе электролита помещают между двумя анодами из меди. Чтобы запустить процесс омеднения, на медные аноды и обрабатываемую деталь необходимо подать электрический ток, величину которого рассчитывают, исходя из показателя 10–15 мА на один квадратный сантиметр площади детали. Тонкий слой меди на поверхности изделия появляется уже через полчаса его нахождения в растворе электролита, причем такой слой будет тем толще, чем дольше будет протекать процесс.
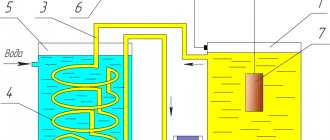
Схема установки для электролитического никелирования
Нанести медный слой на поверхность изделия можно и по другой технологии. Для этого необходимо изготовить кисточку из меди (можно использовать многожильный провод, предварительно сняв с него изоляционный слой). Такую кисточку, сделанную своими руками, надо зафиксировать на деревянной палочке, которая будет служить ручкой.
Изделие, поверхность которого предварительно зачищают и обезжиривают, помещают в емкость из диэлектрического материала и заливают электролитом, в качестве которого можно использовать насыщенный водный раствор медного купороса. Самодельную кисточку подключают к плюсовому контакту источника электрического тока, а обрабатываемую деталь – к его минусу. После этого приступают к процедуре омеднения. Заключается она в том, что кисточкой, которую предварительно обмакивают в электролит, проводят над поверхностью изделия, не прикасаясь к ней. Наносить покрытие, применяя такую методику, можно в несколько слоев, что позволит сформировать на поверхности изделия слой меди, на котором практически отсутствуют поры.
Схема простого приспособления для нанесения покрытия
Электролитическое никелирование выполняется по схожей технологии: при его осуществлении тоже используется раствор электролита. Так же, как и в случае с омеднением, обрабатываемое изделие располагают между двумя анодами, только в данном случае они изготовлены из никеля. Аноды, помещенные в раствор для никелирования, подключаются к плюсовому контакту источника тока, а изделие, подвешенное между ними на металлической проволоке, – к минусовому.
Для осуществления никелирования, в том числе и выполняемого своими руками, используются электролитические растворы двух основных типов:
- водный раствор, включающий в свой состав сернокислый никель, натрий и магний (14:5:3), 2% борной кислоты, 0,5% поваренной соли;
- раствор на основе нейтральной воды, содержащий в своем составе 30% сульфата никеля, 4% хлорида никеля, 3% борной кислоты.
Электролит блестящего никелирования с добавкой органических блескообразователей (натриевых солей)
Выравнивающий электролит блестящего никелирования. Подходит для поверхностей с низким классом очистки
Чтобы приготовить электролитический раствор, сухую смесь из вышеуказанных элементов заливают одним литром нейтральной воды и тщательно перемешивают. Если в полученном растворе образовался осадок, от него избавляются. Только после этого раствор можно использовать для выполнения никелирования.
Обработка по данной технологии обычно длится полчаса, при этом используют источник тока с напряжением 5,8–6 В. Результатом является поверхность, покрытая неравномерным матовым цветом серого цвета. Чтобы она стала красивой и блестящей, необходимо ее зачистить и выполнить ее полировку. Следует иметь в виду, что такая технология не может быть использована для деталей, отличающихся высокой шероховатостью поверхности или имеющих узкие и глубокие отверстия. В таких случаях покрытие поверхности металлического изделия слоем никеля следует выполнять по химической технологии, которую также называют чернением.
Электролит для осаждения черного никеля
Суть технологической операции чернения заключается в том, что на поверхность изделия сначала наносится промежуточное покрытие, основой которого может быть цинк или никель, а на верхней части такого покрытия формируется слой черного никеля толщиной не более 2 мкм. Покрытие никелем, выполненное по технологии чернения, смотрится очень красиво и обеспечивает надежную защиту металла от негативного воздействия различных факторов внешней среды.
В отдельных случаях металлическое изделие одновременно подвергают сразу двум технологическим операциям, таким как никелирование и хромирование.
Катодные процессы при электроосаждении.
Электроосаждение металлов железной группы из растворов простых солей имеет ряд особенностей по сравнению с другими металлами. Разряд ионов металла протекает при высокой катодной поляризации и низком перенапряжении водорода, что создает определенные трудности, так как на катоде одновременно с металлом выделяется водород:
Ni2+ + 2e- → Ni0
2H+ + 2e- → H2
Большой вклад в исследование кинетики электроосаждения никеля внес Ферстер. Им и его сотрудниками было установлено, что поляризационные кривые осаждения металлов подгруппы железа имеют логарифмический характер. При этом наблюдается значительная катодная поляризация уже на малых плотностях тока.
Изначально считалось, что потенциалы осаждения никеля находятся в зависимости от рН среды — при снижении рН с 5 до 2 потенциалы должны были становиться все более отрицательными.
Гластон опроверг эти предположения. Он установил, что в буферированном растворе сернокислого никеля поляризационные кривые всегда медленно поднимаются до -0,57 В, а затем резко идут вверх. Экспериментально при 15о С из 1Н раствора сульфата никеля металл начинает выделяться на медном катоде именно при -0,57 В. При других температурах потенциал выделения никеля смещается в более отрицательную область. По мнению Гластона рН не влияет на потенциал выделения никеля. При уменьшении рН с 5 наблюдается лишь смещение резкого подъема поляризационной кривой (начала выделения металла) к более высоким значениям плотности тока. Данный факт оказался аналогичным для железа и кобальта.
Таким образом, Гластон заключил, что при осаждении никеля процесс не контролируется замедленным разрядом. По его мнению значительная катодная поляризация наблюдается лишь до начала выделения металла, в дальнейшем же поляризация незначительно превышает ту, которая имеет место при осаждении свинца или меди.
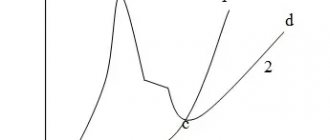
Все вышесказанное иллюстрируется на поляризационных кривых на рисунке 2.
Рисунок 2 — Поляризационные кривые в 1Н растворе сульфата никеля при различных рН. Температура 15о С: 1 — 0,5Н серная кислота; 2 — рН = 2,8; 3 — рН = 4; 4 — рН = 5; 5 — рН = 6.
Повышение температуры закономерно уменьшает поляризацию. На кривых это выражается в более крутом ходе (рисунок 3).
Рисунок 3 — Поляризационные кривые в 1Н растворе сульфата никеля. Температура 95о С: 1 — рН = 2,8; 2 — рН = 4; 3 — рН = 5; 4 — рН = 6; 5 — рН = 6 (без никеля).
Видно, что в растворах катодный потенциал после достижения величины -0,57 В изменяется в дальнейшем с ростом плотности тока незначительно. В то же время, при отсутствии в растворе ионов никеля никакого излома поляризационной кривой не наблюдается. При замене сульфатов на ацетаты, хлориды или нитраты, потенциал излома поляризационной кривой остается неизменным (-0,57 В при 15о С). Изменение концентрации никеля в растворе на 0,01Н приводило к смещению потенциала на -0,06В. Изменение температуры до 55о С смещало потенциал излома до -0,43 В, а еще большее повышение температуры (до 95о С) смещало потенциал излома в еще более положительную область (до -0,29 В). Таким образом, по Гластону, при температурах 15о, 55о, 95о С катодная поляризация поляризация в начальный момент выделения никеля составляет 0,33, 0,19 и 0,06 В соответственно и величина рН не оказывает влияния на потенциал выделения металла. Однако, при снижении рН значительно снижается плотность тока, при которой достигается этот потенциал (что противоречит теории Кольшютера).
Гластон, кроме исследования поляризации при осаждении никеля, первым заметил, что электролитический никель осаждается в очень неравновесной форме, отличной от металлургического.
Ферстер обратил внимание, что Гластном была допущена существенная ошибка — значения потенциалов для данной плотности тока фиксировались на основании кратковременного наблюдения, в течение которого эти потенциалы недостаточно стабилизировались. Кроме этого, не уделялось достаточного внимания защите катодного пространства от доступа кислорода. Устранив эти недостатки Ферстеру удалось получить никель при 16о С из 1Н раствора хлорида никеля при потенциале -0,42 В. В сернокислых растворах никель начинал осаждаться при потенциале -0,50 В, т.е. на 0,07В менее отрицательном, чем об этом указывал Гластон. Природа аниона по Ферстеру оказывала влияние на потенциал выделения никеля — в сернокислых растворах он оказывался отрицательнее.
Дальнейшие исследования, выполненные Томпсоном в стандартной никелевой ванне в присутствии различных посторонних солей, показали зависимость хода поляризационных кривых от состава вводимых слей (рисунок 4).
Рисунок 4 — Поляризационные кривые в нормальных никелевых растворах в присутствии других солей: 1 — стандартная ванна 1Н сульфат никеля, 0,25Н хлорид аммония, 0,25Н борная кислота; 2 — стандартная ванна при 5о С; стандартная ванна + 0,25Н фторид натрия; 4 — стандартная ванна + 0,50Н натрий лимоннокислый; 5 — стандартная ванна + 1Н натрий лимоннокислый; 6 — стандартная ванна + 1Н виннокислый натрий; 7 — стандартная ванна + 1Н уксуснокислый натрий; 8 — стандартная ванна + 1Н NaH2PO4.
Катодная поляризация оказывает заметное влияние на структуру электролитического осадка и на равномерность распределения металла на катодной поверхности. С этой точки зрения катодную поляризацию нужно поднимать настолько, насколько это возможно. В некоторых случаях без заметной катодной поляризации процесс вообще не идет.
Виды никелирования
Никелирование в простых домашних условиях проводят двумя способами:
- электролитическим;
- химическим.
Выбор способа зависит от структуры и формы материала.
Электролитическое никелирование
При электролитическом способе используются вещества, частично или полностью состоящие из ионов и обладающие ионной проводимостью. Никелевое покрытие наносят за счет электрохимических свойств этих веществ. Наибольшее распространение получили электролиты сернокислого натрия и хрома.
В зависимости от степени отражения покрытия различают никелирование:
Функции электролитического никелирования
- матовое;
- блестящее.
Для нанесения матового покрытия используются электролиты без добавок. Изделия с матовым оттенком не имеют металлического блеска.
Блестящее никелирование получают путем добавления в электролит специальных блескообразователей на основе хлорамина, пропаргилового спирта, бепзосульфамида и других окислителей.
Наилучшая защита никелевого покрытия достигается при минимальной пористости защитного слоя. С этой целью производят его омеднение либо используют многослойную структуру материала.
К сведению. При одинаковой толщине многослойные покрытия в несколько раз надёжнее однослойных материалов.
Наиболее распространёнными примерами многослойных материалов являются медно-никелево-хромовые покрытия.
Основными недостатками электролитического никелирования являются:
- высокая степень пористости;
- неравномерность осаждения никеля;
- сложность обработки поверхностей со сложной формой.
Химическое никелирование
Основой метода служит свойство ионов никеля восстанавливаться в жидкой среде. С этой целью используют гипофосфит натрия или другие химические реактивы. Химический способ позволяет обрабатывать изделия со сложной формой поверхности.
Недостатком способа является относительная дороговизна сухих реактивов, используемых для приготовления водных химических растворов.
Анодные процессы при электроосаждении.
Механизм растворения никелевых анодов схематично выражается уравнением реакции:
Ni0 → Ni2+ + 2e-
Никелевые аноды склонны к явлению пассивации. Пассивация анодов приводит к нарушению состава электролита (никель будет израбатываться, а кислотность — расти). Пассивное состояние анодов поддерживается малорастворимыми солями никеля, образующимися на их поверхности при превышении допустимой анодной плотности тока. С момента начала пассивации анод становится все более электроположительным и начинается реакция:
Ni — 3ē → Ni3+
Ионы трехвалентного никеля гидролизуются:
Ni3+ + 3OH- → Ni(OH)3 Ni(OH)3 → Ni2O3 + H2O
Образующийся диэлектрик Ni2O3 способствует еще более глубокой пассивации. Плотность тока пассивации зависит от концентрации сульфат и хлорид ионов. Полная пассивация приводит к выделению на аноде кислорода и хлора. Более подробно анодный процесс при никелировании разобран в статье.
Влияние режима электролиза на качество покрытия и выход по току.
На свойства никелевых покрытий сильно влияют:
- Состав ванны;
- Температура;
- рН;
- Плотность тока;
- Посторонние примеси.
5.1 Влияние состава электролита на свойства никелевых покрытий.
Все электролиты никелирования делятся на следующие основные группы:
- Сульфатный (Уоттса);
- Сульфаминовый;
- Фторборатный;
- Хлоридный;
- Кремнефтористоводородный.
На практике чаще всего применяют первые два. Остальные электролиты предназначены для получения матового никеля на высоких плотностях тока, со 100% выходом по току, либо для покрытия изделий из алюминия непосредственно электролизом. Все они распространены значительно меньше.
Из электролита Уоттса можно получать как матовые, так и блестящие покрытия. В настоящее время около 80 % всех никелевых покрытий получают блестящими. Из сульфаминового электролита с определенными добавками также можно получать блестящие покрытия, однако чаще его используют для получения матового пластичного никеля с низкими внутренними напряжениями для гальванопластики или металлизации диэлектриков.
Введение блескообразующих и выравнивающих добавок в электролит позволяет получать сразу из ванны гладкие и блестящие покрытия. Блестящее никелирование по сравнению с матовым имеет ряд преимуществ:
- отпадает трудоемкая операция механического полирования;
- сокращается расход металла, так как при механическом глянцевании на углах, кромках и ребрах;
- сокращается число технологических операций и создаются условия для автоматизации всего технологического цикла;
- интенсифицируется процесс осаждения за счет применения более высоких плотностей тока.
Основными недостатками блестящих покрытий по сравнению с матовыми являются сильное наводороживание, наличие повышенных внутренних напряжений и большое количество примесей, ухудшающих механические свойства.
Выход по току в сульфатном электролите увеличивается при повышении концентрации ионов никеля в электролите.
Влияние концентрации хлоридов на физико-механические свойства никелевых покрытий приведено на рисунке 5.
Рисунок 5 — Влияние концентрации хлоридов на относительное удлинение (elongation), внутреннее напряжение (internal stress), твердость (hardness) и предел прочности при растяжении (tensile strength) электроосажденного никеля из электролита Уоттса растворов при рН=3.0, температуре 55о С и плотности тока 5А/дм2.
Рассмотрим подробнее влияние добавок в электролит никелирования. Все добавки к электролиту никелирования делятся на блескообразующие, антипиттинговые (смачиватели), выравнивающие, электропроводящие. Они могут быть как органического, так и неорганического происхождения. Многие добавки сегодня не применяются как устаревшие (фталимид, формалин, хлорамин Б и т.п.).
5.1.1 Блескообразователи в электролите никелирования.
По одной из принятых классификаций блескообразующие добавки делятся на два класса:
- Слабые блескообразователи (I класс)
позволяют получать блестящие покрытия только на полированной поверхности, их блеск обратно пропорционален толщине. Они не влияют на катодную поляризацию. К ним относятся уротропин, сахарин, хлорамин Б, динатриевая соль нафталин-1,5-дисульфокислоты и другие. - Сильные блескообразователи (II класс)
способствуют получению блеска не только на полированной, но и на матовой поверхности, причем блеск не зависит от толщины покрытий. Они повышают катодную поляризацию и выравнивают микрорельеф, но ухудшают механические свойства осадков. К ним относятся кумарин, тиомочевина, 1,4-бутиндиол и другие.
Установлено, что блескообразователи второго класса, особенно имеющие двойные и тройные связи, при электролизе, как правило, гидрируются, а сульфогруппы блескообразователей первого класса восстанавливаются в конечном итоге до сульфида. Сульфид никеля, включаясь в осадок деактивирует каталитические центры никеля, замедляет параллельную реакцию разряда ионов водорода и процессы гидрирования блескообразователей, снижает наводораживание осадков. Этим объясняется выгодное использование одновременно сильного и слабого блескообразователя.
В настоящее время из блескообразователей наиболее часто применяются связки бутиндиол-сахарин ввиду того, что их поведение наиболее изучено, а также отработаны способы очистки электролита от продуктов разложения этих добавок.
5.1.2 Выравнивающе добавки.
Выравнивающие добавки, являясь ПАВ, блокируют выступающие части поверхности, в связи с чем осаждение происходит в микроуглублениях. К выравнивающим добавкам относится, например НИБ-3. Некоторые сильные блескообразователи также проявляют выравнивающее действие.
5.1.3 Смачивающие добавки.
Для никелирования характерно явление, называемое питтингом. Пузырьки газообразного водорода задерживаются на катодной поверхности и в этих местах становится невозможным дальнейший разряд никеля. Никель начинает разряжаться около пузырьков (рисунок 6). На покрытии возникают поры, и оно теряет защитные и декоративные свойства. Прилипанию пузырьков к катоду способствуют все вещества, которые увеличивают поверхностное натяжение. Сильное влияние могут оказать гидроксиды и органические соединения, а также продукты их разложения и даже пыль.
Рисунок 6 — Схема образования питтинга на никелевом покрытии.
Смачивающие добавки способствуют снижению поверхностного напряжения электролита, удалению грязи и пузырьков водорода с поверхности катода. К смачивающим добавкам относится изоприлнафталинсульфокислота, лаурилсульат натрия, моющее средство «Прогресс» и т.п.
Следует отметить, что большинство смачивающих и блескообразующих добавок являются сульфосоединениями. Во время электроосаждения в результате ряда превращений образуется сульфамид никеля. Содержание серы в осадках в больших количествах неблагоприятно сказывается на механических и коррозионных свойствах последних.
5.1.4 Электропроводящие добавки.
В основном для повышения электропроводности раствора и, соответственно, снижения напряжения на ванне и экономии электричества, в него вводят неорганические соли. Чаще всего это сульфат натрия, калия или магния. Однако, как будет сказано в пункте 2.6 эти добавки способствуют защелачиванию прикатодного слоя и ухудшению качества покрытия.
5.2 Влияние примесей в электролите на качество никелевого покрытия.
Никелевые осадки очень чувствительны к примесям, попадающим в электролит. Эти примеси делятся на неорганические и органические.
Неорганические примеси вызывают образование хрупких растрескивающихся осадков. В присутствии меди осадки получаются шероховатыми. Примеси цинка вызывают появление темных и даже черных полос. При наличии даже небольших примесей свинца образуется темное, чешуйчатое покрытие, которое легко осыпается. Из анионов наиболее вредным является NО3-, способствующий отслаиванию покрытий. Такие электролиты непригодны к эксплуатации. Аналогичным действием обладают хромовые кислоты.
Органические соединения вызывают образование питтинга, хрупкость и шероховатость покрытий. При загрязнении электролита органикой получить блестящие осадки невозможно.
5.3 Влияние температуры и перемешивания электролита никелирования на качество покрытий.
При увеличении температуры выход по току никеля возрастает, так как вследствие ускорения процесса диффузии снижается поляризация — потенциал осаждения никеля становится более положительным. Перенапряжение водорода при этом изменяется незначительно. Такое же влияние оказывает и перемешивание раствора.
Влияние температуры электролиза на физико-механические свойства никелевых покрытий приведено на рисунке 7.
Рисунок 7 — Зависимость относительного удлинения (elongation), предела прочности при растяжение (tensile strength) и твердости (hardness) никелевых покрытий от температуры электролита при рН = 3,0 и плотности тока 5 А/дм2.
5.4 Влияние рН электролита на качество покрытий.
Ионы никеля в электролите окружены оболочкой из дипольных молекул воды. В двойном электрическом слое часть молекул воды отрывается. Дегидратация последних молекул воды требует затрат энергии, что проявляется ростом перенапряжения, называемого химической поляризацией. При этом равновесный потенциал никеля даже при малых плотностях тока становится отрицательным.
При низких значениях рН<1-2 никель почти не осаждается и на катоде выделяется только водород. По мере увеличения рН потенциал выделения водорода становится более отрицательным и на катоде создаются условия для совместного выделения водорода и никеля. При этом доля выделения водорода тем меньше, чем выше рН. При высоких значениях рН вести осаждение никеля нельзя, так как начинается гидролиз. Продукты гидролиза (оксид и гидроксид никеля), внедряясь в покрытие, способствуют удержанию пузырьков водорода на поверхности катода, поэтому осажденный никель становится пористым, шероховатым и темным. При очень высоких значениях рН невооруженным глазом можно заметить на деталях зеленый осадок нерастворимых солей никеля.
Твердые, напряженные осадки получаются при рН >5,5, особенно при температуре ниже 20 °С. Повышение температуры приводит к некоторому снижению внутренних напряжений. Осадки, полученные при низких значениях рН, более мягки и эластичны.
Влияние рН на физико-механические свойства никелевых покрытий приведено на рисунке 8.
Рисунок 8 — Влияние рН на внутренние напряжения (internal stress), предел прочности при растяжении (tensile strength), пластичность (ductility) и твердость (hardness) никеля, электроосажденного из электролита Уоттса при температуре 55° C и плотности тока 5A/дм2.
5.5 Влияние плотности тока и его формы на качество покрытий.
Увеличение плотности тока в заданных пределах способствует уменьшению внутренних напряжений и увеличению блеска покрытий. Рабочий интервал плотностей тока тем шире, чем выше температура. Следует помнить, что при значительном завышении плотности тока покрытие из мелкокристаллического (компактного) переходит в дендритное (порошкообразное) из-за нарушения устойчивости плоского фронта роста осадка.
Влияние плотности тока на физико-механические свойства никелевых покрытий приведено на рисунке 9.
Рисунок 9 — Влияние плотности тока на внутренние напряжения (internal stress) и твердость (hardness) никеля, электроосажденного из электролита Уоттса при рН=3.0 и температуре 55° С.
Перспективным сегодня является применение нестационарных режимов электролиза и ультразвука. Никелирование с реверсированием тока и воздействием ультразвука проводят в сульфатных электролитах. Никель может пассивироваться при анодной поляризации, поэтому осаждение проводят короткими анодными импульсами или прерывистым током. Это приводит к активации никеля в процессе покрытия. Реверсирование и прерывание тока обеспечивает получение покрытий с незначительной пористостью, малыми внутренними напряжениями и высокими защитными свойствами.
Положительное влияние оказывает последовательное применение асимметричного и постоянного тока. Осаждение постоянным током позволяет повысить блеск и твердость никелевых покрытий.
Электроосаждение никеля импульсным током дает возможность получить зеркально-блестящие покрытия из обычных электролитов никелирования без применения блескообразующих добавок.
Наложение ультразвука, а также совместное применение ультразвука и реверсированного тока позволяют существенно интенсифицировать процесс электроосаждения. При этом повышается допустимая плотность тока осаждения, из электролитов обычного состава получаются светлые, прочные и практически беспористые осадки при весьма малых толщинах покрытия, одновременно улучшается блеск покрытий, снижаются внутренние напряжения.
Для применения нестационарных режимов электролиза необходимо использовать выпрямители со специальными функциями.
5.6 Сравнение физико-механических свойств слоев никелевых покрытий, полученных в различных условиях из электролита Уоттса и сульфаматного раствора.
Рисунок 10 — Схематичная иллюстрация влияния вышеописанных параметров осаждения никеля из электролита Уоттса и сульфаматного раствора на физико-механические свойства покрытия.
Никелирование в домашних условиях: технология и способы никелирования
Процесс никелирования
Процедура никелирования подразумевает нанесение на поверхность изделия никелевого покрытия, которое, как правило, имеет толщину слоем 1-50 мкм. Никелевые покрытия могут быть матовыми черными или блестящими, но вне зависимости от этого, создают надежную и прочную защиту металла от агрессивных воздействий (щелочи, кислоты) и в условиях высоких температур.
Перед никелирования изделие необходимо подготовить. Этапы подготовки:
- деталь обрабатывают наждачкой для снятия оксидной пленки;
- обрабатывают щеткой;
- промывают под водой;
- обезжиривают в теплом содовом растворе;
- подвергают промывке еще раз.
Покрытия из никеля могут с течением времени утрачивать свой изначальный блеск, потому очень часто никелевый слой покрывают более стойким слоем хрома.
Никель, нанесенный на сталь, это катодное покрытие, которое защищает металл только механическим способом.
Слабая плотность защитного слоя способствует появлению коррозионных пор, где растворимым электродом является именно стальная часть.
В итоге под покрытием возникает коррозия, она разрушает стальную подложку и создает отслаивание никелевого слоя. Чтобы этого не допустить металл всегда необходимо обрабатывать толстым слоем никеля.
Покрытия из никеля наносятся на:
- медь;
- железо;
- титан;
- вольфрам и другие металлы.
Нельзя обрабатывать при помощи никелирования такие металлы, как:
- кадмий;
- свинец;
- свинец;
- олово;
- висмут;
- сурьму.
При никелировании деталей из стали необходимо делать подслой меди.
Никелевые покрытия применяют в различных сферах промышленности для специальных, декоративно-защитных целей, а также используют в роли подслоя.
Технику никелирования применяют для восстановления изношенных деталей и запчастей автомобилей, покрытия медицинского инструмента, химической аппаратуры, предметов домашнего обихода, измерительных инструментов, деталей, которые подвергаются небольшим нагрузкам в условии действия крепких щелочей или сухого трения.
Разновидности никелирования
На практике существует два вида никелирования:
- Химическое;
- Электролитическое.
Первый вариант является четь дороже электролитического, но может обеспечить возможность создания равномерного покрытия по толщине и качеству на любых участках изделия, если создано условие доступа раствора к ним.
Электролитическое покрытие никелем в домашних условиях
Для чего в домашних условиях надо подготовить электролит. Необходимо 3,5 гр. хлорида никеля, 30 гр. сульфата никеля и 3 гр. борной кислоты на 100 мл. воды, этот электролит перелейте в емкость. Для никелирования меди или стали будут необходимы никелевые аноды, которые необходимо погрузить в электролит.
Деталь подвешивается на проволочке между никелевыми электродами. Проволочки, которые от никелевых пластинок, нужно соединить вместе. Детали подсоединяют к отрицательному полюсу источнику напряжения, а проволочки – к положительному. После необходимо подключить реостат в цепь и миллиамперметр для регулировки напряжения. Понадобится источник постоянного тока, с напряжением не более 6 Вольт.
Влияние условий эксплуатации покрытий на их свойства.
Рисунок 11 — Влияние температуры эксплуатации на предел прочности при растяжении (tensile strength), предел текучести (yield strength) и относительное удлинение (elongation) электроосажденного никеля.
Рисунок 12 — Влияние толщины осадка и внутренних напряжений на 100-миллионный цикл усталостной долговечности никелированной нержавеющей стали AISI 4340.