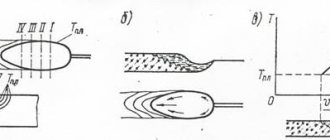
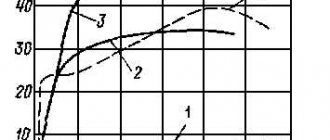
Нахождение в природе
Нахождение в природе свободного молибдена не зафиксировано. Зато выявлено два десятка минералов на его основе. Самые примечательные: молибденит, молибдит, вульфенит.
Молибденит из Австралии
В земной коре элемент распределен равномерно. Также обнаружен в реках, морях, ископаемых органического происхождения (зола растений, уголь, нефть). Однако суммарно массовое содержание металла – сотые доли процента.
Мировые запасы молибдена оцениваются в 11,5 млн. тонн.
Крупными месторождениями располагают Австралия, обе Америки (США, Канада, Мексика, Чили). В Европе – Россия и Норвегия.
Добыча ведется закрытым либо карьерным способом.
Металл обнаружен в космосе. Его концентрации зашкаливают в системах с центральной звездой – красным (сверх)гигантом и нейтронной звездой внутри него.
Что такое барий
- Что такое барий Характеристика элемента
- Барий это
- Получение и использование
(Barium; от греч.тяжелый), Ва — хим. элемент II группы периодической системы элементов; ат. н. 56, ат. м. 137,34. Серебристо-белый металл. В соединениях проявляет степень окисления +2. Природный барий состоит из семи стабильных изотопов, среди к-рых преобладает изотоп 138Ва (71,66%). Барий в виде окиси открыл в 1774 швед, химик К. Шееле. Металлический барий получил в 1808 англ. химик Г. Дэви. Содержание бария в земной коре — 5 X 10 % В свободном состоянии в природе не встречается. Из минералов пром. значение имеют барит и менее распространенный витерит. Важнейшие неорганические соединения: окись BaO, перекись BaO2 , гидроокись Ва (ОН)2,карбонат ВаС03, сульфат BaS04 и хлорид ВаСl2. Кристаллическая решетка Бария кубическая объемноцентрированная с периодом а = 5,019 А;плотность 3,76 г/см3; tпл 710° С; tкип 1637 -1640° С; температурный коэфф линейного расширения (т-ра 0 — 100° С) 1,9 · 10 град ; удельная теплоемкость 0,068 кал/г · град; удельное электрическое сопротивление 6 · 10-5 ом · см, твердость по Бринеллю 4,2, по шкале Мооса 2. По хим. св-вам сходен с кальцием, стронцием и радием. На воздухе быстро окисляется. При нагревании на воздухе легко воспламеняется и сгорает. Энергично разлагает воду. С водородом образует гидрид ВаН2. При нагревании соединяется непосредственно с азотом, серой и галогенами. Основным сырьем для получения бария и его соединений служит барит, к-рый восстанавливают углем в пламенных печах. Образующийся растворимый сульфид бария перерабатывают на др. соли металла. Металлический барий получают термическим восстановлением его окиси порошком алюминия при т-ре 1100— 1200° С Процесс ведут в электровакуумных аппаратах периодического действия, где последовательно проходят восстановление, отгонка, конденсация и отливка металла в слиток. Технический продукт содержит 96—98% металла. Двойной перегонкой в вакууме при т-ре 900° С содержание примесей снижают до 1 X 10—4%. Сплавы бария получают электролизом расплава смеси хлоридов. Практическое применение металлического бария невелико. Барий и его сплавы с магнием и алюминием используют для поглощения остаточных газов в технике высокого вакуума (см. Геттеры). Б. вводят в некоторые антифрикционные материалы. Сплавы свинец — барий вытесняют полиграфические сплавы свинец — сурьма. Сплавы бария с никелем применяют для изготовления электродов запальных свечей двигателей и в радиолампах. Сульфат BaS04 применяют как белый пигмент, а также в произ-ве линолеума и бумаги. Титанат BaTi03 — один из важнейших сегнетоэлектри-ческих материалов. Окись ВаО используют при изготовлении стекла, эмалей и термокатализаторов. Перекись Ва02 служит для получения перекиси водорода, для отбеливания тканей, ее используют также в качестве катализатора крекинг-процесса, как один из компонентов запальных смесей в алюмотермии и пиротехнике. Фторид BaF2 применяется при изготовлении эмалей и оптических стекол. Цирконат BaZr03 — высококачественный огнеупорный материал. Рентгеновское и радиоактивное излучение возбуждает желто-зеленую флуоресценцию комплексной соли Ва , на чем основано применение спец. экранов, покрытых этой солью. Соединения Б. хороню поглощают рентгеновские лучи и гамма-излучение, вследствие чего их вводят в состав защитных материалов в рентгеновских установках и ядерных реакторах. Окрашенные соли Б. являются пигментами: хромат ВаСrO4 — желтый, манганат ВаМnO4 — зеленый. Растворимые соли бария ядовиты.
Как был открыт
История открытия элемента начинается со второй половины 18 века.
Блестящий металл серебристо-белого цвета
Она написана тремя учеными:
- Шведский химик Карл Шееле получил оксид.
- Француз Пьер Гьельм выделил металл. Но его чистота была символической.
- Получение металла почти без «грязи» – заслуга патриарха европейских химиков шведа Йенса Берцелиуса. Случилось это на заре 19 века.
Через столетие началась эпоха расцвета металла.
Молибденовая сталь выплавлялась тоннами для нужд армий, воевавших на фронтах Первой мировой войны.
Позже разработали технологию получения металла методом порошковой металлургии.
У названия элемента древнегреческое происхождение: μόλυβδος означает «свинец».
Путаницу породил молибденит. Его получили первым, но блеском вещество копировало свинец.
По той же причине до 18 века молибденом именовали графит.
Виды бронзы
Оловянная
сплав меди с оловом
Оловянная бронза с трудом поддается ковке, прокатке, резке, заточке и штамповке и в основном пригодна исключительно для цельного литья. Небольшая осадка (не более 1%) позволяет использовать материал при создании особо точных изделий в художественном литье.
По желанию к сплаву могут добавить другие металлы.
- Цинк (не более 10%) повышает коррозионную стойкость сплава и используется для создания элементов кораблей и судов, которым придется часто контактировать с морской водой.
- Благодаря добавлению свинца и фосфора можно существенно улучшить антифрикционные свойства бронзы, также сплав легче обрабатывается давлением и резанием.
Безоловянные
В некоторых случаях применение олова недопустимо. В этом случае на помощь приходят другие металлы, добавление которых позволяет получить необходимые характеристики. И хотя оловянная бронза является эталоном и наиболее востребована, безоловянные бронзы не уступают ей.
Свинцовистая или свинцовая
Свинцовая бронза является прекрасным антифрикционным сплавом, хорошо сопротивляются давлению, обладает повышенной прочностью и тугоплавкостью. Ее применяют для изготовления подшипников, подвергающихся наибольшему давлению при работе.
Кремнецинковая
Бронзу используют при изготовлении пружин, подшипников, решеток, направляющих втулок, испарителей и сетей.
Бериллиевая
Бериллиевая бронза является наиболее твердой из всех видов. Она обладает повышенными антикоррозийными свойствами и жаропрочностью, устойчива при низких температурах, не дают искр при ударах и не магнитятся. Металл закаляют при 750Со — 790Со, состаривают — при 300Со — 325Со. В бериллиевую бронзу иногда добавляют никель, железо или кобальт, чтобы облегчить технологию закалки. Кроме того, никелем можно заменить бериллий.
Материал используют для создания пружин и пружинящих деталей, мембран, для деталей часов.
Алюминиевая
Алюминиевая бронза состоит из меди (95%) и алюминия (5%). Имеет приятный золотой цвет и блеск, выдерживает длительное воздействие агрессивной среды, например, кислот. Сплав обладает большей плотностью отливки, жаропрочностью и повышенной прочностью, хорошо переносит низкие температуры. Из недостатков стоит отметить более слабую коррозийную стойкость, более сильную усадку, а также сильное газопоглощение в жидком состоянии.
Бронзу используют для изготовления деталей автомобилей и в пороховом производстве, выплавляют шестеренки, втулки, монеты и медали.
Остальные металлы
Помимо указанных выше, в бронзе могут присутствовать и другие элементы. Никель и железо увеличивают температуру рекристаллизации и способствуют измельчению зерна. Хром и цирконий снижают электропроводность и повышают жаропрочность бронзы.
Физико-химические характеристики
Молибден наделен многими достоинствами:
- Упругость, практически нулевое расширение при нагреве, стойкость к жару, коррозии.
- Электропроводность выше железа.
- Механическая прочность выше только у вольфрама. Но под давлением молибден обрабатывается проще.
- Главное химическое свойство металла – устойчивость перед почти всеми щелочными растворами, агрессивными кислотами независимо от их концентрации и температуры.
Недостатки металла: хрупкость при сварке, незначительная пластичность.
| Свойства атома | |
| Название, символ, номер | Молибде́н / Molybdaenum (Mo), 42 |
| Атомная масса (молярная масса) | 95,96(2) а. е. м. (г/моль) |
| Электронная конфигурация | [Kr] 4d5 5s1 |
| Радиус атома | 139 пм |
| Химические свойства | |
| Ковалентный радиус | 130 пм |
| Радиус иона | (+6e) 62 (+4e) 70 пм |
| Электроотрицательность | 2,16 (шкала Полинга) |
| Электродный потенциал | −0,2 |
| Степени окисления | 6, 5, 4, 3, 2 |
| Энергия ионизации (первый электрон) | 684,8 (7,10) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 10,22 г/см³ |
| Температура плавления | 2623 °C |
| Температура кипения | 4885 K |
| Уд. теплота плавления | 28 кДж/моль |
| Уд. теплота испарения | ~590 кДж/моль |
| Молярная теплоёмкость | 23,93 Дж/(K·моль) |
| Молярный объём | 9,4 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая объёмноцентрированая |
| Параметры решётки | 3,147 Å |
| Температура Дебая | 450 K |
Отрицательные характеристики молибдена проявляются только при сверхнизких температурах или некорректном использовании.
Достоинства / недостатки
Достоинства:
имеет высокую точку плавления, а следовательно – жаропрочность; т.к. плотность данного металла (10200 кг/м³) почти в два раза меньше плотности вольфрама (19300 кг/м³), то сплавы на основе молибдена обладают значительно большей удельной прочностью (при температурах ниже 1370°С); имеет высокий модуль упругости; малый температурный коэффициент расширения; обладает хорошей термостойкостью; малое сечение захвата тепловых нейтронов; для молибдена характерна высокая коррозионная стойкость. Данный металл устойчив в большей части щелочных растворов, а также в серной, соляной и плавиковой кислотах при разных температурах и концентрациях.
Недостатки:
обладает небольшой окалийностью; высокая хрупкость сварных швов; малая пластичность при низких температурах; упрочнение нагартовкой можно использовать лишь до 700-800°С, при более высоких температурах происходит разупрочнение из-за возврата.
Марки и сплавы
Промышленностью используется молибден как чистый металл, с присадками и сплавы.
Номенклатура марок включает десятки позиций. Самых распространенных несколько:
| Марка | Характеристики |
| МЧ | Mo – присадки отсутствуют. |
| МЧВП | Mo – присадки отсутствуют, выплавлен в вакууме. |
| МРН | Mo – присадки отсутствуют, но есть примеси. |
| МК | Mo + присадка (щелочной кремний). |
| ЦМ | Mo + присадка (циркониевая либо титановая). |
| МВ | Сплав «молибден-вольфрам». |
| МР | Сплав «молибден-рений». |
Добавки Mo (менее процента) к конструкционным сталям кратно увеличивают их вязкость, прочность, противодействие коррозии.
Для повышения твердости металлом снабжают кобальтово-хромовые сплавы.
У сплавов «молибден + никель + кобальт + хром» повышается сопротивляемость кислотам и термовоздействию.
Получение молибдена
Сырье, из которого производится металлический молибден – молибденовые концентраты. В их составе данного элемента содержится около 50%. Также в них содержатся: сера ~ 30%, оксид кремния (до 9%) и около 20% прочих примесей.
Предварительно концентрат обжигают с целью дополнительного окисления. Процесс проводят в печах двух типов: многоподовых или кипящего слоя. Температура обжига 570 °С — 600 °С. В результате чего получается огарок — МоО3 и примеси.
На следующем этапе удаляют примеси для получения чистого оксида молибдена. Применяются два способа:
- Возгонка при температуре 950 °С — 1100 °С.
- Химическое выщелачивание. Суть способа в том, что при взаимодействии с аммиачной водой устраняются примеси меди и железа и получается карбид молибдена, который кристаллизуют выпаркой или нейтрализацией. Далее карбид нагревают и выдерживают при температуре до 500°С. На выходе – чистый оксид МоО3, в котором содержание примесей всего 0,05%.
Производство молибдена основано на восстановлении МоО3. Процесс проводят в два этапа:
- В трубчатой печи при температуре 550°С — 700°С в потоке сухого водорода происходит отделение атомов кислорода.
- Далее температура поднимается до 900°С — 1000°С и происходит окончательное восстановление. Полученный металл находится в виде порошка.
Для получения монолитного металла пользуются плавлением или спеканием порошка. Плавку используют, когда получают заготовки массой от 500 кг. Процесс производят в дуговых печах с охлаждаемым тигелем, в который подается расходуемый электрод из ранее спеченных штабиков.
Получение молибдена
Порошковое спекание – это прессование в атмосфере водорода при высоких значениях давления (2000-3000 атмосфер) и температуры (1000°С — 1200°С). Полученные штабики, подвергаются спеканию при высоких температурах равных 2200°С — 2400°С. В дальнейшем молибдену придается необходимая форма за счет обработки давлением – ковкой, прокаткой, протяжкой.
Широко в промышленности используется ферромолибден, в котором до 60-70% молибдена, а оставшееся — железо. Его получают путем введения в сталь молибденовых присадок. Сплав получают путем восстановления огарка силикатом железа с добавками стальной стружки и железистой руды.
Где используется
Тугоплавкость, многообразие и легкость обработки металла, другие физические и химические свойства определили сферы использования продуктов из него.
Металлургия
Главный потребитель сырья – металлургия. Ее продукция из молибдена – проволока, прутки, порошок, лист, штабик.
Порошок молибденовый
Это заготовки для ассортимента изделий, производимых почти всеми отраслями промышленности.
Другие отрасли
Львиную долю продукции из молибдена, сплавов металла забирают производители радио- и электрических ламп, радиоэлектроники.
Материала хватает и на другие цели:
- Пресс-формы, детали машин для литья сплавов под давлением.
- Электровакуумное производство (рентгеновские трубки).
- Положительный электрод источников тока на основе лития.
- Оболочки деталей ядерных реакторов.
- Нагреватели электропечей, функционирующих в жестких условиях.
- Внешний слой «носового» сегмента корпуса сверхзвуковых самолетов.
- Электроды для выплавки стекла.
- Катализ химических реакций.
- Лаки, краски для фарфора, текстиля, мехов.
Эта продукция создается на основе природных соединений и сплавов металла.
Новейшее направление применения молибдена – космическая техника.
Ассортимент: узлы ракетных (ионных, плазменных) двигателей; обшивка спускаемых аппаратов; теплообменники. Здесь свойства молибдена корректируют сплавы с ниобием и танталом.
Чистый кристаллический Mo используется как компонент зеркал для лазеров специального назначения.
Микродозы металла добавляют в сельхозудобрения.
Физические свойства
Использование молибдена зависит от его свойств и характеристик. Присущие физические свойства молибдена приведены ниже:
- тип металла — высокотемпературная плавка;
- молибденовый цвет – свинцовый;
- плотность молибдена — 10,2 г/cм3;
- плавление при температуре — 2615°С;
- закипание при температуре — 4700°С;
- проводимость тепла — 143 Вт/(м·К);
- тепловая емкость — 0,27 кдЖ/(кгК);
- энергия для плавления — 28000 Дж/моль;
- энергия для испарения — 590000 Дж/моль;
- линейное расширение, коэффициент — 6·10-6;
- электрическое сопротивление — 5,70 мкОм·см;
- расчетный объем — 9,4 см3/моль;
- усилие сдвига — 122·10·6 Па;
- твердость — 125 НВ;
- магнитная проницаемость -90·10-6.
Точению данный металл подвергается не часто, но обработка ведется стандартизованным инструментом.
Значение для человека
Влияние молибдена на живые организмы изучили к середине 20 века.
Выяснилось, что данный микроэлемент:
- Регулирует синтез аминокислот.
- Активирует антиоксиданты, включая аскорбиновую кислоту.
- Входит в состав ферментов, системы тканевого дыхания.
О Mo-дефиците в организме сигнализирует ослабление иммунитета (быстрая утомляемость, частая заболеваемость).
Токсична молибденовая пыль. Ее длительное вдыхание провоцирует заболевания крови, необратимое разрушение легких.
Жаропрочные
Для создания жаропрочных свойств в никелевый раствор добавляют титан, алюминий, молибден, вольфрам, ниобий, рений, рутений и стронций. Данному сплаву характерна длительная прочность, отличная технологичность и устойчивость к высоким температурам. Характеристики марок сплавов зависят от процента наличия определенного металла в составе.
Например, сплав марки Inconel 600 используют при создании деталей для газовых турбин. Выдерживают до 750°C, имеют высокую степень сопротивления окисления и усталости металла. А Inconel 718 подходит для создания рабочих лопаток в газовых турбинах двигателей, которые работают при температуре 800-850°C. После термической обработки сплав не чувствителен к надрезу.
Медно-никелевые сплавы классифицируются на две подгруппы:
- Конструкционные – к этой разновидности можно отнести мельхиор и нейзильбер. Чаще всего, за легируемые элементы принимаются железо и марганец. Самое распространённое соотношение это ~5-30% Ni, все остальное Cu.;
- Электротехнические – одними из представителями данной категории являются копель или константан. Отличительными особенностями является высокое электросопротивление и термоэлектродвижущая сила. Чаще всего, сплав состоит на ~60% из меди, все остальное предоставляется никелем, и другими легирующими частями.
Современная классификация нержавеющей стали
Нержавеющая сталь – это разновидность легированной стали, устойчивая к коррозии за счет содержания хрома. В присутствии кислорода образуется оксид хрома, который создает на поверхности стали инертную пленку, защищающую все изделие от неблагоприятных воздействий.
Не каждая марка нержавеющей стали демонстрирует устойчивость хромоксидной пленки к механическим и химическим повреждениям. Хотя пленка восстанавливается под воздействием кислорода, были разработаны специальные марки нержавейки для применения в агрессивных средах.
Первый условный тип разбиения на группы:
- Пищевая
- Жаропрочная сталь
- Кислотостойкая сталь
Второй тип классификации — по микроструктуре:
- Аустенитные (Austenitic)
— не магнитная сталь с основными составляющими 15-20% хрома и 5-15% никеля который увеличивает сопротивление коррозии. Она хорошо подвергается тепловой обработке и сварке. Именно аустенитная группа сталей наиболее широко используется в промышленности и в производстве элементов крепежа. - Мартенситные (Martensitic)
— значительно более твердые чем аустетнитные стали и могут быть магнитными. Они упрочняются, закалкой и отпуском подобно простым углеродистым сталям, и находят применение главным образом в изготовлении столовых приборов, режущих инструментов и общем машиностроении. Больше поддвержены коррозии. - Ферритные (Ferritic)
стали значительно более мягкие чем мартенситные по причине малого содержания углерода. Они также обладают магнитными свойствами.
Добыча
Залежи молибдена и его добыча по странам
| Страна | Залежи (тыс. т) | 2001 | 2002 | 2003 | 2004 | 2005 | 2006 | 2007 | 2014 |
| США | 2700 | 37,6 | 32,3 | 29,9 | 41,5 | 58,0 | 59,8 | 59,4 | 68,2 |
| Китай | 3000 | 28,2 | 30,33 | 32,22 | 29,0 | 40,0 | 43,94 | 46,0 | 103,0 |
| Чили | 1905 | 33,5 | 29,5 | 33,4 | 41,48 | 47,75 | 43,28 | 41,1 | 48,8 |
| Перу | 850 | 8,35 | 8,32 | 9,63 | 9,6 | 17,32 | 17,21 | 17,25 | 17,0 |
| Канада | 95 | 8,56 | 7,95 | 8,89 | 5,7 | 7,91 | 7,27 | 8,0 | 9,7 |
| Россия | 360 | 3,93 | 4,29 | 3,57 | 3,11 | 3,84 | 3,94 | 4,16 | 4,8 |
| Мексика | 135 | 5,52 | 3,43 | 3,52 | 3,7 | 4,25 | 2,52 | 4,0 | 14,4 |
| Армения | 635 | 3,4 | 3,6 | 3,5 | 3,0 | 2,75 | 3,0 | 3,0 | 7,1 |
| Иран | 120 | 2,6 | 2,4 | 2,4 | 1,5 | 2,0 | 2,0 | 2,5 | 4,0 |
| Монголия | 294 | 1,42 | 1,59 | 1,6 | 1,7 | 1,19 | 1,2 | 1,5 | 2,0 |
| Узбекистан | 203 | 0,58 | 0,5 | 0,5 | 0,5 | 0,57 | 0,6 | 0,5 | 0,5 |
| Болгария | 10 | 0,4 | 0,4 | 0,2 | 0,2 | 0,2 | 0,4 | 0,4 | ? |
| Казахстан | 130 | 0,09 | 0,05 | 0,05 | 0,23 | 0,23 | 0,25 | 0,4 | — |
| Киргизия | 100 | 0,25 | 0,25 | 0,25 | 0,25 | 0,25 | 0,25 | 0,25 | ? |
| Прочие | 1002 | — | — | — | — | — | — | — | — |
| Итого | 11539 | 134,4 | 124,91 | 129,63 | 141,47 | 186,26 | 185,66 | 188,71 |
Генетические группы и промышленные типы месторождений
1. Контактово-метасоматические (скарновые).
2. Гидротермальные.
А. Высокотемпературные (грейзеновые). Б. Среднетемпературные. а. кварц-молибденитовые. б. кварц-сфалерит-галенит-молибденитовые. в. кварц-халькопирит-молибденитовые (меднопорфировые руды). г. настуран-молибденитовые.
История
История металла начинается с Древнего Востока. За две тысячи лет до нашей эры египетские модницы и модники чернили толченой сурьмой брови, подводили веки.
Происхождение русскоязычного термина «сурьма» двояко:
- В Османской империи так именовали порошок металла галенит, которым турчанки чернили брови.
- Персы обозначали словом «сурме» любой металл.
Латинское название вещества восходит к древнегреческому στίμμι. Во времена Средневековья в ходу был термин antimonium. К концу 18 века его ввел в научный оборот и список известных химических элементов «светило» европейской науки Антуан Лавуазье.
Термин Stibium восходит к «стибниту» – так называется природный сульфид сурьмы.
Маркировка нержавеющей стали
В России и странах СНГ принята буквенно-цифровая система, согласно которой цифрами обозначается содержание элементов стали, а буквами — наименование элементов. Общими для всех обозначениями являются буквенные обозначения легирующих элементов: Н — никель, Х — хром, К — кобальт, М — молибден, В — вольфрам, Т — титан, Д — медь, Г — марганец, С — кремний.
Стали нержавеющие стандартные, согласно ГОСТ 5632-72, маркируют буквами и цифрами (например, 08Х18Н10Т). В США существует несколько систем обозначения металлов и их сплавов. Это объясняется наличием нескольких организаций по стандартизации, к ним относятся АMS, ASME, ASTM, AWS, SAE, ACJ, ANSI, AJS. Вполне понятно, что такая маркировка требует дополнительного разъяснения и знания при торговле металлом, оформлении заказов и т. п.
Европа (EN)
Германия (DIN)
США (AISI)
Япония (JIS)
СНГ (ГОСТ)
Из всего многообразия марок мы используем в своём производстве три основные — AISI 304, AISI 316 и AISI 430.